3.8: חלבונים - חומצות אמינו
- Page ID
- 209994
- תאר את המבנה של חומצת אמינו ואת התכונות המקנות את התכונות הספציפיות שלה
מבנה חומצת אמינו
חומצות אמינו הן המונומרים המרכיבים חלבונים. לכל חומצת אמינו אותו מבנה בסיסי, המורכב מאטום פחמן מרכזי, המכונה גם פחמן אלפא (α), הקשור לקבוצת אמינו (NH 2), קבוצת קרבוקסיל (COOH), ולאטום מימן. בסביבה המימית של התא, הן קבוצת האמינו והן קבוצת הקרבוקסיל מיוננים בתנאים פיזיולוגיים, וכך גם המבנים -NH 3 + ו-COO — בהתאמה. לכל חומצת אמינו יש גם אטום או קבוצת אטומים אחרים הקשורים לאטום המרכזי המכונה קבוצת R. קבוצת R זו, או שרשרת צדדית, מעניקה לכל חלבוני חומצת אמינו מאפיינים ספציפיים, כולל גודל, קוטביות ו- pH.

סוגי חומצות אמינו
השם "חומצת אמינו" נגזר מקבוצת האמינו וקבוצת חומצות הקרבוקסיל במבנה הבסיסי שלהם. ישנן 21 חומצות אמינו בחלבונים, שלכל אחת מהן קבוצת R או שרשרת צדדית ספציפית. עשר מהן נחשבות לחומצות אמינו חיוניות בבני אדם מכיוון שגוף האדם אינו יכול לייצר אותן ויש להשיג אותן מהתזונה. לכל האורגניזמים יש חומצות אמינו חיוניות שונות המבוססות על הפיזיולוגיה שלהם.
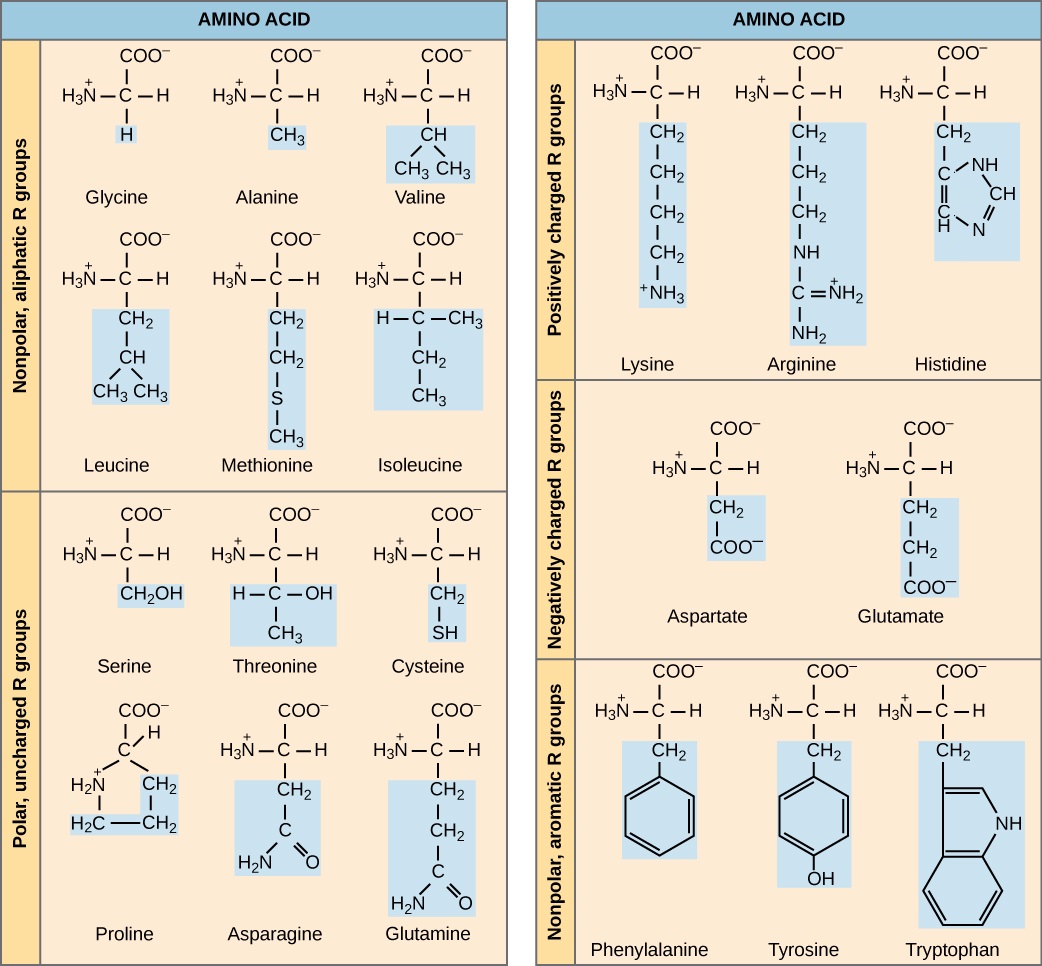
מאפייני חומצות אמינו
אילו קטגוריות של חומצת אמינו היית מצפה למצוא על פני השטח של חלבון מסיס, ואילו היית מצפה למצוא בפנים? איזו התפלגות של חומצות אמינו היית מצפה למצוא בחלבון המוטבע בשכבה דו-שומנית?
ההרכב הכימי של שרשרת הצד קובע את המאפיינים של חומצת האמינו. חומצות אמינו כגון ולין, מתיונין ואלנין אינן קוטביות (הידרופוביות), בעוד שחומצות אמינו כגון סרין, תראונין וציסטאין הן קוטביות (הידרופיליות). שרשראות הצד של ליסין וארגינין טעונות באופן חיובי ולכן חומצות אמינו אלו ידועות גם כחומצות אמינו בסיסיות (pH גבוה). פרולין הוא יוצא מן הכלל למבנה הסטנדרטי של חומצת אמינו מכיוון שקבוצת ה- R שלה מקושרת לקבוצת האמינו ויוצרת מבנה דמוי טבעת.
חומצות אמינו מיוצגות על ידי אות אחת גדולה או קיצור בן שלוש אותיות. לדוגמה, valine ידוע על ידי האות V או סמל שלוש אותיות val.
אג"ח פפטיד
הרצף ומספר חומצות האמינו קובעים בסופו של דבר את צורת החלבון, גודלו ותפקודו. כל חומצת אמינו מחוברת לחומצת אמינו אחרת על ידי קשר קוולנטי, המכונה קשר פפטיד. כאשר שתי חומצות אמינו מחוברות באופן קוולנטי על ידי קשר פפטיד, קבוצת הקרבוקסיל של חומצת אמינו אחת וקבוצת האמינו של חומצת האמינו הנכנסת משלבות ומשחררות מולקולת מים. כל תגובה המשלבת שני מונומרים בתגובה המייצרת H 2 O כאחד התוצרים ידועה כתגובת התייבשות, ולכן היווצרות קשר פפטיד היא דוגמה לתגובת התייבשות.

שרשראות פוליפפטיד
השרשרת המתקבלת של חומצות אמינו נקראת שרשרת פוליפפטיד. לכל פוליפפטיד יש קבוצת אמינו חופשית בקצה אחד. קצה זה נקרא מסוף N, או מסוף האמינו, ובקצה השני יש קבוצת קרבוקסיל חופשית, המכונה גם מסוף C או קרבוקסיל. בעת קריאה או דיווח על רצף חומצות האמינו של חלבון או פוליפפטיד, המוסכמה היא להשתמש בכיוון N-to-C. כלומר, ההנחה היא שחומצת האמינו הראשונה ברצף היא זו במסוף N וההנחה היא שחומצת האמינו האחרונה היא זו שבמסוף C.
למרות שלעתים משתמשים במונחים פוליפפטיד וחלבון לסירוגין, פוליפפטיד הוא מבחינה טכנית כל פולימר של חומצות אמינו, ואילו המונח חלבון משמש לפוליפפטיד או פוליפפטידים שהתקפלו כראוי, בשילוב עם כל הרכיבים הנוספים הדרושים לתפקוד תקין, והוא כעת פונקציונלי.
נקודות מפתח
- כל חומצת אמינו מכילה אטום C מרכזי, קבוצת אמינו (NH2), קבוצת קרבוקסיל (COOH) וקבוצת R ספציפית.
- קבוצת R קובעת את המאפיינים (גודל, קוטביות ו- pH) עבור כל סוג של חומצת אמינו.
- קשרי פפטיד נוצרים בין קבוצת הקרבוקסיל של חומצת אמינו אחת לקבוצת האמינו של אחרת באמצעות סינתזת התייבשות.
- שרשרת של חומצות אמינו היא פוליפפטיד.
מונחי מפתח
- חומצת אמינו: כל אחת מ-20 חומצות α-אמינו המופיעות באופן טבעי (בעלות קבוצות האמינו והחומצה הקרבוקסילית על אותו אטום פחמן), ומגוון שרשראות צד, המשתלבות, באמצעות קשרי פפטיד, ליצירת חלבונים.
- קבוצת R: קבוצת R היא שרשרת צדדית ספציפית לכל חומצת אמינו המקנה תכונות כימיות מסוימות לאותה חומצת אמינו.
- פוליפפטיד: כל פולימר של חומצות אמינו (זהות או שונות) המחוברות באמצעות קשרי פפטיד.


