8.1: אנרגיה, חומר ואנזימים
- Page ID
- 209097
מטרות למידה
- הגדירו ותארו את חילוף החומרים
- השווה והשוואה בין אוטוטרופים והטרוטרופים
- תאר את החשיבות של תגובות הפחתת חמצון בחילוף החומרים
- תאר מדוע ATP, FAD, NAD + ו- NADP+חשובים בתא
- זהה את המבנה והמרכיבים המבניים של אנזים
- תאר את ההבדלים בין מעכבי אנזים תחרותיים ולא תחרותיים
מיקוד קליני: חלק 1
חנה היא ילדה בת 15 חודשים ממדינת וושינגטון. היא מבלה את הקיץ בגמביה, שם הוריה עובדים בארגון לא ממשלתי. כשלושה שבועות לאחר הגעתה לגמביה, התיאבון של חנה החל לרדת והוריה הבחינו שהיא נראית איטית, עייפה ומבולבלת בצורה יוצאת דופן. היא גם נראתה עצבנית מאוד כשהייתה בחוץ, במיוחד במהלך היום. כשהחלה להקיא, הוריה הבינו שהיא נדבקה בנגיף 24 שעות ביממה, אך כאשר הסימפטומים שלה נמשכו, הם לקחו אותה למרפאה. הרופא המקומי הבחין שהרפלקסים של חנה נראים איטיים באופן חריג, וכשבחן את עיניה באור, היא נראתה רגישה לאור בצורה יוצאת דופן. נראה שהיא גם חווה צוואר נוקשה.
תרגיל \(\PageIndex{1}\)
מהן כמה סיבות אפשריות לתסמינים של חנה?
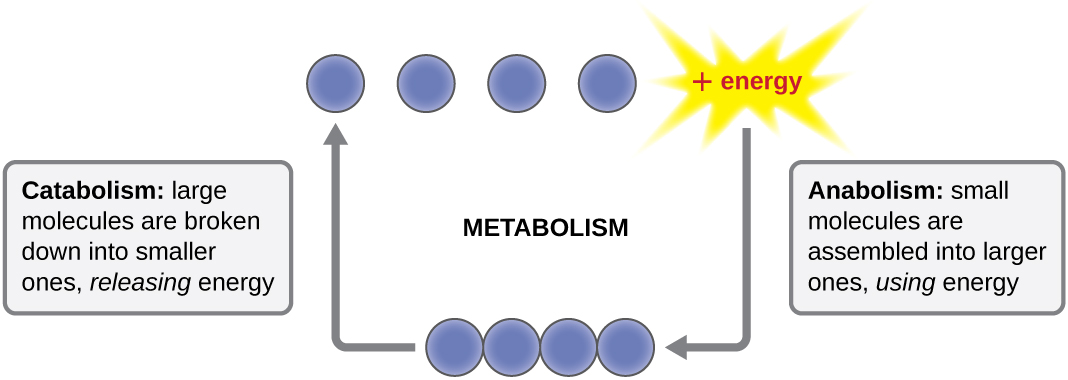
המונח המשמש לתיאור כל התגובות הכימיות בתוך התא הוא חילוף חומרים (איור\(\PageIndex{1}\)). תהליכים תאיים כגון בנייה או פירוק של מולקולות מורכבות מתרחשים באמצעות סדרות של תגובות כימיות מחוברות זו לזו הנקראות מסלולים מטבוליים. תגובות ספונטניות ומשחררות אנרגיה הן תגובות אקסטרגוניות, ואילו תגובות אנדרגוניות דורשות אנרגיה כדי להמשיך. המונח אנבוליזם מתייחס לאותם מסלולים מטבוליים אנדרגוניים המעורבים בביוסינתזה, הממירים אבני בניין מולקולריות פשוטות למולקולות מורכבות יותר, ומונעים על ידי שימוש באנרגיה תאית. לעומת זאת, המונח קטבוליזם מתייחס למסלולים אקסרגוניים המפרקים מולקולות מורכבות לפשוטות יותר. אנרגיה מולקולרית המאוחסנת בקשרים של מולקולות מורכבות משתחררת במסלולים קטבוליים ונקצרת בצורה כזו שניתן להשתמש בה לייצור מולקולות בעלות אנרגיה גבוהה, המשמשות להנעת מסלולים אנבוליים. לפיכך, מבחינת אנרגיה ומולקולות, התאים מאזנים ללא הרף את הקטבוליזם עם אנבוליזם.
סיווג לפי מקור פחמן ואנרגיה
ניתן לזהות אורגניזמים בהתאם למקור הפחמן בו הם משתמשים למטבוליזם וכן למקור האנרגיה שלהם. הקידומות auto- ("עצמי") והטרו- ("אחר") מתייחסות למקורות מקורות הפחמן שאורגניזמים שונים יכולים להשתמש בהם. אורגניזמים הממירים פחמן דו חמצני אנאורגני (CO 2) לתרכובות פחמן אורגניות הם אוטוטרופים. צמחים וציאנובקטריה הם דוגמאות ידועות לאוטוטרופים. לעומת זאת, הטרוטרופים מסתמכים על תרכובות פחמן אורגניות מורכבות יותר כחומרים מזינים; אלה מסופקים להם בתחילה על ידי אוטוטרופים. אורגניזמים רבים, החל מבני אדם ועד פרוקריוטים רבים, כולל Escherichia coli שנחקרו היטב, הם הטרוטרופיים.
ניתן לזהות אורגניזמים גם לפי מקור האנרגיה שהם משתמשים בהם. כל האנרגיה נגזרת מהעברת אלקטרונים, אך מקור האלקטרונים שונה בין סוגים שונים של אורגניזמים. הקידומות צילום- ("אור") וכימו- ("כימי") מתייחסות למקורות האנרגיה בהם משתמשים אורגניזמים שונים. אלה שמקבלים את האנרגיה שלהם להעברת אלקטרונים מאור הם פוטוטרופים, ואילו כימוטרופים משיגים אנרגיה להעברת אלקטרונים על ידי שבירת קשרים כימיים. ישנם שני סוגים של כימוטרופים: אורגנוטרופים וליטוטרופים. אורגנוטרופים, כולל בני אדם, פטריות ופרוקריוטים רבים, הם כימוטרופים שמקבלים אנרגיה מתרכובות אורגניות. ליטוטרופים ("ליטו" פירושו "סלע") הם כימוטרופים שמקבלים אנרגיה מתרכובות אנאורגניות, כולל מימן גופרתי (H 2 S) וברזל מופחת. ליטוטרופיה ייחודית לעולם החיידקים.
ניתן לשלב את האסטרטגיות המשמשות להשגת פחמן ואנרגיה לסיווג אורגניזמים לפי סוג התזונה. רוב האורגניזמים הם כימוהטרוטרופים מכיוון שהם משתמשים במולקולות אורגניות כמקורות האלקטרונים והפחמן שלהם. טבלה \(\PageIndex{1}\) מסכמת את זה ואת הסיווגים האחרים.
| סיווגים | מקור אנרגיה | מקור פחמן | דוגמאות | |
|---|---|---|---|---|
| כימוטרופים | כימואוטוטרופים | כימי | אנאורגני | חיידקים מחמצנים מימן, גופרית, ברזל, חנקן ופחמן חד חמצני |
| כימוהטרוטרופים | כימי | תרכובות אורגניות | כל בעלי החיים, רוב הפטריות, הפרוטוזואה והחיידקים | |
| פוטוטרופים | פוטואוטוטרופים | אור | אנאורגני | כל הצמחים, האצות, הציאנובקטריה וחיידקי הגופרית הירוקה והסגולה |
| פוטוהטרוטרופים | אור | תרכובות אורגניות | חיידקים לא גופרית ירוקים וסגולים, הליובקטריה | |
תרגיל \(\PageIndex{2}\)
- הסבר את ההבדל בין קטבוליזם לאנבוליזם.
- הסבר את ההבדל בין אוטוטרופים להטרוטרופים.
חמצון והפחתה בחילוף החומרים
העברת האלקטרונים בין מולקולות חשובה מכיוון שרוב האנרגיה המאוחסנת באטומים ומשמשת לתפקודי תאי דלק היא בצורה של אלקטרונים בעלי אנרגיה גבוהה. העברת האנרגיה בצורה של אלקטרונים מאפשרת לתא להעביר ולהשתמש באנרגיה באופן הדרגתי; כלומר באריזות קטנות ולא בפרץ הרסני יחיד. תגובות שמסירות אלקטרונים ממולקולות התורם, ומשאירות אותן מחומצנות, הן תגובות חמצון; אלה שמוסיפים אלקטרונים למולקולות המקבלות, ומשאירים אותם מופחתים, הם תגובות הפחתה. מכיוון שאלקטרונים יכולים לעבור ממולקולה אחת לאחרת, חמצון והפחתה מתרחשים במקביל. זוגות התגובות הללו נקראים תגובות להפחתת חמצון, או תגובות חיזור.
נושאי אנרגיה: NAD +, NADP +, FAD ו- ATP
ניתן לאחסן את האנרגיה המשתחררת מפירוק הקשרים הכימיים בתוך חומרים מזינים באמצעות הפחתת נשאי אלקטרונים או בקשרים של אדנוסין טריפוספט (ATP). במערכות חיות, סוג קטן של תרכובות מתפקד כנשאי אלקטרונים ניידים, מולקולות הנקשרות ומעבירות אלקטרונים בעלי אנרגיה גבוהה בין תרכובות במסלולים. נשאי האלקטרונים העיקריים שנשקול מקורם בקבוצת ויטמין B והם נגזרות של נוקלאוטידים; הם ניקוטינאמיד אדנין דינוקלאוטיד, ניקוטין אדנין דינוקלאוטיד פוספט ופלבין אדנין דינוקלאוטיד. ניתן להפחית או לחמצן תרכובות אלה בקלות. ניקוטינאמיד אדנין דינוקלאוטיד (NAD + /NADH) הוא נושא האלקטרונים הנייד הנפוץ ביותר המשמש בקטבוליזם. NAD + היא הצורה המחומצנת של המולקולה; NADH היא הצורה המופחתת של המולקולה. ניקוטין אדנין דינוקלאוטיד פוספט (NADP +), הצורה המחומצנת של גרסת NAD + המכילה קבוצת פוספט נוספת, היא נושאת אלקטרונים חשובה נוספת; הוא יוצר NADPH כאשר הוא מופחת. הצורה המחומצנת של פלבין אדנין דינוקלאוטיד היא FAD, וצורתו המופחתת היא FADH 2. גם NAD + /NADH וגם FAD/FADH 2 נמצאים בשימוש נרחב בהפקת אנרגיה מסוכרים במהלך קטבוליזם בכימוהטרוטרופים, ואילו NADP + /NADPH ממלא תפקיד חשוב בתגובות אנבוליות ובפוטוסינתזה. באופן קולקטיבי, FADH 2, NADH ו-NADPH מכונים לעתים קרובות כבעלי כוח מפחית בשל יכולתם לתרום אלקטרונים לתגובות כימיות שונות.
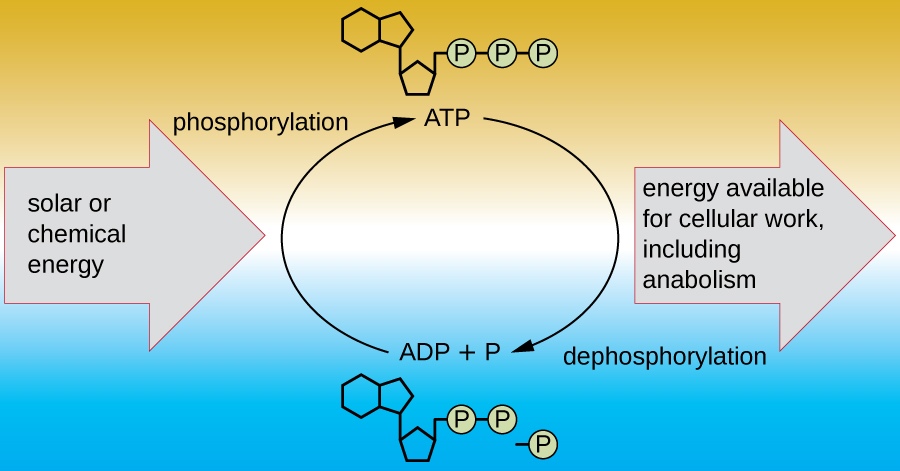
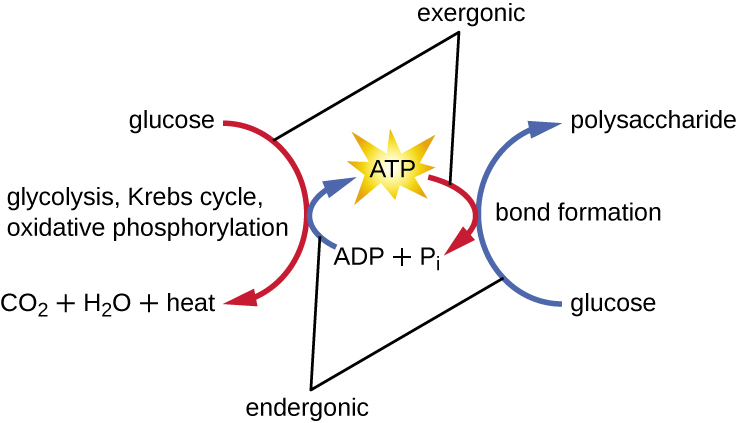
תא חי חייב להיות מסוגל להתמודד עם האנרגיה המשתחררת במהלך הקטבוליזם באופן המאפשר לתא לאגור אנרגיה בבטחה ולשחרר אותה לשימוש רק לפי הצורך. תאים חיים משיגים זאת באמצעות התרכובת אדנוסין טריפוספט (ATP). ATP נקרא לעתים קרובות "מטבע האנרגיה" של התא, וכמו מטבע, ניתן להשתמש בתרכובת רב-תכליתית זו למילוי כל צורך אנרגטי של התא. בלב ה- ATP נמצאת מולקולה של אדנוסין מונופוספט (AMP), המורכבת ממולקולת אדנין המחוברת למולקולת ריבוז וקבוצת פוספט אחת. ריבוז הוא סוכר בעל חמישה פחמנים המצוי ב- RNA, ו- AMP הוא אחד הנוקלאוטידים ב- RNA. הוספת קבוצת פוספט שנייה למולקולת ליבה זו גורמת להיווצרות אדנוסין דיפוספט (ADP); תוספת של קבוצת פוספט שלישית יוצרת ATP (איור). \(\PageIndex{2}\) הוספת קבוצת פוספט למולקולה, תהליך הנקרא זרחון, דורשת אנרגיה. קבוצות פוספט טעונות שלילי ובכך דוחות זו את זו כשהן מסודרות בסדרות, כפי שהן ב-ADP ו-ATP. דחייה זו הופכת את מולקולות ה- ADP וה- ATP לבלתי יציבות מטבען. לפיכך, הקשרים בין קבוצות פוספט (אחת ב- ADP ושניים ב- ATP) נקראים קשרי פוספט בעלי אנרגיה גבוהה. כאשר קשרים בעלי אנרגיה גבוהה אלה נשברים כדי לשחרר פוספט אחד (הנקרא פוספט אנאורגני [P i]) או שתי קבוצות פוספט מחוברות (הנקראות פירופוספט [PP i]) מ-ATP באמצעות תהליך הנקרא דה-פוספורילציה, משתחררת אנרגיה להנעת תגובות אנדרגוניות (איור). \(\PageIndex{3}\)
תרגיל \(\PageIndex{3}\)
מה תפקידו של נושא אלקטרונים?
מבנה ותפקוד האנזים
חומר המסייע להאיץ תגובה כימית הוא זרז. זרזים אינם משמשים או משתנים במהלך תגובות כימיות, ולכן הם ניתנים לשימוש חוזר. בעוד שמולקולות אנאורגניות עשויות לשמש זרזים למגוון רחב של תגובות כימיות, חלבונים הנקראים אנזימים משמשים כזרזים לתגובות ביוכימיות בתוך התאים. אנזימים ממלאים אפוא תפקיד חשוב בשליטה על חילוף החומרים התאי.
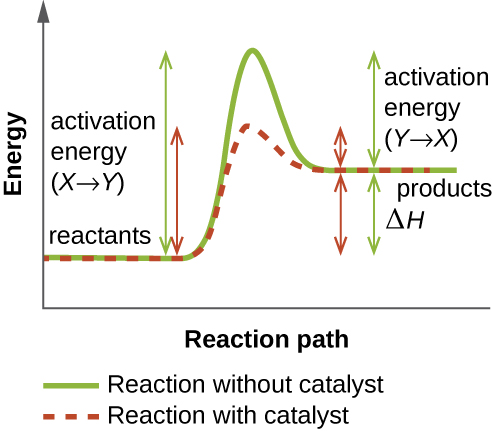
אנזים מתפקד על ידי הורדת אנרגיית ההפעלה של תגובה כימית בתוך התא. אנרגיית הפעלה היא האנרגיה הדרושה ליצירת או שבירת קשרים כימיים ולהמרת מגיבים למוצרים (איור\(\PageIndex{4}\)). אנזימים מורידים את אנרגיית ההפעלה על ידי קישור למולקולות המגיבות ומחזיקים אותן באופן שיאיץ את התגובה.
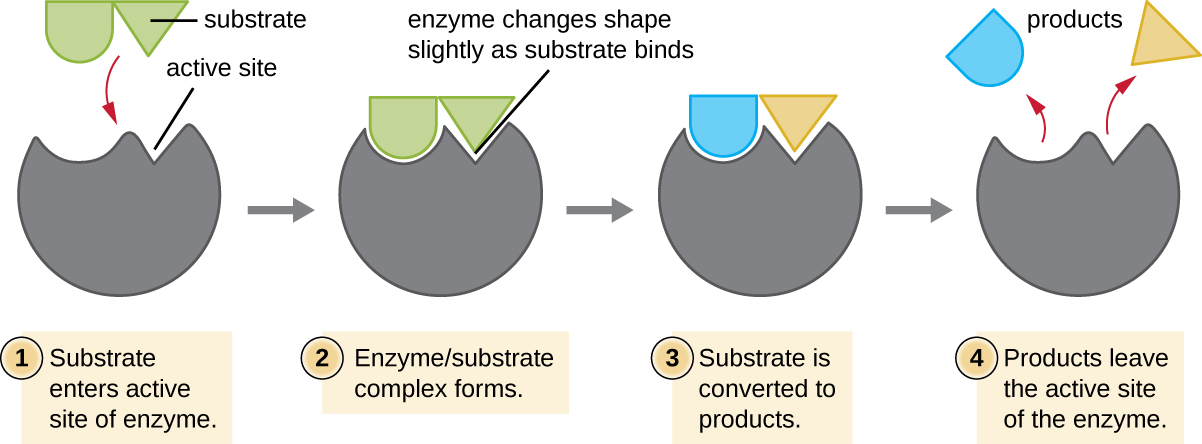
המגיבים הכימיים שאליהם נקשר אנזים נקראים מצעים, והמיקום בתוך האנזים שבו נקשר המצע נקרא האתר הפעיל של האנזים. המאפיינים של חומצות האמינו ליד האתר הפעיל יוצרים סביבה כימית מאוד ספציפית בתוך האתר הפעיל המשרה התאמה לקשירה, אם כי בקצרה, למצע (או מצעים) ספציפיים. בשל התאמה דמוית פאזל זו בין אנזים למצעים שלו, אנזימים ידועים בספציפיות שלהם. למעשה, כאשר אנזים נקשר למצע (ים) שלו, מבנה האנזים משתנה מעט כדי למצוא את ההתאמה הטובה ביותר בין מצב המעבר (תוצר ביניים מבני בין המצע למוצר) לבין האתר הפעיל, בדיוק כפי שמתעצבת כפפת גומי יד המוחדרת לתוכו. שינוי אתר פעיל זה בנוכחות מצע, יחד עם היווצרות סימולטנית של מצב המעבר, נקרא התאמה מושרה (איור\(\PageIndex{5}\)). בסך הכל, יש אנזים מותאם במיוחד לכל מצע, ולפיכך לכל תגובה כימית; עם זאת, יש גם גמישות מסוימת. לאנזימים מסוימים יש את היכולת לפעול על מספר מצעים שונים הקשורים למבנה.
אנזימים נתונים להשפעות על ידי תנאי סביבה מקומיים כגון pH, ריכוז המצע וטמפרטורה. למרות שהעלאת הטמפרטורה הסביבתית בדרך כלל מגבירה את קצבי התגובה, אנזים מזורז או אחר, הגדלה או הפחתה של הטמפרטורה מחוץ לטווח אופטימלי יכולה להשפיע על קשרים כימיים בתוך האתר הפעיל, מה שהופך אותם פחות מתאימים לקשירת מצעים. טמפרטורות גבוהות יגרמו בסופו של דבר לאנזימים, כמו מולקולות ביולוגיות אחרות, להתנתק, לאבד את המבנה והתפקוד התלת מימדי שלהם. אנזימים מתאימים גם לתפקוד הטוב ביותר בטווח pH מסוים, וכמו בטמפרטורה, ערכי pH סביבתיים קיצוניים (חומציים או בסיסיים) יכולים לגרום לאנזימים להתנתק. לשרשראות צד של חומצות אמינו באתר פעיל יש תכונות חומציות או בסיסיות משלהן האופטימליות לקטליזה ולכן רגישות לשינויים ב-pH.
גורם נוסף המשפיע על פעילות האנזים הוא ריכוז המצע: פעילות האנזים מוגברת בריכוזים גבוהים יותר של מצע עד שהיא מגיעה לנקודת רוויה שבה האנזים אינו יכול לקשור מצע נוסף. בסך הכל, אנזימים מותאמים לעבודה הטובה ביותר בתנאים הסביבתיים שבהם חיים האורגניזמים המייצרים אותם. לדוגמה, בעוד שלחיידקים המאכלסים מעיינות חמים יש אנזימים הפועלים בצורה הטובה ביותר בטמפרטורות גבוהות, לפתוגנים אנושיים יש אנזימים הפועלים בצורה הטובה ביותר ב-37 מעלות צלזיוס באופן דומה, בעוד שאנזימים המיוצרים על ידי רוב האורגניזמים פועלים בצורה הטובה ביותר ב-pH ניטרלי, חיידקים הגדלים בסביבות חומציות מייצרים אנזימים מותאמים לתנאי pH נמוכים, ומאפשרים את צמיחתם בתנאים אלה.
אנזימים רבים אינם פועלים בצורה אופטימלית, או אפילו בכלל, אלא אם כן הם נקשרים למולקולות עוזרות ספציפיות אחרות שאינן חלבון, באופן זמני דרך קשרים יוניים או מימן או לצמיתות באמצעות קשרים קוולנטיים חזקים יותר. קשירה למולקולות אלו מקדמת קונפורמציה ותפקוד מיטביים עבור האנזימים שלהם. שני סוגים של מולקולות עוזרות הן קופקטורים וקו-אנזימים. קופקטורים הם יונים אנאורגניים כגון ברזל (Fe 2+) ומגנזיום (Mg 2+) המסייעים בייצוב קונפורמציה ותפקוד האנזים. דוגמה אחת לאנזים הדורש יון מתכת כקופקטור היא האנזים הבונה מולקולות DNA, פולימראז DNA, הדורש יון אבץ קשור (Zn 2+) לתפקד.
קואנזימים הם מולקולות עוזר אורגניות הנדרשות לפעולת האנזים. כמו אנזימים, הם אינם נצרכים, ולכן, הם לשימוש חוזר. המקורות הנפוצים ביותר לקואנזימים הם ויטמינים תזונתיים. חלק מהוויטמינים הם מבשרי קואנזימים ואחרים פועלים ישירות כקואנזימים.
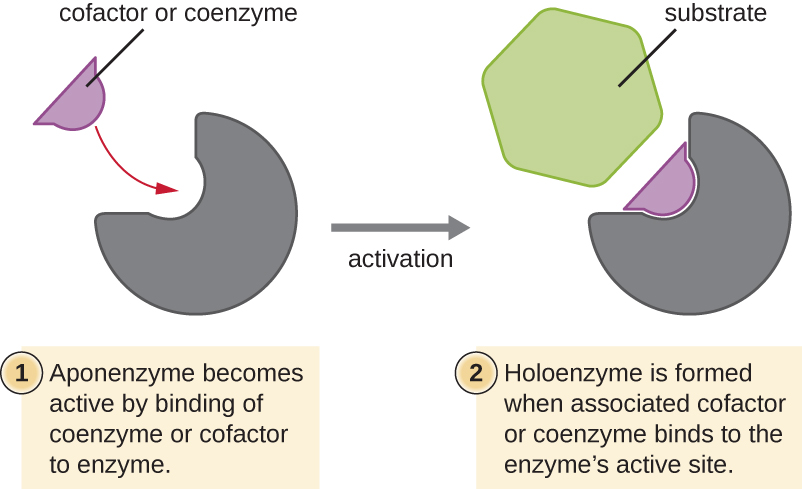
כמה קו-פקטורים וקו-אנזימים, כמו קואנזים A (CoA), נקשרים לעתים קרובות לאתר הפעיל של האנזים, ומסייעים בכימיה של המעבר של מצע למוצר (איור). \(\PageIndex{6}\) במקרים כאלה, אנזים חסר קופקטור או קואנזים נחוץ נקרא אפואנזים ואינו פעיל. לעומת זאת, אנזים עם הקופקטור או הקואנזים הקשורים אליו נקרא הולואנזים והוא פעיל. NADH ו-ATP הן גם דוגמאות לקו-אנזימים נפוצים המספקים אלקטרונים בעלי אנרגיה גבוהה או קבוצות פוספט, בהתאמה, הנקשרים לאנזימים, ובכך מפעילים אותם.
תרגיל \(\PageIndex{4}\)
איזה תפקיד ממלאים אנזימים בתגובה כימית?
מעכבי אנזים
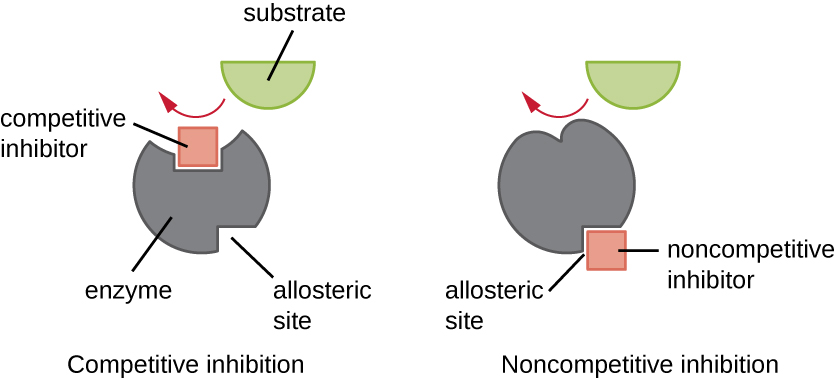
ניתן לווסת אנזימים בדרכים המקדמות או מפחיתות את פעילותם. ישנם סוגים רבים ושונים של מולקולות המעכבות או מקדמות את תפקוד האנזים, וקיימים מנגנונים שונים לשם כך (איור\(\PageIndex{7}\)). מעכב תחרותי הוא מולקולה הדומה מספיק למצע כדי שתוכל להתחרות במצע על הקישור לאתר הפעיל פשוט על ידי חסימת המצע מלהיקשר. כדי שמעכב תחרותי יהיה יעיל, ריכוז המעכב צריך להיות שווה בערך לריכוז המצע. תרופות סולפה מספקות דוגמה טובה לתחרות תחרותית. הם משמשים לטיפול בזיהומים חיידקיים מכיוון שהם נקשרים לאתר הפעיל של אנזים בתוך מסלול סינתזת החומצה הפולית החיידקית. כאשר היא קיימת במינון מספיק, תרופת סולפה מונעת סינתזה של חומצה פולית, וחיידקים אינם מסוגלים לצמוח מכיוון שהם אינם יכולים לסנתז DNA, RNA וחלבונים. בני אדם אינם מושפעים מכיוון שאנו משיגים חומצה פולית מהתזונה שלנו.
מצד שני, מעכב לא תחרותי (אלוסטרי) נקשר לאנזים באתר אלוסטרי, מיקום שאינו האתר הפעיל, ועדיין מצליח לחסום את קישור המצע לאתר הפעיל על ידי גרימת שינוי קונפורמטיבי המפחית את הזיקה של האנזים למצע שלו (איור). \(\PageIndex{8}\) מכיוון שיש צורך רק במולקולת מעכב אחת לכל אנזים לצורך עיכוב יעיל, ריכוז המעכבים הדרושים לעיכוב לא תחרותי הוא בדרך כלל נמוך בהרבה מריכוז המצע.
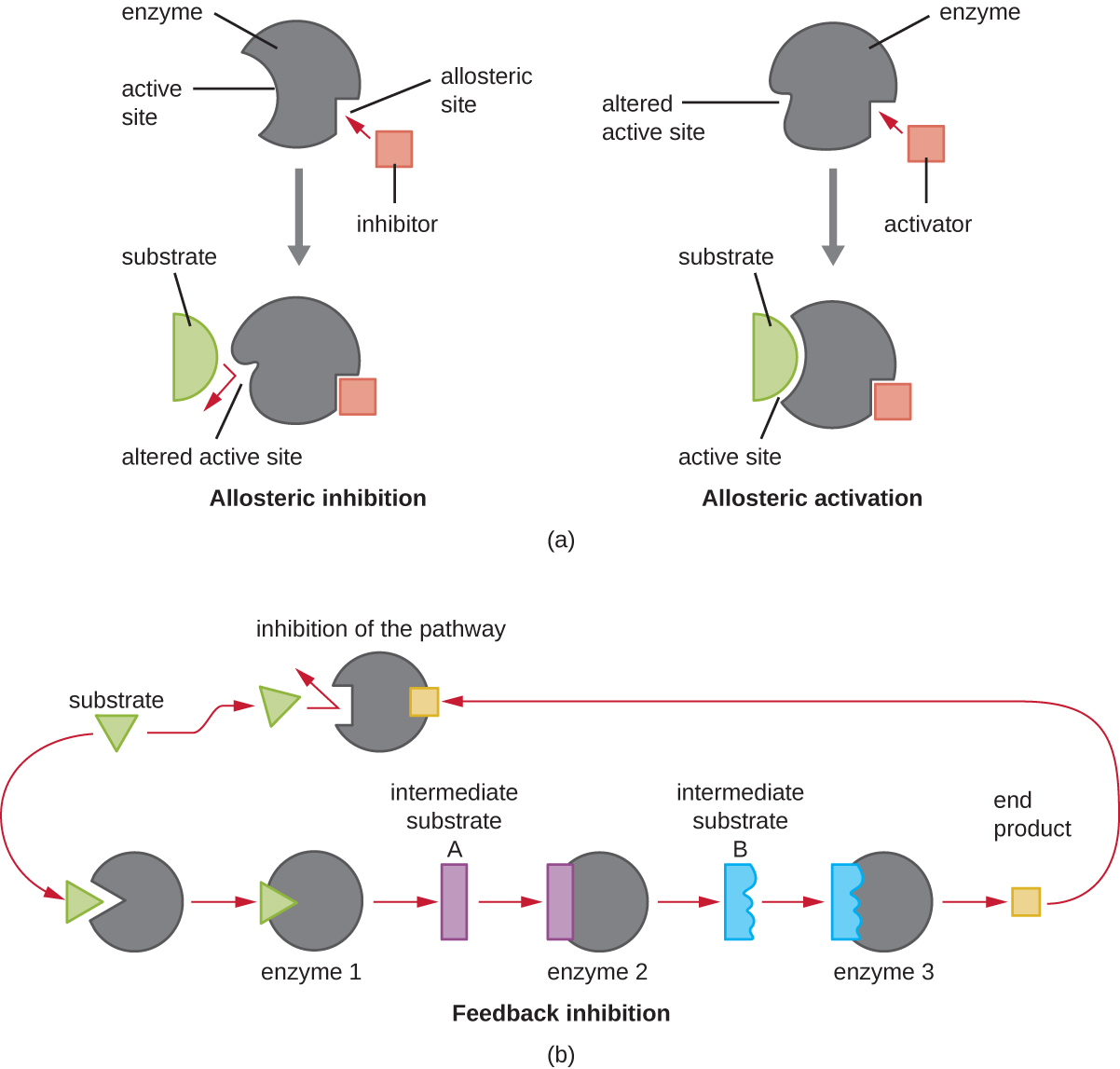
בנוסף למעכבים אלוסטריים, ישנם מפעילים אלוסטריים הנקשרים למיקומים באנזים הרחק מהאתר הפעיל, וגורמים לשינוי קונפורמטיבי המגביר את הזיקה של האתרים הפעילים של האנזים למצע (ים) שלו.
שליטה אלוסטרית היא מנגנון חשוב לוויסות מסלולים מטבוליים המעורבים הן בקטבוליזם והן באנבוליזם. בצורה היעילה והאלגנטית ביותר, תאים התפתחו גם כדי להשתמש במוצרים של תגובות מטבוליות משלהם לעיכוב משוב של פעילות האנזים. עיכוב משוב כרוך בשימוש במוצר מסלול כדי לווסת את המשך הייצור שלו. התא מגיב לשפע המוצרים הספציפיים על ידי האטת הייצור במהלך תגובות אנבוליות או קטבוליות (איור\(\PageIndex{8}\)).
תרגיל \(\PageIndex{5}\)
הסבר את ההבדל בין מעכב תחרותי לבין מעכב לא תחרותי.
מושגי מפתח וסיכום
- חילוף החומרים כולל תגובות כימיות המפרקות מולקולות מורכבות (קטבוליזם) וכאלה הבונות מולקולות מורכבות (אנבוליזם).
- ניתן לסווג אורגניזמים לפי מקור הפחמן שלהם. אוטוטרופים ממירים פחמן דו חמצני אנאורגני לפחמן אורגני; הטרוטרופים משתמשים בתרכובות פחמן אורגניות קבועות.
- ניתן לסווג אורגניזמים גם לפי מקור האנרגיה שלהם. פוטוטרופים משיגים את האנרגיה שלהם מאור. כימוטרופים מקבלים את האנרגיה שלהם מתרכובות כימיות. אורגנוטרופים משתמשים במולקולות אורגניות, וליטוטרופים משתמשים בכימיקלים אנאורגניים.
- נשאי אלקטרונים סלולריים מקבלים אלקטרונים בעלי אנרגיה גבוהה ממזונות ובהמשך משמשים כתורמי אלקטרונים בתגובות חיזור עוקבות. FAD/FADH 2, NAD + /NADH ו - NADP + /NADPH הם נושאי אלקטרונים חשובים.
- אדנוסין טריפוספט (ATP) משמש כמטבע האנרגיה של התא, אוגר בבטחה אנרגיה כימית בשני קשרי הפוספט עתירי האנרגיה שלו לשימוש מאוחר יותר להנעת תהליכים הדורשים אנרגיה.
- אנזימים הם זרזים ביולוגיים המגבירים את קצב התגובות הכימיות בתוך התאים על ידי הורדת אנרגיית ההפעלה הנדרשת להמשך התגובה.
- בטבע, תגובות אקסטרגוניות אינן דורשות אנרגיה מעבר לאנרגיית ההפעלה כדי להמשיך, והן משחררות אנרגיה. הם עשויים להתקדם ללא אנזימים, אך בקצב איטי. לעומת זאת, תגובות אנדרגוניות דורשות אנרגיה מעבר לאנרגיית ההפעלה כדי להתרחש. בתאים, תגובות אנדרגוניות מחוברות לתגובות אקסרגוניות, מה שהופך את השילוב לטובה מבחינה אנרגטית.
- מצעים נקשרים לאתר הפעיל של האנזים. תהליך זה בדרך כלל משנה את המבנים של האתר הפעיל ושל המצע, ומעדיף היווצרות מצב מעבר; זה ידוע בשם התאמה מושרה.
- קופקטורים הם יונים אנאורגניים המייצבים את הקונפורמציה והתפקוד של האנזים. קואנזימים הם מולקולות אורגניות הנדרשות לתפקוד תקין של האנזים ולעתים קרובות נגזרות מוויטמינים. אנזים חסר קופקטור או קואנזים הוא אפואנזים; אנזים עם קופקטור קשור או קואנזים הוא הולואנזים.
- מעכבים תחרותיים מווסתים אנזימים על ידי קישור לאתר הפעיל של האנזים, ומונעים קישור מצע. מעכבים לא תחרותיים (אלוסטריים) נקשרים לאתרים אלוסטריים, וגורמים לשינוי קונפורמטיבי באנזים המונע ממנו לתפקד. עיכוב משוב מתרחש כאשר התוצר של מסלול מטבולי נקשר באופן לא תחרותי לאנזים בשלב מוקדם של המסלול, ובסופו של דבר מונע את הסינתזה של המוצר.


