9.3: תגובה לאות
- Page ID
- 205789
מיומנויות לפיתוח
- תאר כיצד מסלולי איתות מכוונים ביטוי חלבון, מטבוליזם תאי וצמיחת תאים
- זהה את הפונקציה של PKC במסלולי העברת אותות
- הכירו בתפקיד האפופטוזיס בפיתוח ותחזוקה של אורגניזם בריא
בתוך התא, ליגנדים נקשרים לקולטנים הפנימיים שלהם, ומאפשרים להם להשפיע ישירות על ה- DNA והמכונות לייצור החלבון של התא. באמצעות מסלולי העברת אותות, קולטנים בקרום הפלזמה מייצרים מגוון השפעות על התא. התוצאות של מסלולי איתות מגוונות ביותר ותלויות בסוג התא המעורב וכן בתנאים החיצוניים והפנימיים. דגימה קטנה של תגובות מתוארת להלן.
ביטוי גנים
כמה מסלולי העברת אותות מווסתים את התעתיק של RNA. אחרים מווסתים את התרגום של חלבונים מ-mRNA. דוגמה לחלבון המווסת את התרגום בגרעין הוא MAP kinase ERK. ERK מופעל במפל זרחון כאשר גורם גדילה אפידרמיס (EGF) קושר את קולטן EGF (ראה איור 9.2.1). עם זרחון, ERK נכנס לגרעין ומפעיל חלבון קינאז שבתורו מווסת את תרגום החלבון (איור). \(\PageIndex{1}\)
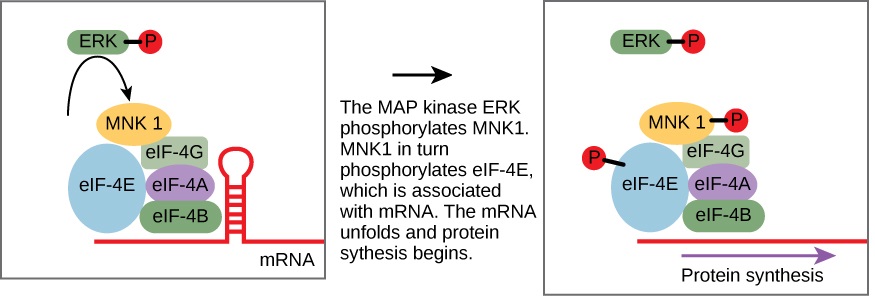
הסוג השני של חלבון איתו PKC יכול לקיים אינטראקציה הוא חלבון הפועל כמעכב. מעכב הוא מולקולה הנקשרת לחלבון ומונעת ממנו לתפקד או מפחיתה את תפקודו. במקרה זה, המעכב הוא חלבון הנקרא Iκ-B, הנקשר לחלבון הרגולטורי NF-κB. (הסמל κ מייצג את האות היוונית קאפה.) כאשר Iκ-B קשור ל-NF-κB, הקומפלקס אינו יכול להיכנס לגרעין התא, אך כאשר Iκ-B מזורחן על ידי PKC, הוא אינו יכול עוד לקשור NF-κB, ו-NF-κB (גורם שעתוק) יכול להיכנס לגרעין וליזום שעתוק RNA. במקרה זה, ההשפעה של זרחון היא להשבית מעכב ובכך להפעיל את תהליך השעתוק.
עלייה בחילוף החומרים הסלולרי
התוצאה של מסלול איתות אחר משפיעה על תאי השריר. הפעלת קולטני β-אדרנרגיים בתאי השריר על ידי אדרנלין מובילה לעלייה ב- AMP מחזורי (cAMP) בתוך התא. הידוע גם בשם אפינפרין, אדרנלין הוא הורמון (המיוצר על ידי בלוטת יותרת הכליה המחוברת לכליה) שמכין את הגוף למקרי חירום לטווח קצר. AMP מחזורי מפעיל PKA (חלבון קינאז A), אשר בתורו מזרחן שני אנזימים. האנזים הראשון מקדם את פירוק הגליקוגן על ידי הפעלת גליקוגן פוספורילאז קינאז ביניים (GPK) שבתורו מפעיל גליקוגן פוספורילאז (GP) המפרק את הגליקוגן לגלוקוז. (נזכיר שגופך ממיר עודף גלוקוז לגליקוגן לאחסון לטווח קצר. כאשר יש צורך באנרגיה, הגליקוגן הופך במהירות לגלוקוז.) זרחון של האנזים השני, גליקוגן סינתאז (GS), מעכב את יכולתו ליצור גליקוגן מגלוקוז. באופן זה, תא שריר משיג מאגר מוכן של גלוקוז על ידי הפעלת היווצרותו באמצעות פירוק גליקוגן ועל ידי עיכוב השימוש בגלוקוז ליצירת גליקוגן, ובכך מונע מחזור חסר תועלת של פירוק וסינתזה של גליקוגן. לאחר מכן הגלוקוז זמין לשימוש על ידי תא השריר בתגובה לעלייה פתאומית של אדרנלין - רפלקס "הילחם או ברח".
צמיחת תאים
מסלולי איתות תאים ממלאים גם תפקיד מרכזי בחלוקת התא. תאים אינם מתחלקים בדרך כלל אלא אם כן הם מעוררים על ידי אותות מתאי אחרים. הליגנדים המקדמים צמיחת תאים נקראים גורמי גדילה. רוב גורמי הגדילה נקשרים לקולטנים על פני התא המקושרים לטירוסין קינאזות. קולטנים אלה על פני התא נקראים קולטן טירוסין קינאזות (RTKs). הפעלת RTKs יוזמת מסלול איתות הכולל חלבון G בשם RAS, המפעיל את מסלול MAP kinase שתואר קודם לכן. לאחר מכן האנזים MAP kinase מגרה את הביטוי של חלבונים המקיימים אינטראקציה עם רכיבים תאיים אחרים כדי ליזום חלוקת תאים.
קשר לקריירה: ביולוג סרטן
ביולוגים של סרטן חוקרים את המקורות המולקולריים של סרטן במטרה לפתח שיטות מניעה ואסטרטגיות טיפול חדשות שיעכבו את צמיחת הגידולים מבלי לפגוע בתאים התקינים בגוף. כפי שהוזכר קודם לכן, מסלולי איתות שולטים בצמיחת התאים. מסלולי איתות אלה נשלטים על ידי חלבוני איתות, אשר בתורם באים לידי ביטוי על ידי גנים. מוטציות בגנים אלה עלולות לגרום לחלבוני איתות לא תקינים. זה מונע מהתא לווסת את מחזור התא שלו, ומפעיל חלוקת תאים בלתי מוגבלת וסרטן. הגנים המווסתים את חלבוני האיתות הם סוג אחד של אונקוגן שהוא גן שיש לו פוטנציאל לגרום לסרטן. הגן המקודד ל- RAS הוא אונקוגן שהתגלה במקור כאשר מוטציות בחלבון RAS נקשרו לסרטן. מחקרים נוספים הצביעו על כך של-30 אחוז מתאי הסרטן יש מוטציה בגן RAS המובילה לצמיחה בלתי מבוקרת. אם לא נבדקים, חלוקת תאים בלתי מבוקרת עלולה להוביל להיווצרות גידולים וגרורות, צמיחת תאים סרטניים במקומות חדשים בגוף.
ביולוגים של סרטן הצליחו לזהות אונקוגנים רבים אחרים התורמים להתפתחות סרטן. לדוגמה, HER2 הוא קולטן משטח התא שנמצא בכמויות מוגזמות ב -20 אחוז ממקרי סרטן השד האנושיים. ביולוגים של סרטן הבינו ששכפול גנים הוביל לביטוי יתר של HER2 ב -25% מחולי סרטן השד ופיתחו תרופה בשם Herceptin (trastuzumab). הרספטין הוא נוגדן חד שבטי המכוון ל-HER2 להסרה על ידי המערכת החיסונית. טיפול בהרספטין עוזר לשלוט באיתות באמצעות HER2. השימוש בהרספטין בשילוב עם כימותרפיה סייע להגדיל את שיעור ההישרדות הכולל של חולים עם סרטן שד גרורתי.
מוות תאי
כאשר תא פגום, מיותר או שעלול להיות מסוכן לאורגניזם, תא יכול ליזום מנגנון להפעלת מוות תאי מתוכנת, או אפופטוזיס. אפופטוזיס מאפשר לתא למות בצורה מבוקרת המונעת שחרור של מולקולות שעלולות להזיק מתוך התא. ישנם מחסומים פנימיים רבים העוקבים אחר בריאות התא; אם נצפים חריגות, תא יכול ליזום באופן ספונטני את תהליך האפופטוזיס. עם זאת, במקרים מסוימים, כמו זיהום נגיפי או חלוקת תאים בלתי מבוקרת כתוצאה מסרטן, הבדיקות והאיזונים התקינים של התא נכשלים. איתות חיצוני יכול גם ליזום אפופטוזיס. לדוגמה, לרוב תאי בעלי החיים הרגילים יש קולטנים המקיימים אינטראקציה עם המטריצה החוץ -תאית, רשת של גליקופרוטאינים המספקת תמיכה מבנית לתאים באורגניזם. הקישור של קולטנים תאיים למטריצה החוץ -תאית יוזם מפל איתות בתוך התא. עם זאת, אם התא מתרחק מהמטריצה החוץ תאית, האיתות נפסק, והתא עובר אפופטוזיס. מערכת זו מונעת מהתאים לנוע בגוף ולהתרבות ללא שליטה, כפי שקורה בתאי גידול שגוררים גרורות.
דוגמה נוספת לאיתות חיצוני המוביל לאפופטוזיס מתרחשת בהתפתחות תאי T. תאי T הם תאי חיסון הנקשרים למקרומולקולות וחלקיקים זרים, ומכוונים אותם להרס על ידי מערכת החיסון. בדרך כלל, תאי T אינם מכוונים לחלבונים "עצמיים" (אלה של האורגניזם שלהם), תהליך שיכול להוביל למחלות אוטואימוניות. על מנת לפתח את היכולת להבחין בין עצמי ללא עצמי, תאי T לא בשלים עוברים בדיקה כדי לקבוע אם הם נקשרים לחלבונים עצמיים כביכול. אם הקולטן לתאי T נקשר לחלבונים עצמיים, התא יוזם אפופטוזיס כדי להסיר את התא שעלול להיות מסוכן.
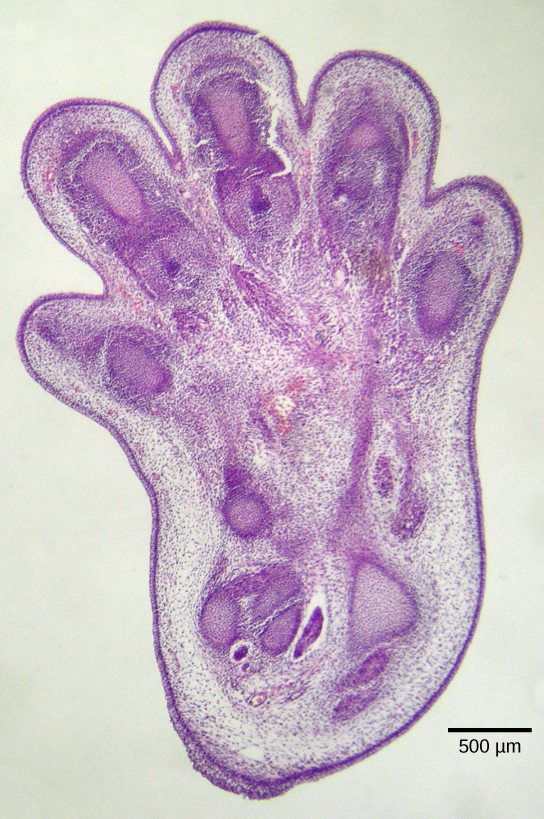
אפופטוזיס חיוני גם להתפתחות אמבריולוגית תקינה. בבעלי חוליות, למשל, שלבי התפתחות מוקדמים כוללים היווצרות רקמה דמוית רשת בין אצבעות ואצבעות בודדות (איור\(\PageIndex{2}\)). במהלך ההתפתחות התקינה, יש לחסל את התאים הלא נחוצים הללו, מה שמאפשר להיווצר אצבעות ובהונות מופרדות לחלוטין. מנגנון איתות תאים מעורר אפופטוזיס, ההורס את התאים בין הספרות המתפתחות.
סיום מפל האותות
האיתות החריג הנראה לעתים קרובות בתאי הגידול הוא הוכחה לכך שסיום האות בזמן המתאים יכול להיות חשוב לא פחות מהתחלת האות. שיטה אחת לעצירת אות ספציפי היא לפרק את הליגנד או להסיר אותו כך שהוא כבר לא יוכל לגשת לקולטן שלו. אחת הסיבות לכך שהורמונים הידרופוביים כמו אסטרוגן וטסטוסטרון מעוררים אירועים ארוכי טווח היא מכיוון שהם קושרים חלבונים נשאים. חלבונים אלה מאפשרים למולקולות הבלתי מסיסות להיות מסיסות בדם, אך הם גם מגנים על ההורמונים מפני פירוק על ידי אנזימים במחזור הדם.
בתוך התא, אנזימים רבים ושונים הופכים את השינויים התאיים הנובעים ממפלי איתות. לדוגמה, פוספטאזות הם אנזימים המסירים את קבוצת הפוספטים המחוברת לחלבונים על ידי קינאזות בתהליך הנקרא דה-פוספורילציה. AMP מחזורי (cAMP) מתפרק ל- AMP על ידי פוספודיאסטרז, ושחרור מאגרי הסידן מתהפך על ידי משאבות Ca 2+ הממוקמות בממברנות החיצוניות והפנימיות של התא.
סיכום
התחלת מסלול איתות היא תגובה לגירויים חיצוניים. תגובה זו יכולה ללבוש צורות רבות ושונות, כולל סינתזת חלבון, שינוי בחילוף החומרים של התא, צמיחת תאים או אפילו מוות של תאים. מסלולים רבים משפיעים על התא על ידי התחלת ביטוי גנים, והשיטות בהן נעשה שימוש הן רבות למדי. חלק מהמסלולים מפעילים אנזימים המקיימים אינטראקציה עם גורמי שעתוק DNA. אחרים משנים חלבונים וגורמים להם לשנות את מיקומם בתא. בהתאם למצב האורגניזם, תאים יכולים להגיב על ידי אחסון אנרגיה כגליקוגן או שומן, או הפיכתה לזמינה בצורה של גלוקוז. מסלול העברת אותות מאפשר לתאי שריר להגיב לדרישות מיידיות לאנרגיה בצורה של גלוקוז. צמיחת תאים מגורה כמעט תמיד על ידי אותות חיצוניים הנקראים גורמי גדילה. צמיחת תאים בלתי מבוקרת מובילה לסרטן, ומוטציות בגנים המקודדים לרכיבי חלבון של מסלולי איתות נמצאות לרוב בתאי הגידול. מוות תאים מתוכנת, או אפופטוזיס, חשוב להסרת תאים פגומים או מיותרים. השימוש באיתות סלולרי לארגון פירוק התא מבטיח שמולקולות מזיקות מהציטופלזמה לא ישוחררו לחללים שבין התאים, שכן הן נמצאות במוות בלתי מבוקר, נמק. אפופטוזיס מבטיח גם מיחזור יעיל של מרכיבי התא המת. סיום מפל האיתות הסלולרי חשוב מאוד כך שהתגובה לאות מתאימה הן בתזמון והן בעוצמה. פירוק מולקולות איתות ודה-פוספורילציה של תוצרי ביניים זרחניים של המסלול על ידי פוספטאזות הן שתי דרכים לסיים אותות בתוך התא.
רשימת מילים
- אפופטוזיס
- מוות תאים מתוכנת
- גורם גדילה
- ליגנד הנקשר לקולטנים משטח התא וממריץ את צמיחת התאים
- מעכב
- מולקולה הנקשרת לחלבון (בדרך כלל אנזים) ומונעת ממנו לתפקד
- פוספטאז
- אנזים המסיר את קבוצת הפוספטים ממולקולה שעברה זרחון בעבר
- פוספודיאסטרז
- אנזים המפרק cAMP, מייצר AMP, כדי להפסיק את האיתות


