2.3: كربون
- Page ID
- 195983
المهارات اللازمة للتطوير
- اشرح سبب أهمية الكربون للحياة
- وصف دور المجموعات الوظيفية في الجزيئات البيولوجية
تتكون الخلايا من العديد من الجزيئات المعقدة التي تسمى الجزيئات الكبيرة، مثل البروتينات والأحماض النووية (RNA و DNA) والكربوهيدرات والدهون. الجزيئات الكبيرة هي مجموعة فرعية من الجزيئات العضوية (أي سائل أو صلب أو غاز يحتوي على الكربون) والتي تعتبر مهمة بشكل خاص للحياة. المكون الأساسي لجميع هذه الجزيئات الكبيرة هو الكربون. تتميز ذرة الكربون بخصائص فريدة تسمح لها بتكوين روابط تساهمية لما يصل إلى أربع ذرات مختلفة، مما يجعل هذا العنصر متعدد الاستخدامات مثاليًا ليكون بمثابة المكون الهيكلي الأساسي، أو «العمود الفقري» للجزيئات الكبيرة.
تحتوي ذرات الكربون الفردية على غلاف إلكتروني خارجي غير مكتمل. بعدد ذري قدره 6 (ستة إلكترونات وستة بروتونات)، يملأ الإلكترونان الأولان الغلاف الداخلي، تاركًا أربعة في الغلاف الثاني. لذلك، يمكن أن تشكل ذرات الكربون ما يصل إلى أربع روابط تساهمية مع ذرات أخرى لتلبية قاعدة الثمانية. يقدم جزيء الميثان مثالاً: يحتوي على الصيغة الكيميائية CH 4. تشكل كل ذرة من ذرات الهيدروجين الأربعة رابطة تساهمية واحدة مع ذرة الكربون من خلال مشاركة زوج من الإلكترونات. ينتج عن هذا غلاف خارجي ممتلئ.
هيدروكربونات
الهيدروكربونات هي جزيئات عضوية تتكون بالكامل من الكربون والهيدروجين، مثل الميثان (CH 4) الموصوف أعلاه. غالبًا ما نستخدم الهيدروكربونات في حياتنا اليومية كوقود - مثل البروبان في موقد الغاز أو البيوتان في الولاعة. تخزن الروابط التساهمية العديدة بين الذرات في الهيدروكربونات كمية كبيرة من الطاقة، والتي يتم إطلاقها عند حرق هذه الجزيئات (الأكسدة). الميثان، وهو وقود ممتاز، هو أبسط جزيء هيدروكربوني، مع ذرة كربون مركزية مرتبطة بأربع ذرات هيدروجين مختلفة، كما هو موضح في الشكل\(\PageIndex{1}\). يتم تحديد هندسة جزيء الميثان، حيث توجد الذرات في ثلاثة أبعاد، من خلال شكل مدارات الإلكترون الخاصة به. تشكل الكربونات وذرات الهيدروجين الأربع شكلًا يُعرف باسم رباعي السطوح، بأربعة وجوه مثلثة؛ لهذا السبب، يوصف الميثان بأنه ذو هندسة رباعية السطوح.
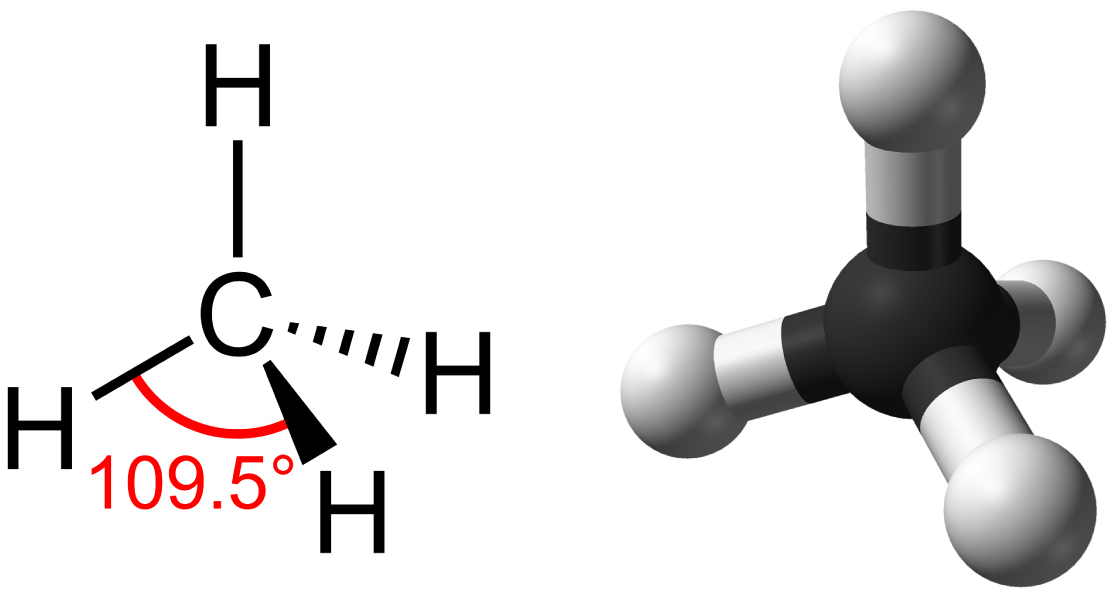
باعتبارها العمود الفقري للجزيئات الكبيرة للكائنات الحية، قد توجد الهيدروكربونات كسلاسل كربون خطية أو حلقات كربونية أو مجموعات من الاثنين. علاوة على ذلك، قد تكون الروابط الفردية من الكربون إلى الكربون روابط تساهمية مفردة أو مزدوجة أو ثلاثية، ويؤثر كل نوع من أنواع الروابط على هندسة الجزيء بطريقة معينة. يعد هذا الشكل ثلاثي الأبعاد أو التشكل لجزيئات الحياة الكبيرة (الجزيئات الكبيرة) أمرًا بالغ الأهمية لكيفية عملها.
سلاسل هيدروكربونية
تتكون سلاسل الهيدروكربون من روابط متتالية بين ذرات الكربون وقد تكون متفرعة أو غير متفرعة. علاوة على ذلك، يتم تغيير الهندسة الكلية للجزيء من خلال الأشكال الهندسية المختلفة للروابط التساهمية الفردية والمزدوجة والثلاثية، كما هو موضح في الشكل\(\PageIndex{2}\). تُستخدم الهيدروكربونات الإيثان والإيثين والإيثين والإيثين كأمثلة على كيفية تأثير الروابط المختلفة بين الكربون والكربون على هندسة الجزيء. تبدأ أسماء الجزيئات الثلاثة بالبادئة «eth-»، وهي بادئة اثنين من الهيدروكربونات الكربونية. تشير اللواحق «-ane» و «-ene» و «-yne» إلى وجود روابط كربون-كربون مفردة أو مزدوجة أو ثلاثية، على التوالي. وهكذا، يتبع البروبان والبروبين والبروبين نفس النمط مع ثلاثة جزيئات كربون، البيوتان، والبيوتان، والبيوتين لأربعة جزيئات كربون، وما إلى ذلك. تعمل الروابط المزدوجة والثلاثية على تغيير هندسة الجزيء: تسمح الروابط الفردية بالدوران على طول محور الرابطة، بينما تؤدي الروابط المزدوجة إلى تكوين مستوٍ والروابط الثلاثية إلى تكوين خطي. هذه الأشكال الهندسية لها تأثير كبير على الشكل الذي يمكن أن يتخذه جزيء معين.
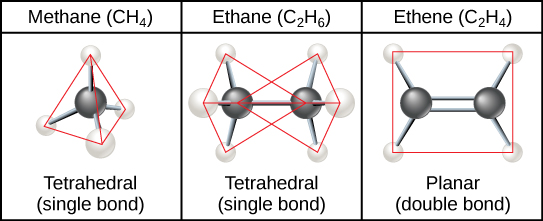
حلقات هيدروكربونية
حتى الآن، كانت الهيدروكربونات التي ناقشناها هي الهيدروكربونات الأليفاتية، والتي تتكون من سلاسل خطية من ذرات الكربون. نوع آخر من الهيدروكربون، الهيدروكربونات العطرية، يتكون من حلقات مغلقة من ذرات الكربون. توجد الهياكل الحلقية في الهيدروكربونات، وأحيانًا مع وجود روابط مزدوجة، والتي يمكن رؤيتها من خلال مقارنة بنية السيكلوهكسان بالبنزين في الشكل\(\PageIndex{3}\). تشمل أمثلة الجزيئات البيولوجية التي تدمج حلقة البنزين بعض الأحماض الأمينية والكوليسترول ومشتقاته، بما في ذلك هرموني الإستروجين والتستوستيرون. توجد حلقة البنزين أيضًا في مبيد الأعشاب 2,4-D. البنزين هو مكون طبيعي من النفط الخام وقد تم تصنيفه كمادة مسرطنة. تحتوي بعض الهيدروكربونات على أجزاء أليفاتية وعطرية؛ والبيتا كاروتين هو مثال على هذا الهيدروكربون.
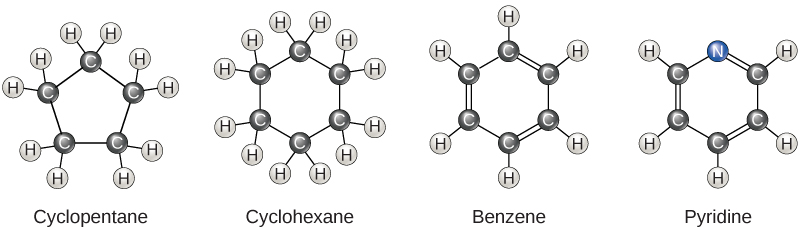
أيزومرات
يعد وضع الذرات والروابط الكيميائية ثلاثي الأبعاد داخل الجزيئات العضوية أمرًا أساسيًا لفهم كيمياءها. تُعرف الجزيئات التي تشترك في نفس الصيغة الكيميائية ولكنها تختلف في موضع (بنية) ذراتها و/أو روابطها الكيميائية باسم الأيزومرات. تختلف الأيزومرات الهيكلية (مثل البيوتان والأيزوبوتين الموضحة في الشكل\(\PageIndex{4}\) أ) في موضع روابطها التساهمية: يحتوي كلا الجزيئين على أربعة كربونات وعشرة هيدروجينات (C 4 H 10)، لكن الترتيب المختلف للذرات داخل الجزيئات يؤدي إلى اختلافات في خصائصها الكيميائية. على سبيل المثال، نظرًا لخصائصه الكيميائية المختلفة، فإن البيوتان مناسب للاستخدام كوقود لولاعات السجائر والمشاعل، في حين أن الأيزوبوتين مناسب للاستخدام كمبرد وداسر في علب الرش.
من ناحية أخرى، تحتوي الأيزومرات الهندسية على مواضع متشابهة لروابطها التساهمية ولكنها تختلف في كيفية تكوين هذه الروابط مع الذرات المحيطة، خاصة في الروابط المزدوجة من الكربون إلى الكربون. في جزيء البيوتين البسيط (C 4 H 8)، يمكن أن تكون مجموعتا الميثيل (CH 3) على جانبي الرابطة التساهمية المزدوجة المركزية للجزيء، كما هو موضح في الشكل\(\PageIndex{4}\) ب. عندما تكون الكربونات مرتبطة على نفس الجانب من الرابطة المزدوجة، فهذا هو رابطة الدول المستقلة التكوين؛ إذا كانت على طرفي نقيض من الرابطة المزدوجة، فهذا تكوين متحول. في التكوين العابر، تشكل الكربونات هيكلًا خطيًا إلى حد ما، في حين أن الكربونات في تكوين cis تقوم بانحناء (تغيير في الاتجاه) للعمود الفقري الكربوني.
آرت كونيكشن

أي من العبارات التالية خاطئة؟
- يمكن أن تكون الجزيئات ذات الصيغ CH 3 CH 2 COOH و C 3 H 6 O 2 أيزومرات هيكلية.
- يجب أن تحتوي الجزيئات على رابطة مزدوجة لتكون أيزومرات cis-trans.
- لكي يكون الجزيء متجانسًا، يجب أن يحتوي الجزيء على ثلاث ذرات أو مجموعات مختلفة على الأقل متصلة بكربون مركزي.
- لكي يكون الجزيء متجانسًا، يجب أن يحتوي الجزيء على أربع ذرات أو مجموعات مختلفة على الأقل متصلة بكربون مركزي.
في الدهون الثلاثية (الدهون والزيوت)، قد تحتوي سلاسل الكربون الطويلة المعروفة باسم الأحماض الدهنية على روابط مزدوجة، والتي يمكن أن تكون إما في تكوين رابطة الدول المستقلة أو المتحولة، كما هو موضح في الشكل\(\PageIndex{5}\). الدهون التي تحتوي على رابطة مزدوجة واحدة على الأقل بين ذرات الكربون هي دهون غير مشبعة. عندما تكون بعض هذه الروابط في تكوين رابطة الدول المستقلة، فإن الانحناء الناتج في العمود الفقري الكربوني للسلسلة يعني أن جزيئات الدهون الثلاثية لا يمكن أن تحزم بإحكام، لذلك تظل سائلة (زيتية) في درجة حرارة الغرفة. من ناحية أخرى، تحتوي الدهون الثلاثية ذات الروابط المزدوجة المتحولة (المعروفة باسم الدهون المتحولة) على أحماض دهنية خطية نسبيًا قادرة على التجميع بإحكام معًا في درجة حرارة الغرفة وتشكيل دهون صلبة. في النظام الغذائي البشري، ترتبط الدهون المتحولة بزيادة خطر الإصابة بأمراض القلب والأوعية الدموية، لذلك قامت العديد من الشركات المصنعة للأغذية بتقليل أو إلغاء استخدامها في السنوات الأخيرة. وعلى النقيض من الدهون غير المشبعة، فإن الدهون الثلاثية التي لا تحتوي على روابط مزدوجة بين ذرات الكربون تسمى الدهون المشبعة، مما يعني أنها تحتوي على جميع ذرات الهيدروجين المتاحة. الدهون المشبعة صلبة في درجة حرارة الغرفة وعادة ما تكون من أصل حيواني.
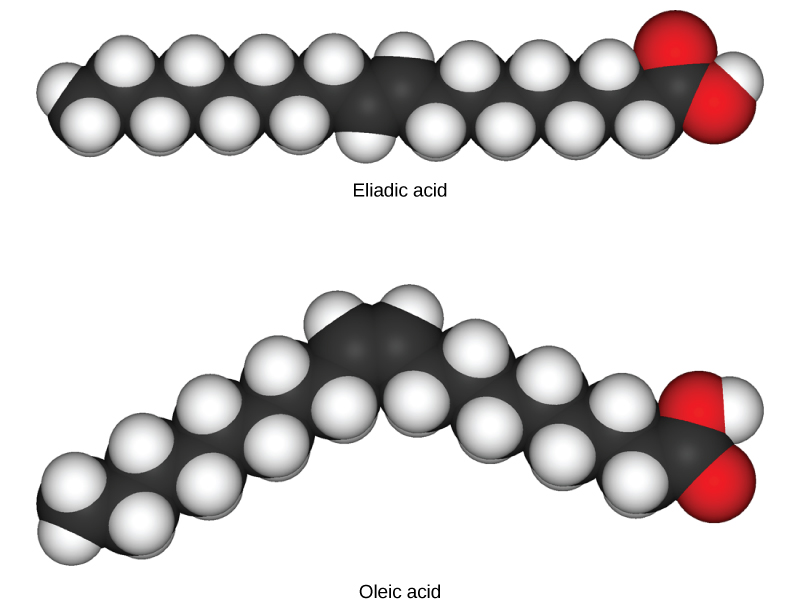
إنانتيومرات
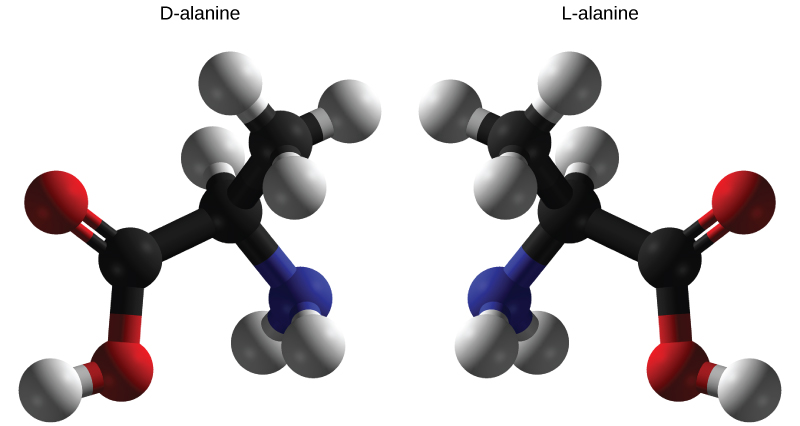
التماثلات هي جزيئات تشترك في نفس التركيب الكيميائي والروابط الكيميائية ولكنها تختلف في الموضع ثلاثي الأبعاد للذرات بحيث تكون صورًا معكوسة. كما هو موضح في الشكل\(\PageIndex{6}\)، وهو مثال لألانين الأحماض الأمينية، فإن الهيكلين غير قابلين للتراكب. في الطبيعة، يتم استخدام الأشكال L فقط من الأحماض الأمينية لصنع البروتينات. تظهر بعض أشكال D من الأحماض الأمينية في جدران خلايا البكتيريا، ولكن ليس في بروتيناتها أبدًا. وبالمثل، فإن الشكل D للجلوكوز هو المنتج الرئيسي لعملية التمثيل الضوئي ونادرًا ما يُرى الشكل L للجزيء في الطبيعة.
مجموعات وظيفية
المجموعات الوظيفية هي مجموعات من الذرات التي تحدث داخل الجزيئات وتمنح خصائص كيميائية محددة لتلك الجزيئات. توجد على طول «العمود الفقري الكربوني» للجزيئات الكبيرة. يتكون العمود الفقري الكربوني هذا من سلاسل و/أو حلقات من ذرات الكربون مع الاستبدال العرضي لعنصر مثل النيتروجين أو الأكسجين. يتم استبدال الجزيئات ذات العناصر الأخرى في العمود الفقري الكربوني بهيدروكربونات.
عادةً ما ترتبط المجموعات الوظيفية في الجزيء الكبير بالعمود الفقري الكربوني في مكان واحد أو عدة أماكن مختلفة على طول السلسلة و/أو هيكل الحلقة. لكل نوع من الأنواع الأربعة للجزيئات الكبيرة - البروتينات والدهون والكربوهيدرات والأحماض النووية - مجموعته المميزة من المجموعات الوظيفية التي تساهم بشكل كبير في خصائصها الكيميائية المختلفة ووظيفتها في الكائنات الحية.
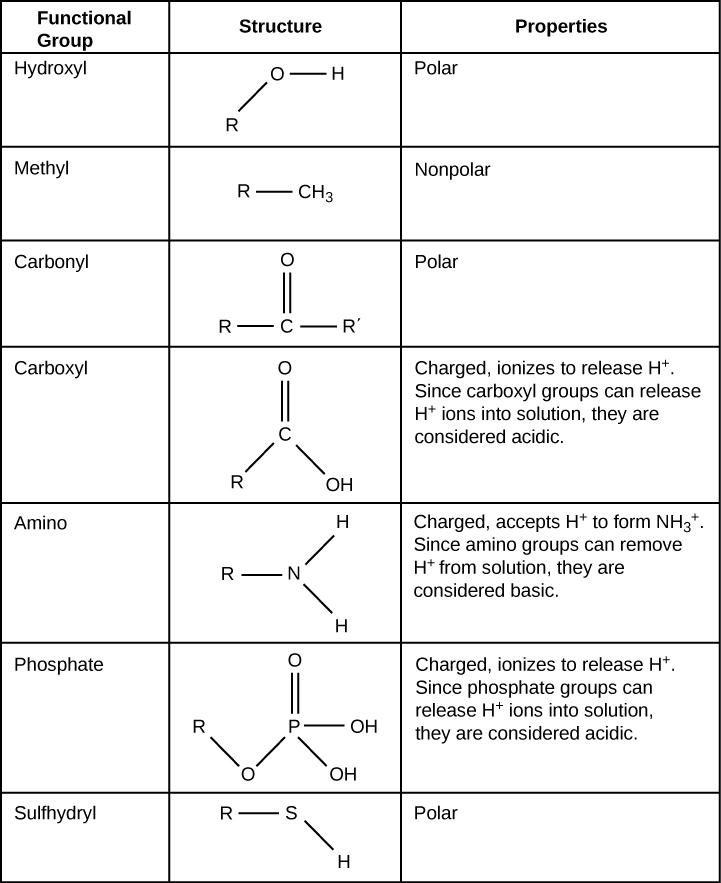
يمكن أن تشارك مجموعة وظيفية في تفاعلات كيميائية محددة. تظهر بعض المجموعات الوظيفية المهمة في الجزيئات البيولوجية في الشكل\(\PageIndex{7}\)؛ وهي تشمل: الهيدروكسيل والميل والكربونيل والكربوكسيل والأمينو والفوسفات والسلفهيدريل. تلعب هذه المجموعات دورًا مهمًا في تكوين جزيئات مثل الحمض النووي والبروتينات والكربوهيدرات والدهون. عادة ما يتم تصنيف المجموعات الوظيفية على أنها كارهة للماء أو محبة للماء اعتمادًا على خصائص الشحنة أو القطبية. مثال على المجموعة الكارهة للماء هو جزيء الميثان غير القطبي. من بين المجموعات الوظيفية المحبة للماء مجموعة الكربوكسيل الموجودة في الأحماض الأمينية وبعض السلاسل الجانبية للأحماض الأمينية والأحماض الدهنية التي تشكل الدهون الثلاثية والفوسفوليبيدات. تتأين مجموعة الكربوكسيل هذه لإطلاق أيونات الهيدروجين (H +) من مجموعة COOH مما يؤدي إلى مجموعة COO ذات الشحنة السالبة؛ هذا يساهم في الطبيعة المحبة للماء لأي جزيء توجد عليه. تحتوي المجموعات الوظيفية الأخرى، مثل مجموعة الكربونيل، على ذرة أكسجين سالبة الشحنة جزئيًا قد تشكل روابط هيدروجينية مع جزيئات الماء، مما يجعل الجزيء مرة أخرى أكثر محبة للماء.
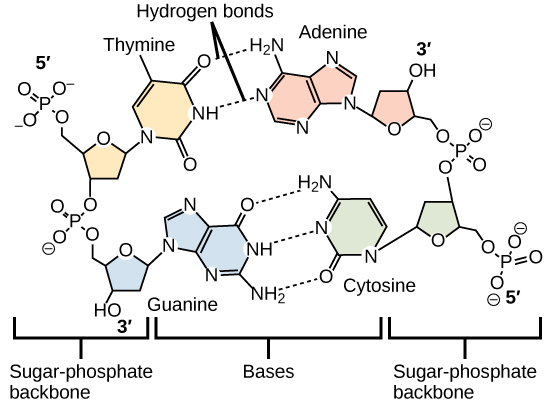
تعتبر الروابط الهيدروجينية بين المجموعات الوظيفية (داخل نفس الجزيء أو بين الجزيئات المختلفة) مهمة لوظيفة العديد من الجزيئات الكبيرة وتساعدها على الانحناء بشكل صحيح والحفاظ على الشكل المناسب للعمل. تشارك الروابط الهيدروجينية أيضًا في عمليات التعرف المختلفة، مثل الاقتران الأساسي التكميلي للحمض النووي وربط الإنزيم بالركيزة، كما هو موضح في الشكل\(\PageIndex{8}\).
ملخص
الخصائص الفريدة للكربون تجعله جزءًا أساسيًا من الجزيئات البيولوجية. يرتبط الكربون بالأكسجين والهيدروجين والنيتروجين تساهميًا لتشكيل العديد من الجزيئات المهمة للوظيفة الخلوية. يحتوي الكربون على أربعة إلكترونات في غلافه الخارجي ويمكن أن يشكل أربع روابط. يمكن أن يشكل الكربون والهيدروجين سلاسل أو حلقات هيدروكربونية. المجموعات الوظيفية هي مجموعات من الذرات التي تمنح خصائص محددة لسلاسل أو حلقات الهيدروكربون (أو الهيدروكربون البديل) التي تحدد خصائصها ووظائفها الكيميائية الشاملة.
اتصالات فنية
الشكل\(\PageIndex{4}\): أي العبارات التالية خاطئة؟
- يمكن أن تكون الجزيئات ذات الصيغ CH 3 CH 2 COOH و C 3 H 6 O 2 أيزومرات هيكلية.
- يجب أن تحتوي الجزيئات على رابطة مزدوجة لتكون أيزومرات متحولة.
- لكي يكون الجزيء متجانسًا، يجب أن يحتوي الجزيء على ثلاث ذرات أو مجموعات مختلفة على الأقل متصلة بكربون مركزي.
- لكي يكون الجزيء متجانسًا، يجب أن يحتوي الجزيء على أربع ذرات أو مجموعات مختلفة على الأقل متصلة بكربون مركزي.
- إجابة
-
ج
مسرد المصطلحات
- الهيدروكربون الأليفاتي
- هيدروكربون يتكون من سلسلة خطية من ذرات الكربون
- هيدروكربون عطري
- هيدروكربون يتكون من حلقات مغلقة من ذرات الكربون
- إنانتيومرات
- الجزيئات التي تشترك في البنية العامة وأنماط الترابط، ولكنها تختلف في كيفية وضع الذرات في ثلاثة أبعاد بحيث تكون صورًا معكوسة لبعضها البعض
- مجموعة وظيفية
- مجموعة من الذرات التي توفر أو تضفي وظيفة محددة على الهيكل الكربوني
- أيزومر هندسي
- أيزومر ذو أنماط ترابط متشابهة تختلف في وضع الذرات بجانب رابطة تساهمية مزدوجة
- الهيدروكربون
- جزيء يتكون فقط من الكربون والهيدروجين
- أيزومرات
- جزيئات تختلف عن بعضها البعض على الرغم من أنها تشترك في نفس الصيغة الكيميائية
- جزيء عضوي
- أي جزيء يحتوي على الكربون (باستثناء ثاني أكسيد الكربون)
- أيزومرات هيكلية
- الجزيئات التي تشترك في الصيغة الكيميائية ولكنها تختلف في وضع روابطها الكيميائية
- هيدروكربون مستبدل
- سلسلة أو حلقة هيدروكربونية تحتوي على ذرة عنصر آخر بدلاً من أحد الكربونات الأساسية


