4.1: Nishati na Kimetaboliki
- Page ID
- 174470
Wanasayansi hutumia bioenergetics neno kuelezea dhana ya mtiririko wa nishati (Kielelezo\(\PageIndex{1}\)) kupitia mifumo ya maisha, kama vile seli. Michakato ya seli kama vile kujenga na kuvunjika kwa molekuli tata hutokea kwa njia ya athari za kemikali za hatua kwa hatua. Baadhi ya athari hizi za kemikali ni za kutosha na kutolewa nishati, wakati wengine wanahitaji nishati kuendelea. Kama vile vitu vilivyo hai vinapaswa kuendelea kula chakula ili kujaza vifaa vyao vya nishati, seli lazima ziendelee kuzalisha nishati zaidi ili kujaza ile inayotumiwa na athari nyingi za kemikali zinazohitaji nishati ambazo zinaendelea kutokea. Kwa pamoja, athari zote za kemikali zinazotokea ndani ya seli, ikiwa ni pamoja na zile zinazotumia au kuzalisha nishati, hujulikana kama kimetaboliki ya seli.
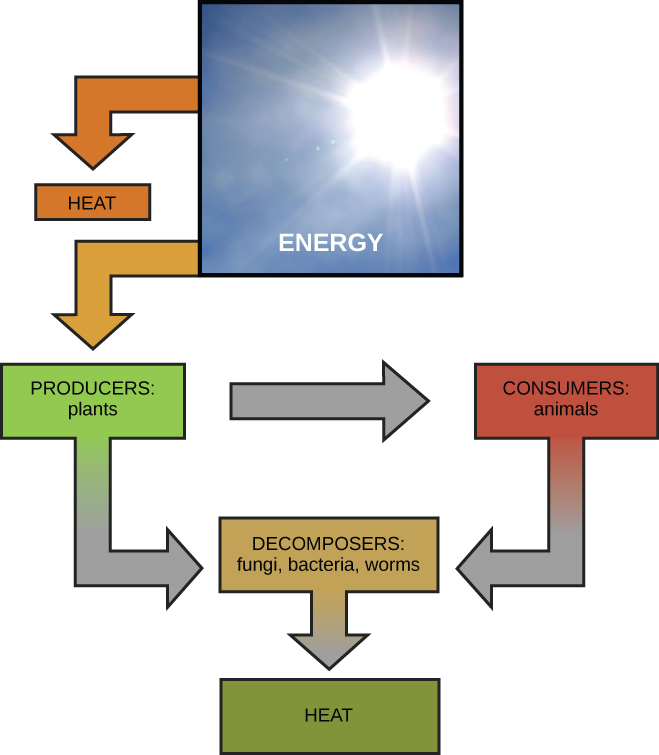
Metabolic pathways
Fikiria kimetaboliki ya sukari. Huu ni mfano wa classic wa moja ya michakato mingi ya seli ambayo hutumia na kuzalisha nishati. Mambo hai hutumia sukari kama chanzo kikubwa cha nishati, kwa sababu molekuli za sukari zina nishati kubwa iliyohifadhiwa ndani ya vifungo vyao. Kwa sehemu kubwa, viumbe vya photosynthesizing kama mimea huzalisha sukari hizi. Wakati wa usanisinuru, mimea hutumia nishati (awali kutoka jua) kubadilisha gesi ya dioksidi kaboni (CO 2) kuwa molekuli ya sukari (kama glucose: C 6 H 12 O 6). Wanatumia dioksidi kaboni na kuzalisha oksijeni kama bidhaa taka. Majibu haya yamefupishwa kama:
\[\ce{6CO2 + 6H2O -> C6H12O6 + 6O2}\nonumber\]
Kwa sababu mchakato huu unahusisha kuunganisha molekuli ya kuhifadhi nishati, inahitaji pembejeo ya nishati kuendelea. Wakati wa athari za mwanga za usanisinuru, nishati hutolewa na molekuli inayoitwa adenosine triphosphate (ATP), ambayo ni sarafu ya msingi ya nishati ya seli zote. Kama vile dola inatumiwa kama sarafu ya kununua bidhaa, seli hutumia molekuli za ATP kama sarafu ya nishati kufanya kazi ya haraka. Kwa upande mwingine, molekuli za kuhifadhi nishati kama vile glucose zinatumiwa tu kuvunjwa ili kutumia nishati zao. Mmenyuko unaovuna nishati ya molekuli ya sukari katika seli zinazohitaji oksijeni kuishi zinaweza kufupishwa kwa majibu ya reverse kwa usanisinuru. Katika mmenyuko huu, oksijeni hutumiwa na dioksidi kaboni hutolewa kama bidhaa taka. Majibu ni muhtasari kama:
\[\ce{C6H12O6 + 6O2 -> 6H2O + 6CO2}\nonumber\]
Athari hizi zote mbili zinahusisha hatua nyingi.
Michakato ya kufanya na kuvunja molekuli za sukari zinaonyesha mifano miwili ya njia za kimetaboliki. Njia ya metabolic ni mfululizo wa athari za kemikali ambazo huchukua molekuli ya kuanzia na huibadilisha, hatua kwa hatua, kupitia mfululizo wa intermediates ya kimetaboliki, hatimaye hutoa bidhaa ya mwisho. Katika mfano wa kimetaboliki sukari, kwanza metabolic njia synthesized sukari kutoka molekuli ndogo, na njia nyingine kuvunja sukari chini katika molekuli ndogo. Hizi mbili michakato kinyume - kwanza wanaohitaji nishati na pili kuzalisha nishati-ni inajulikana kama anabolic pathways (kujenga polima) na catabolic pathways (kuvunja polima katika monoma yao), kwa mtiririko huo. Kwa hiyo, kimetaboliki inajumuisha awali (anabolism) na uharibifu (catabolism) (Kielelezo\(\PageIndex{2}\)).
Ni muhimu kujua kwamba athari za kemikali za njia za kimetaboliki hazifanyiki peke yao. Kila hatua ya majibu huwezeshwa, au kuchochewa, na protini inayoitwa enzyme. Enzymes ni muhimu kwa kuchochea kila aina ya athari za kibiolojia-zile zinazohitaji nishati pamoja na zile zinazotoa nishati.
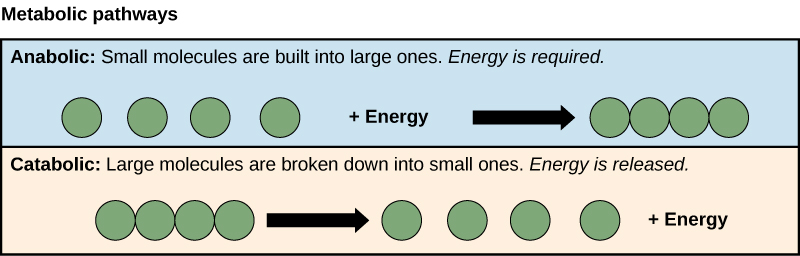
Nishati
Thermodynamics inahusu utafiti wa uhamisho wa nishati na nishati inayohusisha suala la kimwili. Suala linalofaa kwa kesi fulani ya uhamisho wa nishati inaitwa mfumo, na kila kitu nje ya jambo hilo kinaitwa mazingira. Kwa mfano, wakati inapokanzwa sufuria ya maji kwenye jiko, mfumo unajumuisha jiko, sufuria, na maji. Nishati huhamishwa ndani ya mfumo (kati ya jiko, sufuria, na maji). Kuna aina mbili za mifumo: kufunguliwa na kufungwa. Katika mfumo wa wazi, nishati inaweza kubadilishana na mazingira yake. Mfumo wa stovetop unafunguliwa kwa sababu joto linaweza kupotea hewa. Mfumo uliofungwa hauwezi kubadilishana nishati na mazingira yake.
Viumbe vya kibaiolojia ni mifumo ya wazi. Nishati hubadilishana kati yao na mazingira yao wanapotumia nishati kutoka jua kufanya usanisinuru au hutumia molekuli za kuhifadhi nishati na kutolewa nishati kwa mazingira kwa kufanya kazi na kutoa joto. Kama vitu vyote katika ulimwengu wa kimwili, nishati inakabiliwa na sheria za kimwili. Sheria za thermodynamics zinatawala uhamisho wa nishati ndani na kati ya mifumo yote ulimwenguni.
Kwa ujumla, nishati hufafanuliwa kama uwezo wa kufanya kazi, au kuunda aina fulani ya mabadiliko. Nishati ipo katika aina tofauti. Kwa mfano, nishati ya umeme, nishati ya mwanga, na nishati ya joto ni aina zote za nishati. Ili kufahamu jinsi nishati inapita ndani na nje ya mifumo ya kibiolojia, ni muhimu kuelewa sheria mbili za kimwili zinazoongoza nishati.
Thermodynamics
Sheria ya kwanza ya thermodynamics inasema kwamba jumla ya nishati katika ulimwengu ni mara kwa mara na kuhifadhiwa. Kwa maneno mengine, daima kumekuwa, na daima itakuwa, kiasi sawa cha nishati katika ulimwengu. Nishati ipo katika aina nyingi tofauti. Kwa mujibu wa sheria ya kwanza ya thermodynamics, nishati inaweza kuhamishwa kutoka sehemu kwa mahali au kubadilishwa kuwa aina tofauti, lakini haiwezi kuundwa au kuharibiwa. Uhamisho na mabadiliko ya nishati hufanyika karibu nasi wakati wote. Mababu ya mwanga hubadilisha nishati ya umeme kuwa nishati ya mwanga na joto. Miiko ya gesi hubadilisha nishati ya kemikali kutoka gesi asilia kuwa nishati ya joto. Mimea hufanya mojawapo ya mabadiliko ya nishati yenye manufaa zaidi duniani: ile ya kubadili nishati ya jua kwa nishati ya kemikali iliyohifadhiwa ndani ya molekuli za kikaboni (Kielelezo\(\PageIndex{1}\)). Baadhi ya mifano ya mabadiliko ya nishati ni inavyoonekana katika Kielelezo\(\PageIndex{3}\).
Changamoto kwa viumbe hai wote ni kupata nishati kutoka mazingira yao katika fomu ambazo zinaweza kuhamisha au kubadilisha kuwa nishati inayoweza kutumika kufanya kazi. Seli hai zimebadilika ili kukidhi changamoto hii. Nishati ya kemikali iliyohifadhiwa ndani ya molekuli za kikaboni kama vile sukari na mafuta huhamishwa na kubadilishwa kupitia mfululizo wa athari za kemikali za mkononi kuwa nishati ndani ya molekuli za ATP. Nishati katika molekuli za ATP zinapatikana kwa urahisi kufanya kazi. Mifano ya aina za kazi ambazo seli zinahitaji kufanya ni pamoja na kujenga molekuli tata, kusafirisha vifaa, kuimarisha mwendo wa cilia au flagella, na kuambukizwa nyuzi za misuli ili kuunda harakati.

Kazi ya msingi ya kiini hai ya kupata, kubadilisha, na kutumia nishati kufanya kazi inaweza kuonekana rahisi. Hata hivyo, sheria ya pili ya thermodynamics inaelezea kwa nini kazi hizi ni ngumu kuliko zinaonekana. Uhamisho wote wa nishati na mabadiliko haujawahi ufanisi kabisa. Katika kila uhamisho wa nishati, kiasi fulani cha nishati kinapotea kwa fomu ambayo haitumiki. Mara nyingi, fomu hii ni nishati ya joto. Thermodynamically, nishati ya joto hufafanuliwa kama nishati iliyohamishwa kutoka kwenye mfumo mmoja hadi mwingine ambayo haifanyi kazi. Kwa mfano, wakati bomba la taa limegeuka, baadhi ya nishati inayobadilishwa kutoka nishati ya umeme kwenye nishati ya mwanga inapotea kama nishati ya joto. Vivyo hivyo, nishati fulani hupotea kama nishati ya joto wakati wa athari za metabolic za mkononi.
Dhana muhimu katika mifumo ya kimwili ni ile ya utaratibu na ugonjwa. Nishati zaidi ambayo imepotea na mfumo kwa mazingira yake, chini ya kuamuru na zaidi random mfumo ni. Wanasayansi wanataja kipimo cha randomness au machafuko ndani ya mfumo kama entropy. Entropy ya juu ina maana ugonjwa wa juu na nishati ya chini. Molekuli na athari za kemikali zina entropy tofauti pia. Kwa mfano, entropy huongezeka kama molekuli kwenye mkusanyiko wa juu katika sehemu moja hueneza na kuenea nje. Sheria ya pili ya thermodynamics inasema kuwa nishati daima itapotea kama joto katika uhamisho wa nishati au mabadiliko.
Vitu vilivyo hai vinatakiwa sana, vinahitaji pembejeo ya nishati ya mara kwa mara kuhifadhiwa katika hali ya entropy ya chini.
Uwezo na Kinetic Nishati
Wakati kitu kinaendelea, kuna nishati inayohusishwa na kitu hicho. Fikiria mpira wa kuvunja. Hata mpira wa kuvunja polepole unaweza kufanya uharibifu mkubwa kwa vitu vingine. Nishati inayohusishwa na vitu katika mwendo inaitwa nishati ya kinetic (Kielelezo\(\PageIndex{4}\)). Risasi ya kasi, mtu anayetembea, na harakati ya haraka ya molekuli katika hewa (ambayo hutoa joto) wote wana nishati ya kinetic.
Sasa vipi ikiwa mpira huo usio na mwendo unaovunjika unainuliwa hadithi mbili juu ya ardhi na gane? Ikiwa mpira wa uharibifu uliosimamishwa hauwezi kusonga, kuna nishati inayohusishwa nayo? Jibu ni ndiyo. Nishati ambayo ilitakiwa kuinua mpira wa kuvunja haikutoweka, lakini sasa imehifadhiwa kwenye mpira wa kuvunja kwa sababu ya msimamo wake na nguvu ya mvuto inayofanya juu yake. Aina hii ya nishati inaitwa nishati ya uwezo (Kielelezo\(\PageIndex{4}\)). Ikiwa mpira ungeanguka, nishati inayoweza kubadilishwa kuwa nishati ya kinetic mpaka nishati yote ya uwezo ilikuwa imechoka wakati mpira ulipumzika chini. Kuvunja mipira pia swing kama pendulum; kwa njia ya swing, kuna mabadiliko ya mara kwa mara ya nishati ya uwezo (juu juu ya swing) kwa nishati ya kinetic (juu chini ya swing). Mifano mingine ya uwezo wa nishati ni pamoja na nishati ya maji iliyoshikiliwa nyuma ya bwawa au mtu anayekaribia kuruka nje ya ndege.

Nishati inayoweza sio tu inayohusishwa na eneo la suala, lakini pia na muundo wa suala. Hata chemchemi ardhini ina nishati ya uwezo ikiwa imesisitizwa; ndivyo ilivyo bendi ya mpira ambayo ni vunjwa taut. Kwenye kiwango cha Masi, vifungo vinavyoshikilia atomi za molekuli pamoja zipo katika muundo fulani ambao una nishati ya uwezo. Kumbuka kwamba anabolic njia za mkononi zinahitaji nishati ya kuunganisha molekuli tata kutoka kwa wale rahisi na pathways catabolic kutolewa nishati wakati molekuli tata ni kuvunjwa. Ukweli kwamba nishati inaweza kutolewa na kuvunjika kwa vifungo fulani vya kemikali inamaanisha kwamba vifungo hivyo vina nishati. Kwa kweli, kuna nishati inayoweza kuhifadhiwa ndani ya vifungo vya molekuli zote za chakula tunazokula, ambazo hatimaye zimeunganishwa kwa matumizi. Hii ni kwa sababu vifungo hivi vinaweza kutolewa nishati wakati umevunjika. Aina ya nishati inayoweza kuwepo ndani ya vifungo vya kemikali, na hutolewa wakati vifungo hivyo vimevunjika, huitwa nishati ya kemikali. Nishati ya kemikali ni wajibu wa kutoa seli hai na nishati kutoka kwa chakula. Kuondolewa kwa nishati hutokea wakati vifungo vya Masi ndani ya molekuli za chakula vimevunjika.
DHANA KATIKA HATUA
Tembelea tovuti na uchague “Pendulum” kutoka kwenye orodha ya “Kazi na Nishati” ili uone nishati ya kinetic na uwezo wa pendulum inayoendelea.
Free na Activation Nishati
Baada ya kujifunza kwamba athari za kemikali hutoa nishati wakati vifungo vya kuhifadhi nishati vimevunjika, swali muhimu linalofuata ni yafuatayo: Nishati inayohusishwa na athari hizi za kemikali zinahesabiwa na kuelezwa? Nishati iliyotolewa kutoka kwa mmenyuko mmoja inawezaje kulinganishwa na ile ya mmenyuko mwingine? Upimaji wa nishati ya bure hutumiwa kupima uhamisho huu wa nishati. Kumbuka kwamba kwa mujibu wa sheria ya pili ya thermodynamics, uhamisho wote wa nishati unahusisha kupoteza kiasi fulani cha nishati kwa fomu isiyoweza kutumika kama joto. Nishati ya bure hasa inahusu nishati inayohusishwa na mmenyuko wa kemikali ambayo inapatikana baada ya hasara kuhesabiwa. Kwa maneno mengine, nishati ya bure ni nishati inayoweza kutumika, au nishati ambayo inapatikana kufanya kazi.
Ikiwa nishati hutolewa wakati wa mmenyuko wa kemikali, basi mabadiliko katika nishati ya bure, yaliyotajwa kama G (delta G) itakuwa namba hasi. Mabadiliko mabaya katika nishati ya bure pia ina maana kwamba bidhaa za mmenyuko zina nishati ndogo zaidi kuliko majibu, kwa sababu hutoa nishati ya bure wakati wa majibu. Majibu ambayo yana mabadiliko mabaya katika nishati ya bure na hivyo kutolewa nishati ya bure huitwa athari za exergonic. Fikiria: ex ergonic maana nishati ni zamani iting mfumo. Athari hizi pia hujulikana kama athari za hiari, na bidhaa zao zina nishati ndogo iliyohifadhiwa kuliko majibu. Tofauti muhimu inapaswa kupatikana kati ya neno kwa hiari na wazo la mmenyuko wa kemikali hutokea mara moja. Kinyume na matumizi ya kila siku ya neno, mmenyuko wa hiari sio moja ambayo ghafla au haraka hutokea. Kutu kwa chuma ni mfano wa mmenyuko wa pekee ambao hutokea polepole, kidogo na kidogo, baada ya muda.
Ikiwa mmenyuko wa kemikali unachukua nishati badala ya kutoa nishati kwa usawa, basi G kwa mmenyuko huo itakuwa thamani nzuri. Katika kesi hiyo, bidhaa zina nishati zaidi ya bure kuliko majibu. Hivyo, bidhaa za athari hizi zinaweza kufikiriwa kama molekuli za kuhifadhi nishati. Athari hizi za kemikali huitwa athari za endergonic na hazipatikani. Mmenyuko wa endergonic hautafanyika peke yake bila kuongeza nishati ya bure.
UHUSIANO WA S

Angalia kila mchakato ulioonyeshwa na uamua ikiwa ni endergonic au exergonic.
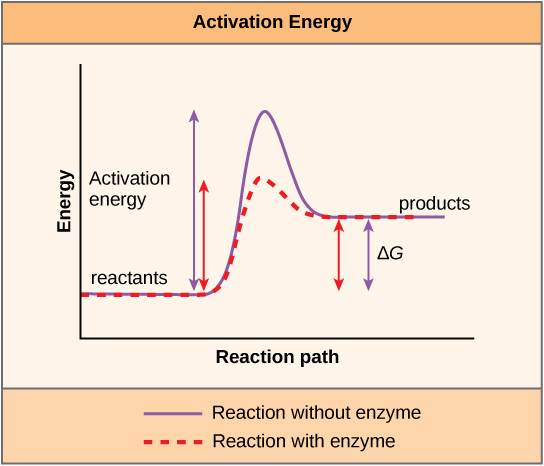
Kuna dhana nyingine muhimu ambayo inapaswa kuzingatiwa kuhusu athari za endergonic na exergonic. Athari za exergonic zinahitaji kiasi kidogo cha pembejeo ya nishati ili uende, kabla ya kuendelea na hatua zao za kutolewa kwa nishati. Athari hizi zina kutolewa kwa nishati, lakini bado zinahitaji pembejeo ya nishati mwanzoni. Kiasi hiki kidogo cha pembejeo ya nishati muhimu kwa athari zote za kemikali kutokea huitwa nishati ya uanzishaji.
DHANA KATIKA HATUA
Tazama uhuishaji wa hoja kutoka nishati ya bure hadi hali ya mpito ya majibu.
Enzyme
Dutu ambayo husaidia mmenyuko wa kemikali kutokea inaitwa kichocheo, na molekuli zinazochochea athari za biochemical huitwa enzymes. Enzymes nyingi ni protini na hufanya kazi muhimu ya kupunguza nguvu za uanzishaji wa athari za kemikali ndani ya seli. Zaidi ya athari muhimu kwa seli hai kutokea polepole mno katika joto ya kawaida kuwa ya matumizi yoyote kwa seli. Bila enzymes ili kuharakisha athari hizi, maisha hayakuweza kuendelea. Enzymes kufanya hivyo kwa kumfunga kwa molekuli reactant na kushikilia yao kwa njia ya kufanya kemikali kuvunja dhamana na -forming michakato kufanyika kwa urahisi zaidi. Ni muhimu kukumbuka kwamba enzymes hazibadilika ikiwa mmenyuko ni exergonic (hiari) au endergonic. Hii ni kwa sababu hawana mabadiliko ya nishati ya bure ya reactants au bidhaa. Wao hupunguza tu nishati ya uanzishaji inahitajika kwa majibu ya kuendelea (Kielelezo\(\PageIndex{6}\)). Kwa kuongeza, enzyme yenyewe haibadilishwa na majibu ambayo huchochea. Mara baada ya mmenyuko mmoja umechochewa, enzyme inaweza kushiriki katika athari nyingine.
Vipengele vya kemikali ambavyo enzyme hufunga huitwa substrates ya enzyme. Kunaweza kuwa na substrates moja au zaidi, kulingana na mmenyuko fulani wa kemikali. Katika baadhi ya athari, substrate moja ya reactant imevunjika katika bidhaa nyingi. Kwa wengine, substrates mbili zinaweza kuja pamoja ili kuunda molekuli moja kubwa. reactants mbili pia kuingia majibu na wote kuwa iliyopita, lakini wao kuondoka majibu kama bidhaa mbili. Eneo ndani ya enzyme ambapo substrate hufunga inaitwa tovuti ya kazi ya enzyme. Tovuti ya kazi ni ambapo “hatua” hutokea. Kwa kuwa enzymes ni protini, kuna mchanganyiko wa kipekee wa minyororo ya upande wa amino asidi ndani ya tovuti ya kazi. Kila mlolongo wa upande una sifa ya mali tofauti. Wanaweza kuwa kubwa au ndogo, dhaifu tindikali au msingi, hydrophilic au hydrophobic, vyema au vibaya kushtakiwa, au neutral. Mchanganyiko wa kipekee wa minyororo ya upande hujenga mazingira maalum ya kemikali ndani ya tovuti ya kazi. Mazingira haya maalum yanafaa kumfunga kwenye substrate moja maalum ya kemikali (au substrates).
Maeneo ya kazi yanakabiliwa na mvuto wa mazingira ya ndani. Kuongezeka kwa joto la mazingira kwa ujumla huongeza viwango vya mmenyuko, enzyme-kichocheo au vinginevyo. Hata hivyo, joto nje ya aina mojawapo hupunguza kiwango ambacho enzyme huchochea mmenyuko. Joto la joto hatimaye husababisha enzymes kwa denature, mabadiliko yasiyotumiwa katika sura tatu-dimensional na hivyo kazi ya enzyme. Enzymes pia inafaa kufanya kazi bora ndani ya aina fulani ya pH na chumvi, na, kama ilivyo kwa joto, pH kali, na viwango vya chumvi vinaweza kusababisha enzymes kwa denature.
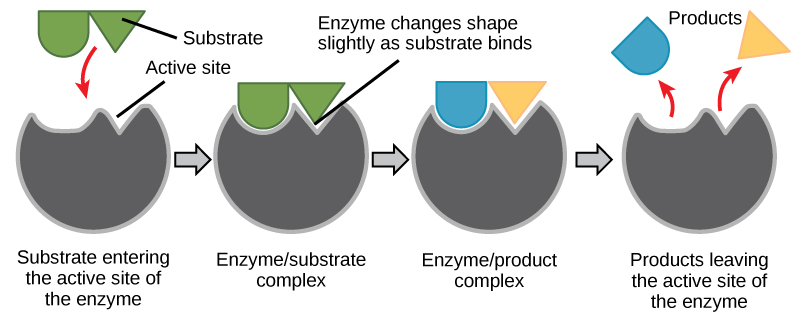
Kwa miaka mingi, wanasayansi walidhani kuwa kisheria ya enzyme-substrate ilifanyika kwa mtindo rahisi wa “lock na ufunguo”. Mfano huu ulisema kuwa enzyme na substrate vinafaa pamoja kikamilifu katika hatua moja ya papo hapo. Hata hivyo, utafiti wa sasa unasaidia mfano unaoitwa ikiwa fit (Kielelezo\(\PageIndex{7}\)). Mfano wa induced-fit unazidi juu ya mfano wa lock-na-muhimu kwa kuelezea kisheria zaidi nguvu kati ya enzyme na substrate. Kama enzyme na substrate kuja pamoja, mwingiliano wao husababisha mabadiliko kali katika muundo wa enzyme ambayo hufanya mpangilio bora wa kisheria kati ya enzyme na substrate.
DHANA KATIKA HATUA
View uhuishaji wa ikiwa fit.
Wakati enzyme inafunga substrate yake, tata ya enzyme-substrate inaundwa. Ugumu huu hupunguza nishati ya uanzishaji wa mmenyuko na inakuza maendeleo yake ya haraka katika mojawapo ya njia nyingi zinazowezekana. Katika ngazi ya msingi, enzymes huendeleza athari za kemikali zinazohusisha substrate zaidi ya moja kwa kuleta substrates pamoja katika mwelekeo bora wa majibu. Njia nyingine ambayo enzymes huendeleza mmenyuko wa substrates zao ni kwa kujenga mazingira bora ndani ya tovuti ya kazi kwa majibu ya kutokea. Mali za kemikali zinazojitokeza kutoka kwa utaratibu fulani wa vikundi vya amino asidi R ndani ya tovuti ya kazi huunda mazingira kamili kwa substrates maalum ya enzyme ili kuitikia.
Tata ya substrate ya enzyme pia inaweza kupunguza nishati ya uanzishaji kwa kuacha muundo wa dhamana ili iwe rahisi kuvunja. Hatimaye, enzymes pia zinaweza kupunguza nguvu za uanzishaji kwa kushiriki katika mmenyuko wa kemikali yenyewe. Katika kesi hizi, ni muhimu kukumbuka kuwa enzyme itarudi hali yake ya awali kwa kukamilika kwa majibu. Moja ya mali ya mahususi ya enzymes ni kwamba hubakia hatimaye bila kubadilika na athari ambazo huchochea. Baada ya enzyme imechochea mmenyuko, hutoa bidhaa (s) zake na inaweza kuchochea mmenyuko mpya.
Inaonekana kuwa bora kuwa na hali ambayo enzymes zote za viumbe zilikuwepo katika ugavi mwingi na zimefanya kazi vizuri chini ya hali zote za mkononi, katika seli zote, wakati wote. Hata hivyo, njia mbalimbali zinahakikisha kwamba hii haitoke. Mahitaji ya seli na hali hutofautiana mara kwa mara kutoka kiini hadi kiini, na mabadiliko ndani ya seli za mtu binafsi kwa muda. Enzymes zinazohitajika za seli za tumbo hutofautiana na zile za seli za kuhifadhi mafuta, seli za ngozi, seli za damu, na seli za ujasiri. Aidha, utumbo chombo kiini kazi ngumu sana kwa mchakato na kuvunja virutubisho wakati huo karibu ifuatavyo chakula ikilinganishwa na masaa mengi baada ya mlo. Kama mahitaji haya ya mkononi na hali kutofautiana, hivyo lazima kiasi na utendaji wa enzymes mbalimbali.
Kwa kuwa viwango vya athari biochemical ni kudhibitiwa na nishati uanzishaji, na Enzymes chini na kuamua nguvu uanzishaji kwa athari za kemikali, kiasi jamaa na utendaji wa aina ya Enzymes ndani ya seli hatimaye kuamua ambayo athari itaendelea na kwa viwango gani. Uamuzi huu ni tightly kudhibitiwa katika seli. Katika mazingira fulani ya seli, shughuli za enzyme hudhibitiwa kwa sehemu na mambo ya mazingira kama pH, joto, mkusanyiko wa chumvi, na, wakati mwingine, cofactors au coenzymes.
Enzymes pia inaweza kudhibitiwa kwa njia ambazo zinaweza kukuza au kupunguza shughuli za enzyme. Kuna aina nyingi za molekuli zinazozuia au kukuza kazi ya enzyme, na taratibu mbalimbali ambazo zinafanya hivyo. Katika baadhi ya matukio ya kuzuia enzyme, molekuli ya kizuizi ni sawa na substrate ambayo inaweza kumfunga kwenye tovuti ya kazi na kuzuia tu substrate kutoka kumfunga. Wakati hii itatokea, enzyme imezuiliwa kwa njia ya kuzuia ushindani, kwa sababu molekuli ya kizuizi inashindana na substrate ya kumfunga kwenye tovuti ya kazi.
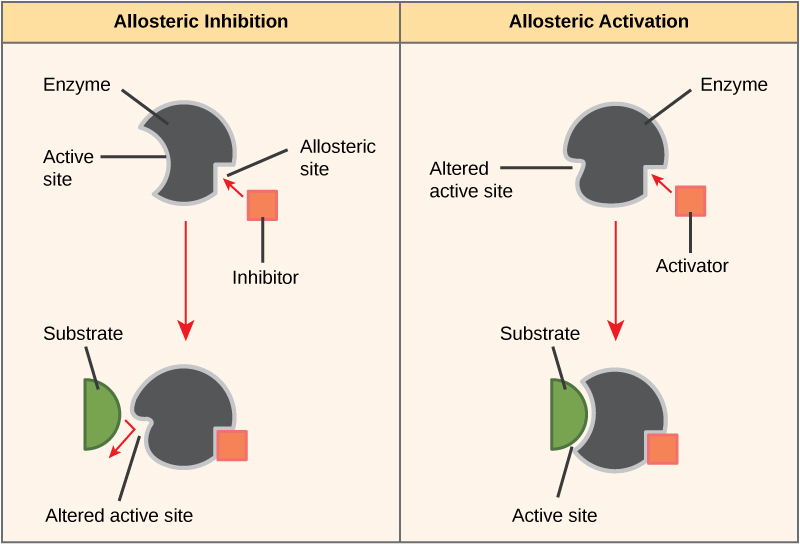
Kwa upande mwingine, katika kukandamiza yasiyo ya ushindani, molekuli ya kiviza hufunga kwa enzyme katika eneo lisilo na tovuti ya kazi, inayoitwa tovuti ya allosteric, lakini bado itaweza kuzuia kisheria cha substrate kwenye tovuti ya kazi. Baadhi ya molekuli za kizuizi hufunga kwa enzymes mahali ambapo kumfunga kwao husababisha mabadiliko ya kufanana ambayo hupunguza mshikamano wa enzyme kwa substrate yake. Aina hii ya kuzuia inaitwa kuzuia allosteric (Kielelezo\(\PageIndex{8}\)). Wengi allosterically umewekwa Enzymes ni linajumuisha zaidi ya moja polipeptidi, maana kwamba wana zaidi ya moja protini subunit. Wakati kizuizi cha allosteric kinafunga kwa kanda kwenye enzyme, maeneo yote ya kazi kwenye subunits ya protini yanabadilishwa kidogo kama vile hufunga substrates zao kwa ufanisi mdogo. Kuna watendaji wa allosteric pamoja na inhibitors. Allosteric activators kumfunga kwa maeneo ya enzyme mbali na tovuti ya kazi, na kusababisha mabadiliko conformational ambayo huongeza mshikamano wa enzyme kazi tovuti (s) kwa substrate yake (s) (Mtini.\(\PageIndex{8}\)).
KAZI KATIKA ACTION: Dawa Developer Madawa

Enzymes ni sehemu muhimu za njia za kimetaboliki. Kuelewa jinsi enzymes zinavyofanya kazi na jinsi gani zinaweza kudhibitiwa ni kanuni muhimu nyuma ya maendeleo ya madawa mengi ya dawa kwenye soko la leo. Wanabiolojia wanaofanya kazi katika uwanja huu kushirikiana na wanasayansi wengine kubuni madawa ya kulevya (Kielelezo\(\PageIndex{9}\)).
Fikiria statins kwa mfano-statins ni jina lililopewa darasa moja la madawa ya kulevya ambayo yanaweza kupunguza viwango vya cholesterol. Misombo hii ni inhibitors ya enzyme HMG-COA reductase, ambayo ni enzyme ambayo synthesizes cholesterol kutoka lipids katika mwili. Kwa kuzuia enzyme hii, kiwango cha cholesterol synthesized katika mwili kinaweza kupunguzwa. Vile vile, acetaminophen, maarufu kuuzwa chini ya jina la brand Tylenol, ni kizuizi cha cyclooxygenase ya enzyme. Wakati hutumiwa kutoa misaada kutokana na homa na kuvimba (maumivu), utaratibu wake wa utekelezaji bado haueleweki kabisa.
Je! Madawa ya kulevya yanagunduliwaj Moja ya changamoto kubwa katika ugunduzi wa madawa ya kulevya ni kutambua lengo la madawa ya kulevya. Lengo la madawa ya kulevya ni molekuli ambayo ni halisi lengo la dawa. Katika kesi ya statins, HMG-coa reductase ni lengo la madawa ya kulevya. Malengo ya madawa ya kulevya yanatambuliwa kupitia utafiti wa maumivu katika maabara. Kutambua lengo peke yake haitoshi; wanasayansi pia wanahitaji kujua jinsi shabaha inavyofanya ndani ya seli na ni athari gani zinazotoka katika kesi ya ugonjwa. Mara baada ya lengo na njia ni kutambuliwa, basi mchakato halisi wa kubuni madawa ya kulevya huanza. Katika hatua hii, wanakemia na wanabiolojia hufanya kazi pamoja ili kubuni na kuunganisha molekuli zinazoweza kuzuia au kuamsha mmenyuko fulani. Hata hivyo, hii ni mwanzo tu: Ikiwa na wakati mfano wa madawa ya kulevya unafanikiwa katika kutekeleza kazi yake, basi inakabiliwa na vipimo vingi kutoka majaribio ya vitro hadi majaribio ya kliniki kabla ya kupata idhini kutoka kwa Utawala wa Chakula na Dawa ya Marekani kuwa kwenye soko.
Enzymes nyingi hazifanyi kazi optimalt, au hata wakati wote, isipokuwa amefungwa kwa molekuli nyingine maalum zisizo protini msaidizi. Wanaweza kushikamana ama kwa muda kwa njia ya vifungo ionic au hidrojeni, au kudumu kwa njia ya vifungo vikali vya nguvu. Kufungia kwa molekuli hizi kukuza sura bora na kazi ya enzymes zao. Mifano miwili ya aina hizi za molekuli za msaidizi ni cofactors na coenzymes. Cofactors ni ions isokaboni kama vile ions ya chuma na magnesiamu. Coenzymes ni molekuli za msaidizi wa kikaboni, zile zilizo na muundo wa atomiki wa msingi unaoundwa na kaboni Kama enzymes, molekuli hizi hushiriki katika athari bila kubadilishwa wenyewe na hatimaye zinatengenezwa tena na kutumika tena. Vitamini ni chanzo cha coenzymes. Vitamini vingine ni watangulizi wa coenzymes na wengine hufanya moja kwa moja kama coenzymes. Vitamini C ni coenzyme moja kwa moja kwa enzymes nyingi zinazohusika katika kujenga tishu muhimu zinazojumuisha, collagen. Kwa hiyo, kazi ya enzyme ni, kwa sehemu, inasimamiwa na wingi wa cofactors mbalimbali na coenzymes, ambayo inaweza kutolewa na chakula cha viumbe au, wakati mwingine, zinazozalishwa na viumbe.
Uzuiaji wa maoni katika Njia za Metabolic
Molekuli zinaweza kudhibiti kazi ya enzyme kwa njia nyingi. Swali kuu linabakia, hata hivyo: Molekuli hizi ni nini na zinatoka wapi? Baadhi ni cofactors na coenzymes, kama umejifunza. Nini molekuli nyingine katika seli kutoa kanuni enzymatic kama vile ubadilikaji allosteric, na ushindani na yasiyo ya ushindani kukandamiza? Labda vyanzo muhimu zaidi vya molekuli za udhibiti, kuhusiana na kimetaboliki ya seli za enzymatic, ni bidhaa za athari za metabolic za mkononi wenyewe. Kwa njia ya ufanisi zaidi na ya kifahari, seli zimebadilika kutumia bidhaa za athari zao wenyewe kwa kuzuia maoni ya shughuli za enzyme. Uzuiaji wa maoni unahusisha matumizi ya bidhaa ya mmenyuko ili kudhibiti uzalishaji wake zaidi (Kielelezo\(\PageIndex{10}\)). Kiini hujibu kwa wingi wa bidhaa kwa kupunguza kasi ya uzalishaji wakati wa athari za anabolic au catabolic. Bidhaa hizo za majibu zinaweza kuzuia enzymes ambazo zilichochea uzalishaji wao kupitia taratibu zilizoelezwa hapo juu.
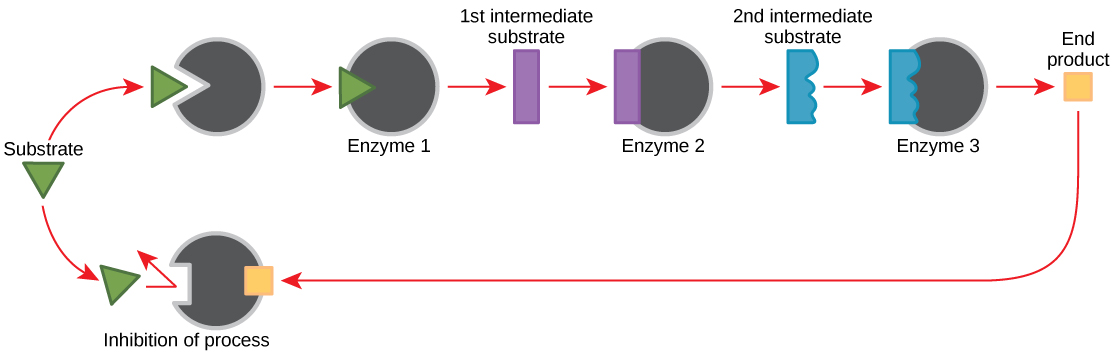
Uzalishaji wa amino asidi na nucleotides hudhibitiwa kwa njia ya kuzuia maoni. Zaidi ya hayo, ATP ni mdhibiti wa allosteric wa baadhi ya enzymes zinazohusika katika kuvunjika kwa catabolic ya sukari, mchakato unaojenga ATP. Kwa njia hii, wakati ATP iko katika ugavi mwingi, kiini kinaweza kuzuia uzalishaji wa ATP. Kwa upande mwingine, ADP hutumika kama mdhibiti mzuri wa allosteric (activator ya allosteric) kwa baadhi ya enzymes sawa ambazo zinazuia na ATP. Hivyo, wakati viwango vya jamaa vya ADP ni vya juu ikilinganishwa na ATP, kiini husababishwa kuzalisha ATP zaidi kupitia catabolism ya sukari.
Muhtasari wa sehemu
Viini hufanya kazi za maisha kupitia athari mbalimbali za kemikali. Kimetaboliki ya kiini inahusu mchanganyiko wa athari za kemikali zinazofanyika ndani yake. Athari za kikataboli huvunja kemikali tata ndani ya rahisi na huhusishwa na kutolewa kwa nishati. Michakato ya anabolic hujenga molekuli tata nje ya rahisi na inahitaji nishati.
Katika kusoma nishati, mfumo wa neno unahusu suala na mazingira yanayohusika katika uhamisho wa nishati. Entropy ni kipimo cha ugonjwa wa mfumo. Sheria za kimwili zinazoelezea uhamisho wa nishati ni sheria za thermodynamics. Sheria ya kwanza inasema kwamba jumla ya nishati katika ulimwengu ni mara kwa mara. Sheria ya pili ya thermodynamics inasema kwamba kila uhamisho wa nishati unahusisha kupoteza kwa nishati kwa fomu isiyoweza kutumika, kama vile nishati ya joto. Nishati huja kwa aina tofauti: kinetic, uwezo, na bure. Mabadiliko katika nishati ya bure ya mmenyuko inaweza kuwa hasi (hutoa nishati, exergonic) au chanya (hutumia nishati, endergonic). Athari zote zinahitaji pembejeo ya awali ya nishati kuendelea, inayoitwa nishati ya uanzishaji.
Enzymes ni vichocheo vya kemikali vinavyoharakisha athari za kemikali kwa kupunguza nishati zao za uanzishaji. Enzymes zina tovuti yenye kazi na mazingira ya kipekee ya kemikali ambayo yanafaa kemikali maalum za kemikali kwa enzyme hiyo, inayoitwa substrates. Enzymes na substrates hufikiriwa kumfunga kulingana na mfano unaofaa. Hatua ya enzyme imewekwa ili kuhifadhi rasilimali na kujibu optimalt kwa mazingira.
Sanaa Connections
Kielelezo\(\PageIndex{5}\): Angalia kila mchakato ulioonyeshwa na uamua ikiwa ni endergonic au exergonic.
- Jibu
-
Rundo la mbolea linaloharibika ni mchakato wa exergonic. Mtoto anayeendelea kutoka yai ya mbolea ni mchakato wa endergonic. Chai ya kufuta ndani ya maji ni mchakato wa exergonic. Mpira unaoteremka ni mchakato wa exergonic.
faharasa
- uanzishaji nishati
- kiasi cha nishati ya awali muhimu kwa athari kutokea
- tovuti ya kazi
- kanda maalum juu ya enzyme ambapo substrate hufunga
- kizuizi cha allosteric
- utaratibu wa kuzuia hatua ya enzyme ambayo molekuli ya udhibiti hufunga kwenye tovuti ya pili (sio tovuti ya kazi) na huanzisha mabadiliko ya conformation kwenye tovuti ya kazi, kuzuia kumfunga na substrate
- anaboli
- inaelezea njia ambayo inahitaji pembejeo ya nishati ya wavu ili kuunganisha molekuli tata kutoka kwa rahisi
- bioenergetics
- dhana ya mtiririko wa nishati kupitia mifumo ya maisha
- ya ukataboli
- inaelezea njia ambayo molekuli tata huvunjika kuwa rahisi, kutoa nishati kama bidhaa ya ziada ya mmenyuko
- kuzuia ushindani
- utaratibu wa jumla wa kanuni za shughuli za enzyme ambapo molekuli isipokuwa substrate ya enzyme inaweza kumfunga tovuti ya kazi na kuzuia substrate yenyewe kutoka kumfunga, hivyo kuzuia kiwango cha jumla cha mmenyuko kwa enzyme
- endergonic
- inaelezea mmenyuko wa kemikali ambayo husababisha bidhaa zinazohifadhi nishati zaidi ya uwezo wa kemikali kuliko majibu
- kimeng'enya
- molekuli ambayo huchochea mmenyuko wa biochemical
- exergonic
- inaelezea mmenyuko wa kemikali ambayo husababisha bidhaa zilizo na nishati ndogo ya kemikali kuliko majibu, pamoja na kutolewa kwa nishati ya bure
- kizuizi cha maoni
- utaratibu wa kanuni za shughuli za enzyme, ambapo bidhaa ya mmenyuko au bidhaa ya mwisho ya mfululizo wa athari za mtiririko huzuia enzyme kwa hatua ya awali katika mfululizo wa majibu.
- nishati ya joto
- nishati kuhamishwa kutoka mfumo mmoja hadi mwingine ambayo si kazi
- nishati kinetic
- aina ya nishati inayohusishwa na vitu vilivyo katika mwendo
- kimetaboliki
- athari zote za kemikali zinazofanyika ndani ya seli, ikiwa ni pamoja na wale wanaotumia nishati na wale ambao hutoa nishati
- kukandamiza yasiyo ya ushind
- utaratibu wa jumla wa kanuni za shughuli za enzyme ambapo molekuli ya udhibiti hufunga kwenye tovuti isipokuwa tovuti ya kazi na kuzuia tovuti ya kazi kutoka kumfunga substrate; hivyo, molekuli ya kizuizi haina kushindana na substrate kwa tovuti ya kazi; kuzuia allosteric ni aina ya kukandamiza yasiyo ya ushind
- uwezo wa nishati
- aina ya nishati ambayo inahusu uwezo wa kufanya kazi
- sabstreti
- molekuli ambayo enzyme hufanya
- thermodynamics
- sayansi ya uhusiano kati ya joto, nishati, na kazi


