10.3: Mabadiliko ya Awamu
- Page ID
- 182408
- Eleza mabadiliko ya awamu na joto la awamu ya mpito
- Eleza uhusiano kati ya joto la mpito wa awamu na vikosi vya kuvutia vya intermolecular
- Eleza taratibu zinazowakilishwa na joto la kawaida na baridi, na kukokotoa mtiririko wa joto na mabadiliko ya enthalpy yanayoambatana na taratibu hizi
Tunashuhudia na kutumia mabadiliko ya hali ya kimwili, au mabadiliko ya awamu, kwa njia nyingi. Kama mfano mmoja wa umuhimu wa kimataifa, fikiria uvukizi, condensation, kufungia, na kiwango cha maji. Mabadiliko haya ya hali ni mambo muhimu ya mzunguko wa maji ya dunia yetu pamoja na matukio mengine mengi ya asili na michakato ya kiteknolojia ya umuhimu wa kati kwa maisha yetu. Katika moduli hii, mambo muhimu ya mabadiliko ya awamu yanachunguzwa.
Uvukizi na Condensation
Kiowevu kinapovukiza katika chombo kilichofungwa, molekuli za gesi haziwezi kutoroka. Kama molekuli hizi za awamu ya gesi hoja nasibu juu, wao mara kwa mara kugongana na uso wa awamu kufupishwa, na wakati mwingine, migongano haya itasababisha molekuli tena kuingia awamu kufupishwa. Mabadiliko kutoka awamu ya gesi hadi kioevu huitwa condensation. Wakati kiwango cha condensation kinakuwa sawa na kiwango cha mvuke, wala kiasi cha kioevu wala kiasi cha mvuke katika chombo kinabadilika. Mvuke ndani ya chombo husemekana kuwa katika usawa na kioevu. Kumbuka kwamba hii sio hali ya tuli, kama molekuli zinaendelea kubadilishana kati ya awamu zilizopunguzwa na za gesi. Hiyo ni mfano wa usawa wa nguvu, hali ya mfumo ambao michakato ya usawa (kwa mfano, mvuke na condensation) hutokea kwa viwango sawa. Shinikizo linalofanywa na mvuke katika usawa na kioevu kwenye chombo kilichofungwa kwenye joto lililopewa linaitwa shinikizo la mvuke la kioevu (au shinikizo la mvuke la usawa). Eneo la uso wa kioevu katika kuwasiliana na mvuke na ukubwa wa chombo hauna athari juu ya shinikizo la mvuke, ingawa huathiri muda unaohitajika kwa usawa kufikiwa. Tunaweza kupima shinikizo la mvuke la kioevu kwa kuweka sampuli kwenye chombo kilichofungwa, kama kilichoonyeshwa kwenye Kielelezo\(\PageIndex{1}\), na kutumia manometer kupima ongezeko la shinikizo ambalo linatokana na mvuke katika usawa na awamu iliyosafishwa.
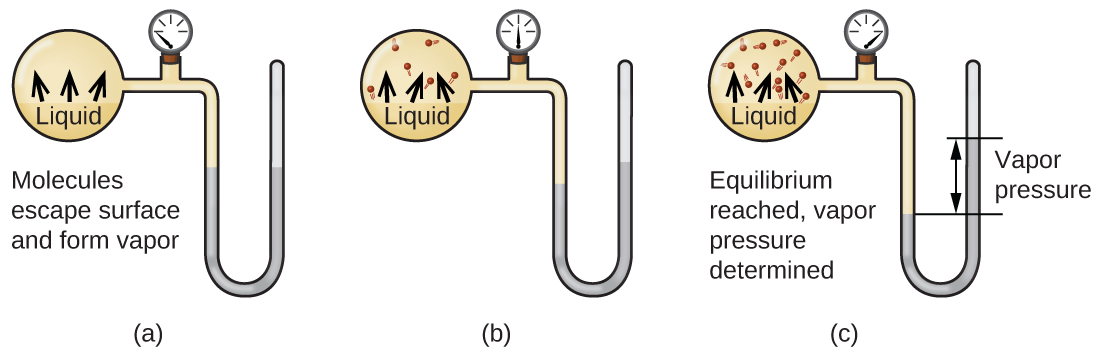
Utambulisho wa kemikali wa molekuli katika kioevu huamua aina (na nguvu) za vivutio vya intermolecular iwezekanavyo; kwa hiyo, vitu tofauti vitaonyesha shinikizo tofauti za mvuke za usawa. Vikosi vyenye nguvu vya kuvutia vya intermolecular vitatumika kuzuia uvukizi pamoja na kupendelea “recapture” ya molekuli ya awamu ya gesi wakati wanapogongana na uso wa kioevu, na kusababisha shinikizo la chini la mvuke. Vivutio dhaifu vya intermolecular sasa chini ya kizuizi kwa uvukizi, na uwezekano mdogo wa kupunguzwa kwa gesi, kutoa shinikizo la juu la mvuke. Mfano unaofuata unaonyesha utegemezi huu wa shinikizo la mvuke kwenye vikosi vya kuvutia vya intermolecular.
Kutokana na fomu zilizoonyeshwa za miundo kwa misombo hii minne, kuelezea shinikizo la mvuke la jamaa kwa suala la aina na kiwango cha IMF:
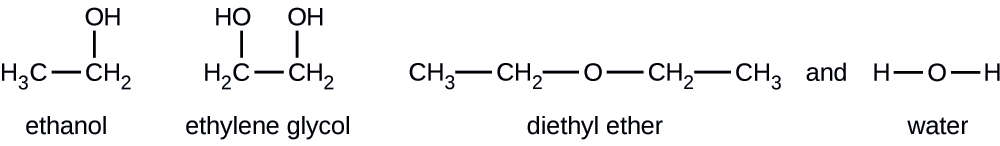
Suluhisho
Diethyl ether ina dipole ndogo sana na vivutio vyake vingi vya intermolecular ni vikosi vya London. Ingawa molekuli hii ni kubwa zaidi kati ya nne zinazozingatiwa, IMF zake ni dhaifu zaidi na, kwa sababu hiyo, molekuli zake hutoroka kwa urahisi kutoka kwenye kioevu. Pia ina shinikizo la juu la mvuke. Kutokana na ukubwa wake mdogo, ethanol inaonyesha nguvu za utawanyiko dhaifu kuliko ether ya diethyl. Hata hivyo, ethanol ina uwezo wa kuunganisha hidrojeni na, kwa hiyo, inaonyesha IMF yenye nguvu kwa ujumla, ambayo ina maana kwamba molekuli wachache hutoroka kutoka kioevu kwenye joto lolote, na hivyo ethanol ina shinikizo la chini la mvuke kuliko diethyl ether. Maji ni ndogo sana kuliko ama ya dutu uliopita na maonyesho kuwa vikosi utawanyiko, lakini kina hidrojeni yake bonding hutoa nguvu vivutio intermolecular, molekuli wachache kukimbia kioevu, na chini mvuke shinikizo kuliko kwa ama diethyl ether au ethanol. Ethylene glycol ina makundi mawili -OH, hivyo, kama maji, inaonyesha uhusiano mkubwa wa hidrojeni. Ni kubwa zaidi kuliko maji na hivyo uzoefu vikosi kubwa London. IMF yake ya jumla ni kubwa zaidi ya vitu hivi vinne, ambayo inamaanisha kiwango chake cha uvukizi kitakuwa cha polepole na, kwa hiyo, shinikizo lake la mvuke ni la chini kabisa.


