9.1: Pressão do gás
- Page ID
- 185474
- Defina a propriedade da pressão
- Defina e converta entre as unidades de medições de pressão
- Descreva a operação de ferramentas comuns para medir a pressão do gás
- Calcule a pressão a partir dos dados do manômetro
A atmosfera terrestre exerce uma pressão, assim como qualquer outro gás. Embora normalmente não percebamos a pressão atmosférica, somos sensíveis às mudanças de pressão — por exemplo, quando seus ouvidos “estalam” durante a decolagem e aterrissagem enquanto voa ou quando você mergulha na água. A pressão do gás é causada pela força exercida pelas moléculas de gás colidindo com as superfícies dos objetos (Figura\(\PageIndex{1}\)). Embora a força de cada colisão seja muito pequena, qualquer superfície de área apreciável sofre um grande número de colisões em pouco tempo, o que pode resultar em uma alta pressão. Na verdade, a pressão normal do ar é forte o suficiente para esmagar um recipiente de metal quando não é balanceada por igual pressão de dentro do recipiente.
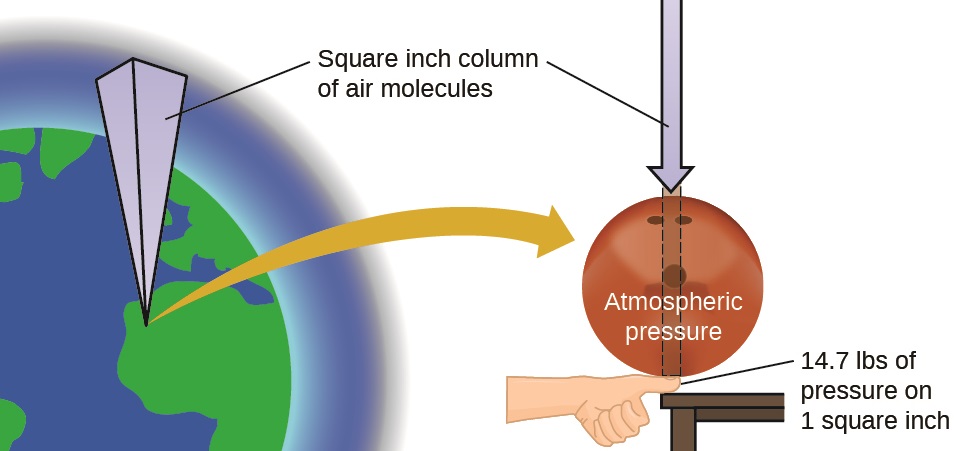
A pressão atmosférica é causada pelo peso da coluna de moléculas de ar na atmosfera acima de um objeto, como o vagão-tanque. Ao nível do mar, essa pressão é aproximadamente a mesma exercida por um elefante africano adulto em pé sobre um capacho ou por uma bola de boliche típica apoiada na miniatura. Podem parecer grandes quantidades, e são, mas a vida na Terra evoluiu sob essa pressão atmosférica. Se você realmente colocar uma bola de boliche na miniatura, a pressão sentida é o dobro da pressão normal e a sensação é desagradável.

Uma ilustração dramática da pressão atmosférica é fornecida neste breve vídeo, que mostra um vagão-tanque ferroviário implodindo quando sua pressão interna diminui.
A pressão é definida como a força exercida em uma determinada área:
\[P=\dfrac{F}{A} \label{9.2.1} \]
Como a pressão é diretamente proporcional à força e inversamente proporcional à área (Equação\ ref {9.2.1}), a pressão pode ser aumentada aumentando a quantidade de força ou diminuindo a área sobre a qual ela é aplicada. Da mesma forma, a pressão pode ser diminuída diminuindo a força ou aumentando a área.
Vamos aplicar a definição de pressão (Equação\ ref {9.2.1}) para determinar qual teria maior probabilidade de cair no gelo fino na Figura\(\PageIndex{2}\). —o elefante ou o patinador artístico?

Um grande elefante africano pode pesar 7 toneladas, apoiado em quatro pés, cada um com um diâmetro de cerca de 1,5 pés (área de pegada de 250 em 2), então a pressão exercida por cada pé é de cerca de 14 lb/in 2:
\[\mathrm{pressure\: per\: elephant\: foot=14,000\dfrac{lb}{elephant}×\dfrac{1\: elephant}{4\: feet}×\dfrac{1\: foot}{250\:in^2}=14\:lb/in^2} \label{9.2.2} \]
O patinador artístico pesa cerca de 120 libras, apoiado em duas lâminas de skate, cada uma com uma área de cerca de 2 em 2, então a pressão exercida por cada lâmina é de cerca de 30 lb/in 2:
\[\mathrm{pressure\: per\: skate\: blade=120\dfrac{lb}{skater}×\dfrac{1\: skater}{2\: blades}×\dfrac{1\: blade}{2\:in^2}=30\:lb/in^2} \label{9.2.3} \]
Embora o elefante seja mais de cem vezes mais pesado que o patinador, ele exerce menos da metade da pressão e, portanto, teria menos probabilidade de cair no gelo fino. Por outro lado, se a patinadora remover seus patins e ficar com os pés descalços (ou calçados normais) no gelo, a área maior sobre a qual seu peso é aplicado reduz muito a pressão exercida:
\[\mathrm{pressure\: per\: human\: foot=120\dfrac{lb}{skater}×\dfrac{1\: skater}{2\: feet}×\dfrac{1\: foot}{30\:in^2}=2\:lb/in^2} \label{9.2.4} \]
A unidade de pressão SI é o pascal (Pa), com 1 Pa = 1 N/m 2, onde N é o newton, uma unidade de força definida como 1 kg m/s 2. Um pascal é uma pressão pequena; em muitos casos, é mais conveniente usar unidades de quilopascal (1 kPa = 1000 Pa) ou bar (1 bar = 100.000 Pa). Nos Estados Unidos, a pressão geralmente é medida em libras de força em uma área de uma polegada quadrada — libras por polegada quadrada (psi) — por exemplo, em pneus de automóveis. A pressão também pode ser medida usando a unidade de atmosfera (atm), que originalmente representava a pressão média do ar ao nível do mar na latitude aproximada de Paris (45°). \(\PageIndex{1}\)A tabela fornece algumas informações sobre essas e algumas outras unidades comuns para medições de pressão
| Nome e abreviatura da unidade | Definição ou relação com outra unidade | Comentário |
|---|---|---|
| pascal (Pa) | 1 Pa = 1 N/m 2 | unidade IUPAC recomendada |
| quilopascal (kPa) | 1 kPa = 1000 Pa | |
| libras por polegada quadrada (psi) | a pressão do ar ao nível do mar é de ~ 14,7 psi | |
| atmosfera (atm) | 1 atm = 101.325 Pa | a pressão do ar ao nível do mar é de ~ 1 atm |
| bar (bar ou b) | 1 bar = 100.000 Pa (exatamente) | comumente usado em meteorologia |
| milibar (mbar ou mb) | 1000 mbar = 1 bar | |
| polegadas de mercúrio (em. Hg) | 1 pol. Hg = 3386 Pa | usado pela indústria da aviação, também alguns boletins meteorológicos |
| rasgar | \(\mathrm{1\: torr=\dfrac{1}{760}\:atm}\) | em homenagem a Evangelista Torricelli, inventor do barômetro |
| milímetros de mercúrio (mm Hg) | 1 mm Hg ~ 1 torr |
O Serviço Meteorológico Nacional dos Estados Unidos relata pressão em polegadas de Hg e milibares. Converta uma pressão de 29,2 pol. Entre em:
- rasgar
- caixa eletrônico
- KPa
- mbar
Solução
Esse é um problema de conversão de unidades. As relações entre as várias unidades de pressão são dadas na Tabela 9.2.1.
- \(\mathrm{29.2\cancel{in\: Hg}×\dfrac{25.4\cancel{mm}}{1\cancel{in}} ×\dfrac{1\: torr}{1\cancel{mm\: Hg}} =742\: torr}\)
- \(\mathrm{742\cancel{torr}×\dfrac{1\: atm}{760\cancel{torr}}=0.976\: atm}\)
- \(\mathrm{742\cancel{torr}×\dfrac{101.325\: kPa}{760\cancel{torr}}=98.9\: kPa}\)
- \(\mathrm{98.9\cancel{kPa}×\dfrac{1000\cancel{Pa}}{1\cancel{kPa}} \times \dfrac{1\cancel{bar}}{100,000\cancel{Pa}} \times\dfrac{1000\: mbar}{1\cancel{bar}}=989\: mbar}\)
Uma pressão barométrica típica em Kansas City é de 740 torr. O que é essa pressão nas atmosferas, em milímetros de mercúrio, em quilopascais e em bar?
- Resposta
-
0,974 atm; 740 mm Hg; 98,7 kPa; 0,987 bar
Podemos medir a pressão atmosférica, a força exercida pela atmosfera na superfície da Terra, com um barômetro (Figura\(\PageIndex{3}\)). Um barômetro é um tubo de vidro que é fechado em uma extremidade, preenchido com um líquido não volátil, como mercúrio, e então invertido e imerso em um recipiente desse líquido. A atmosfera exerce pressão sobre o líquido fora do tubo, a coluna de líquido exerce pressão dentro do tubo e a pressão na superfície do líquido é a mesma dentro e fora do tubo. A altura do líquido no tubo é, portanto, proporcional à pressão exercida pela atmosfera.
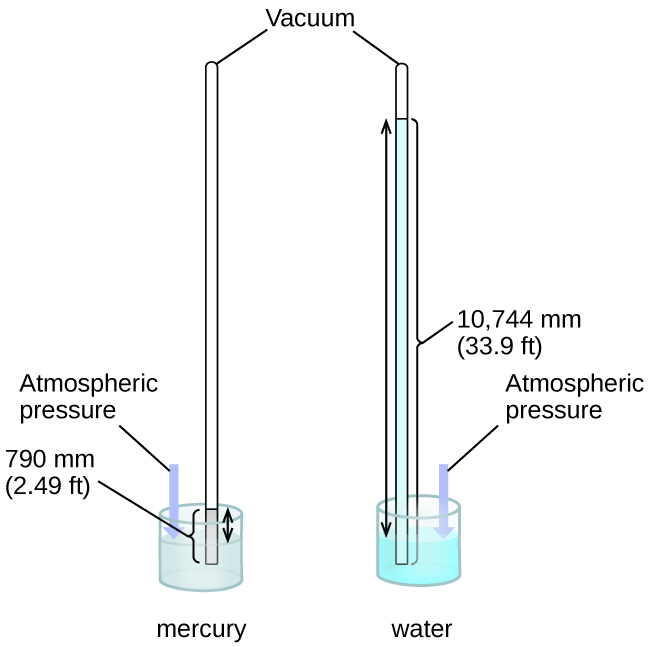
Se o líquido for água, a pressão atmosférica normal suportará uma coluna de água com mais de 10 metros de altura, o que é bastante inconveniente para fazer (e ler) um barômetro. Como o mercúrio (Hg) é cerca de 13,6 vezes mais denso que a água, um barômetro de mercúrio só precisa ter\(\dfrac{1}{13.6}\) a altura de um barômetro de água — um tamanho mais adequado. A pressão atmosférica padrão de 1 atm ao nível do mar (101.325 Pa) corresponde a uma coluna de mercúrio com cerca de 760 mm (29,92 pol.) de altura. O torr foi originalmente planejado para ser uma unidade igual a um milímetro de mercúrio, mas não corresponde mais exatamente. A pressão exercida por um fluido devido à gravidade é conhecida como pressão hidrostática, p:
\[p=hρg \label{9.2.5} \]
onde
- \(h\)é a altura do fluido,
- \(ρ\)é a densidade do fluido e
- \(g\)é a aceleração devido à gravidade.
Mostre o cálculo que apóia a afirmação de que a pressão atmosférica perto do nível do mar corresponde à pressão exercida por uma coluna de mercúrio com cerca de 760 mm de altura. A densidade do mercúrio =\(13.6 \,g/cm^3\).
Solução
A pressão hidrostática é dada pela Equação\ ref {9.2.5}\(h = 760 \,mm\), com\(ρ = 13.6\, g/cm^3\),,\(g = 9.81 \,m/s^2\) e. Inserir esses valores na Equação\ ref {9.2.5} e fazer as conversões de unidades necessárias nos dará o valor que buscamos. (Nota: Esperamos encontrar uma pressão de ~ 101.325 Pa:)
\[\mathrm{101,325\:\mathit{N}/m^2=101,325\:\dfrac{kg·m/s^2}{m^2}=101,325\:\dfrac{kg}{m·s^2}} \nonumber \]
\ [\ begin {align*}
p&\ mathrm {=\ left (760\: mm×\ dfrac {1\: m} {1000\: mm}\ direita) ×\ left (\ dfrac {13.6\: g} {1\ :cm^3} ×\ dfrac {1\: kg} {1000\: g} ×\ dfrac {(100\ cm:) ^3} {(1\: m) ^3}\ direita) ×\ esquerda (\ dfrac {9,81\: m} {1\ :s^2}\ direita)}\\ [4pt]
&\ mathrm {=( 0,760\: m) (13.600\ :kg/m^3) (9,81\ :m/s^2) =1. 01\ times 10^5\ :kg/ms^2=1,01 × 10^5\ mathit {N} /m^2}\\[4pt] & \mathrm{=1.01×10^5\:Pa} \end {align*} \nonumber \]
Calcule a altura de uma coluna de água a 25 °C que corresponde à pressão atmosférica normal. A densidade da água a essa temperatura é de 1,0 g/cm 3.
- Resposta
-
10,3 mm
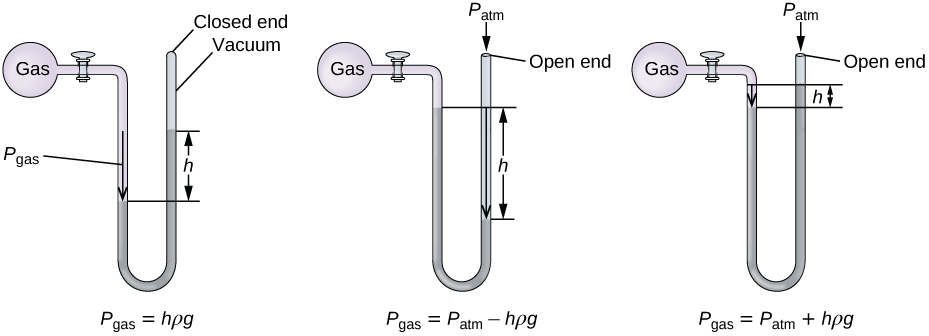
Um manômetro é um dispositivo semelhante a um barômetro que pode ser usado para medir a pressão de um gás preso em um recipiente. Um manômetro de extremidade fechada é um tubo em forma de U com um braço fechado, um braço que se conecta ao gás a ser medido e um líquido não volátil (geralmente mercúrio) no meio. Assim como em um barômetro, a distância entre os níveis de líquido nos dois braços do tubo (h no diagrama) é proporcional à pressão do gás no recipiente. Um manômetro de extremidade aberta (Figura\(\PageIndex{3}\)) é o mesmo que um manômetro de extremidade fechada, mas um de seus braços está aberto para a atmosfera. Nesse caso, a distância entre os níveis do líquido corresponde à diferença de pressão entre o gás no recipiente e a atmosfera.
A pressão de uma amostra de gás é medida ao nível do mar com um manômetro de Hg (mercúrio) de extremidade aberta, conforme mostrado abaixo. Determine a pressão do gás em:
- mm Hg
- caixa eletrônico
- KPa
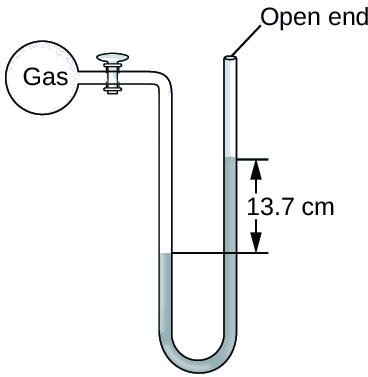
Solução
A pressão do gás é igual à pressão hidrostática devido a uma coluna de mercúrio de altura 13,7 cm mais a pressão da atmosfera ao nível do mar. (A pressão na linha horizontal inferior é igual em ambos os lados do tubo. A pressão à esquerda é devida ao gás e a pressão à direita é devida a 13,7 cm de Hg mais a pressão atmosférica.)
- Em mm Hg, isso é: 137 mm Hg + 760 mm Hg = 897 mm Hg
- \(\mathrm{897\cancel{mm Hg}×\dfrac{1\: atm}{760\cancel{mm Hg}}=1.18\: atm}\)
- \(\mathrm{1.18\cancel{atm}×\dfrac{101.325\: kPa}{1\cancel{atm}}=1.20×10^2\:kPa}\)
A pressão de uma amostra de gás é medida ao nível do mar com um manômetro de Hg de extremidade aberta, conforme mostrado abaixo Determine a pressão do gás em:
- mm Hg
- caixa eletrônico
- KPa
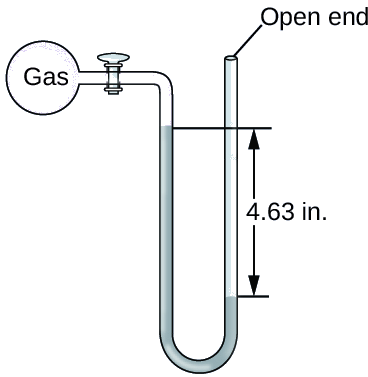
Responda a um
-
642 mm Hg
- Resposta b
-
0,845 atm
- Resposta c
-
85,6 kPa
A pressão arterial é medida usando um dispositivo chamado esfigmomanômetro (esfigmomanômetro grego = “pulso”). Consiste em um manguito inflável para restringir o fluxo sanguíneo, um manômetro para medir a pressão e um método para determinar quando o fluxo sanguíneo começa e quando ele é impedido (Figura\(\PageIndex{5}\)). Desde sua invenção em 1881, ele tem sido um dispositivo médico essencial. Existem muitos tipos de esfigmomanômetros: manuais que requerem um estetoscópio e são usados por profissionais médicos; os de mercúrio, usados quando a maior precisão é necessária; os mecânicos menos precisos; e os digitais que podem ser usados com pouco treinamento, mas com limitações. Ao usar um esfigmomanômetro, o manguito é colocado ao redor do braço e inflado até que o fluxo sanguíneo seja completamente bloqueado e, em seguida, liberado lentamente. À medida que o coração bate, o sangue forçado pelas artérias causa um aumento na pressão. Esse aumento na pressão na qual o fluxo sanguíneo começa é a pressão sistólica — o pico de pressão no ciclo cardíaco. Quando a pressão do manguito é igual à pressão arterial sistólica, o sangue passa pelo manguito, criando sons audíveis que podem ser ouvidos usando um estetoscópio. Isso é seguido por uma diminuição na pressão à medida que os ventrículos do coração se preparam para outra batida. À medida que a pressão do manguito continua diminuindo, eventualmente o som não é mais ouvido; essa é a pressão diastólica — a pressão mais baixa (fase de repouso) no ciclo cardíaco. As unidades de pressão arterial de um esfigmomanômetro são em termos de milímetros de mercúrio (mm Hg).

Meteorologia, Climatologia e Ciência Atmosférica
Ao longo dos tempos, as pessoas observaram nuvens, ventos e precipitações, tentando discernir padrões e fazer previsões: quando é melhor plantar e colher; se é seguro partir em uma viagem marítima; e muito mais. Agora enfrentamos desafios climáticos e atmosféricos complexos que terão um grande impacto em nossa civilização e no ecossistema. Várias disciplinas científicas diferentes usam princípios químicos para nos ajudar a entender melhor o clima, a atmosfera e o clima. São meteorologia, climatologia e ciências atmosféricas. Meteorologia é o estudo da atmosfera, dos fenômenos atmosféricos e dos efeitos atmosféricos no clima da Terra. Os meteorologistas buscam entender e prever o clima no curto prazo, o que pode salvar vidas e beneficiar a economia. As previsões meteorológicas (Figura\(\PageIndex{5}\)) são o resultado de milhares de medições de pressão do ar, temperatura e similares, que são compiladas, modeladas e analisadas em centros meteorológicos em todo o mundo.
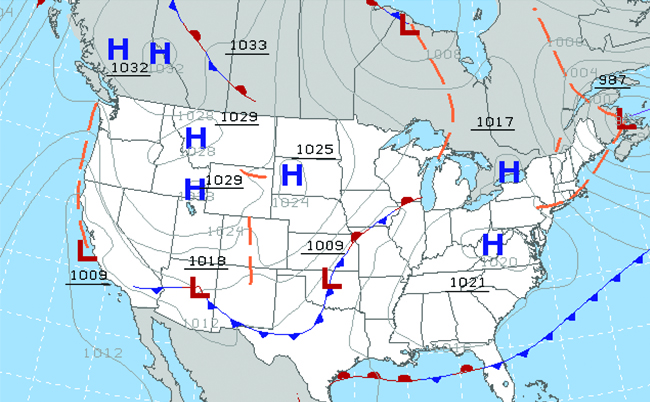
Em termos climáticos, os sistemas de baixa pressão ocorrem quando a pressão atmosférica da superfície terrestre é menor do que a do ambiente circundante: o ar úmido sobe e condensa, produzindo nuvens. O movimento da umidade e do ar em várias frentes climáticas instiga a maioria dos eventos climáticos.
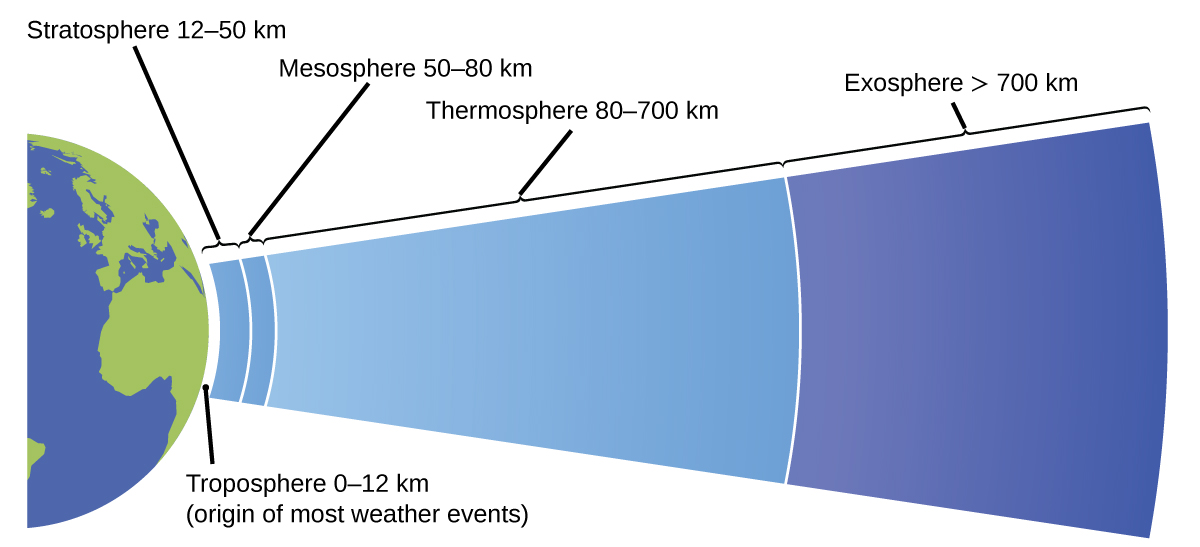
A atmosfera é a camada gasosa que envolve um planeta. A atmosfera da Terra, que tem aproximadamente 100-125 km de espessura, consiste em aproximadamente 78,1% de nitrogênio e 21,0% de oxigênio e pode ser subdividida ainda mais nas regiões mostradas na Figura\(\PageIndex{7}\): a exosfera (mais distante da Terra, > 700 km acima do nível do mar), a termosfera (80—700 km), a mesosfera (50—80 km), a mesosfera (50—80 km), a estratosfera (segundo nível mais baixo da nossa atmosfera, 12—50 km acima do nível do mar) e a troposfera (até 12 km acima do nível do mar, cerca de 80% da atmosfera terrestre em massa e a camada de origem da maioria dos eventos climáticos). À medida que você sobe na troposfera, a densidade do ar e a temperatura diminuem.
Climatologia é o estudo do clima, das condições climáticas médias em longos períodos de tempo, usando dados atmosféricos. No entanto, os climatologistas estudam padrões e efeitos que ocorrem ao longo de décadas, séculos e milênios, em vez de períodos mais curtos de horas, dias e semanas, como os meteorologistas. A ciência atmosférica é um campo ainda mais amplo, combinando meteorologia, climatologia e outras disciplinas científicas que estudam a atmosfera.
Resumo
Os gases exercem pressão, que é força por unidade de área. A pressão de um gás pode ser expressa na unidade SI de pascal ou quilopascal, bem como em muitas outras unidades, incluindo torr, atmosfera e bar. A pressão atmosférica é medida usando um barômetro; outras pressões de gás podem ser medidas usando um dos vários tipos de manômetros.
Equações chave
- \(P=\dfrac{F}{A}\)
- p = hρ g
Glossário
- atmosfera (atm)
- unidade de pressão; 1 atm = 101.325 Pa
- barra
- (bar ou b) unidade de pressão; 1 bar = 100.000 Pa
- barômetro
- dispositivo usado para medir a pressão atmosférica
- pressão hidrostática
- pressão exercida por um fluido devido à gravidade
- manômetro
- dispositivo usado para medir a pressão de um gás preso em um recipiente
- pascal (Pa)
- Unidade de pressão SI; 1 Pa = 1 N/m 2
- libras por polegada quadrada (psi)
- unidade de pressão comum nos EUA
- pressão
- força exercida por unidade de área
- rasgar
- unidade de pressão;\(\mathrm{1\: torr=\dfrac{1}{760}\,atm}\)


