12.1: Espontaneidade
- Page ID
- 195547
Habilidades para desenvolver
- Faça a distinção entre processos espontâneos e não espontâneos
- Descreva a dispersão de matéria e energia que acompanha certos processos espontâneos
Nesta seção, considere as diferenças entre dois tipos de mudanças em um sistema: aquelas que ocorrem espontaneamente e aquelas que ocorrem pela força. Ao fazer isso, entenderemos por que alguns sistemas são naturalmente inclinados a mudar em uma direção sob certas condições e com que rapidez ou lentidão essa mudança natural ocorre. Também obteremos uma visão de como a espontaneidade de um processo afeta a distribuição de energia e matéria dentro do sistema.
Processos espontâneos e não espontâneos
Os processos têm uma tendência natural de ocorrer em uma direção sob um determinado conjunto de condições. A água fluirá naturalmente em declive, mas o fluxo em subida requer intervenção externa, como o uso de uma bomba. O ferro exposto à atmosfera terrestre corroerá, mas a ferrugem não é convertida em ferro sem tratamento químico intencional. Um processo espontâneo é aquele que ocorre naturalmente sob certas condições. Um processo não espontâneo, por outro lado, não ocorrerá a menos que seja “conduzido” pela entrada contínua de energia de uma fonte externa. Um processo que é espontâneo em uma direção sob um determinado conjunto de condições não é espontâneo na direção inversa. À temperatura ambiente e à pressão atmosférica típica, por exemplo, o gelo derrete espontaneamente, mas a água não congela espontaneamente.
A espontaneidade de um processo não está correlacionada com a velocidade do processo. Uma mudança espontânea pode ser tão rápida que é essencialmente instantânea ou tão lenta que não pode ser observada em nenhum período prático de tempo. Para ilustrar esse conceito, considere o decaimento dos isótopos radioativos, um tópico tratado mais detalhadamente no capítulo sobre química nuclear. O decaimento radioativo é, por definição, um processo espontâneo no qual os núcleos de isótopos instáveis emitem radiação à medida que são convertidos em núcleos mais estáveis. Todos os processos de decaimento ocorrem espontaneamente, mas as taxas nas quais diferentes isótopos decaem variam amplamente. O tecnécio-99M é um radioisótopo popular para estudos de imagens médicas que sofre um decaimento relativamente rápido e apresenta uma meia-vida de cerca de seis horas. O urânio-238 é o isótopo mais abundante de urânio, e sua decomposição ocorre muito mais lentamente, exibindo uma meia-vida de mais de quatro bilhões de anos (Figura\(\PageIndex{1}\)).
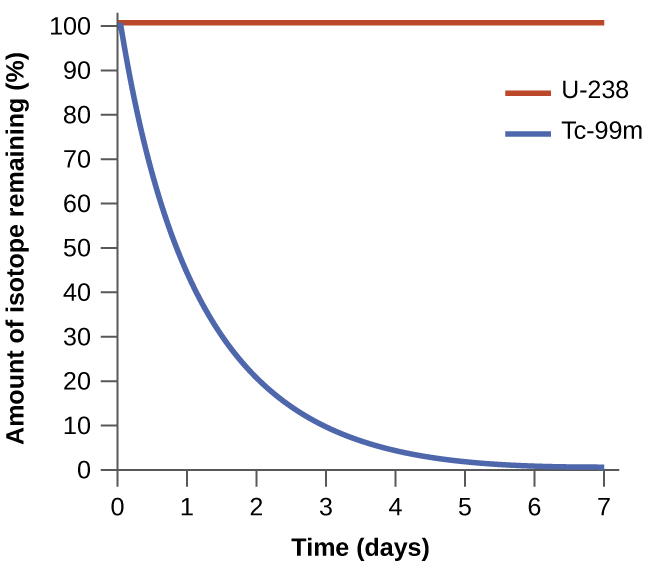
Como outro exemplo, considere a conversão de diamante em grafite (Figura\(\PageIndex{2}\)).
\[\ce{C}_{(s,\textrm{ diamond})}⟶\ce{C}_{(s,\textrm{ graphite})} \label{Eq1}\]
O diagrama de fases do carbono indica que o grafite é a forma estável desse elemento sob pressão atmosférica ambiente, enquanto o diamante é o alótropo estável em pressões muito altas, como as presentes durante sua formação geológica. Cálculos termodinâmicos do tipo descrito na última seção deste capítulo indicam que a conversão de diamante em grafite à pressão ambiente ocorre espontaneamente, mas observa-se que os diamantes existem e persistem nessas condições. Embora o processo seja espontâneo em condições ambientais típicas, sua taxa é extremamente lenta e, portanto, para todos os fins práticos, os diamantes são de fato “para sempre”. Situações como essas enfatizam a importante distinção entre os aspectos termodinâmicos e cinéticos de um processo. Nesse caso específico, diz-se que os diamantes são termodinamicamente instáveis, mas cineticamente estáveis em condições ambientais.
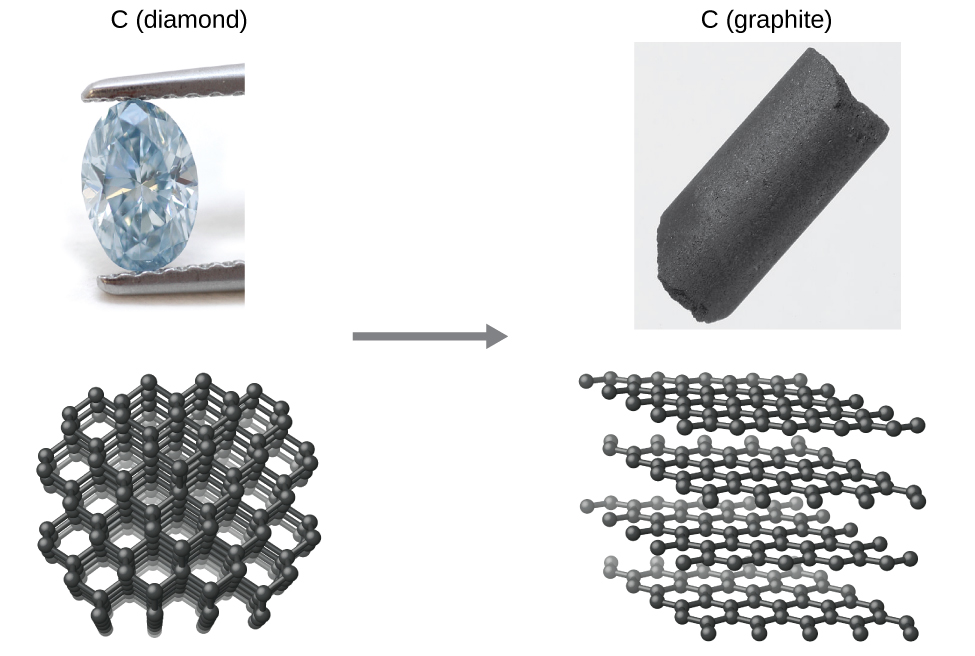
Figura\(\PageIndex{2}\):The conversion of carbon from the diamond allotrope to the graphite allotrope is spontaneous at ambient pressure, but its rate is immeasurably slow at low to moderate temperatures. This process is known as graphitization, and its rate can be increased to easily measurable values at temperatures in the 1000–2000 K range. (credit "diamond" photo: modification of work by "Fancy Diamonds"/Flickr; credit "graphite" photo: modificaton of work by images-of-elements.com/carbon.php)
Dispersal of Matter and Energy
As we extend our discussion of thermodynamic concepts toward the objective of predicting spontaneity, consider now an isolated system consisting of two flasks connected with a closed valve. Initially there is an ideal gas on the left and a vacuum on the right (Figure \(\PageIndex{3}\)). When the valve is opened, the gas spontaneously expands to fill both flasks. Recalling the definition of pressure-volume work from the chapter on thermochemistry, note that no work has been done because the pressure in a vacuum is zero.
\[w=−PΔV=0 \;\;\; \mathrm{(P=0\: in\: a\: vaccum)} \label{Eq2}\]
Note as well that since the system is isolated, no heat has been exchanged with the surroundings (q = 0). The first law of thermodynamics confirms that there has been no change in the system’s internal energy as a result of this process.
\[ΔU=q+w=0+0=0 \label{Eq3}\]
The spontaneity of this process is therefore not a consequence of any change in energy that accompanies the process. Instead, the driving force appears to be related to the greater, more uniform dispersal of matter that results when the gas is allowed to expand. Initially, the system was comprised of one flask containing matter and another flask containing nothing. After the spontaneous process took place, the matter was distributed both more widely (occupying twice its original volume) and more uniformly (present in equal amounts in each flask).
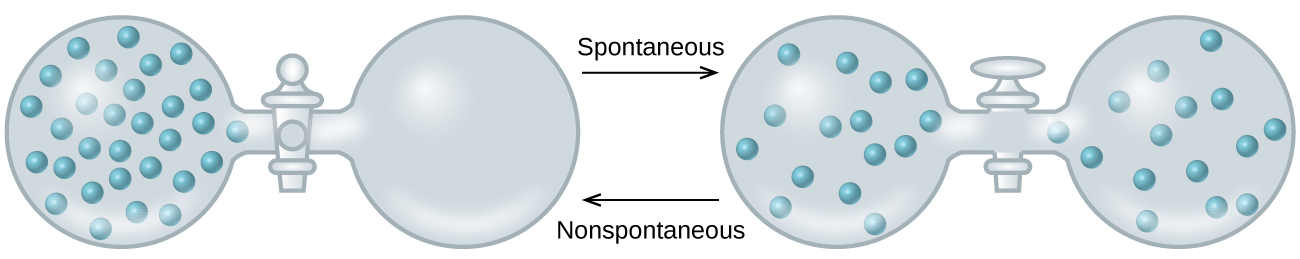
Figura\(\PageIndex{3}\):An isolated system consists of an ideal gas in one flask that is connected by a closed valve to a second flask containing a vacuum. Once the valve is opened, the gas spontaneously becomes evenly distributed between the flasks.
Now consider two objects at different temperatures: object X at temperature TX and object Y at temperature TY, with TX > TY (Figure \(\PageIndex{4}\)). When these objects come into contact, heat spontaneously flows from the hotter object (X) to the colder one (Y). This corresponds to a loss of thermal energy by X and a gain of thermal energy by Y.
\[q_\ce{X}<0 \hspace{20px} \ce{and} \hspace{20px} q_\ce{Y}=−q_\ce{X}>0 \label{Eq4}\]
From the perspective of this two-object system, there was no net gain or loss of thermal energy, rather the available thermal energy was redistributed among the two objects. This spontaneous process resulted in a more uniform dispersal of energy.

Figura: Quando\(\PageIndex{4}\) dois objetos em temperaturas diferentes entram em contato, o calor flui espontaneamente do objeto mais quente para o mais frio.
Conforme ilustrado pelos dois processos descritos, um fator importante na determinação da espontaneidade de um processo é até que ponto ele altera a dispersão ou distribuição de matéria e/ou energia. Em cada caso, ocorreu um processo espontâneo que resultou em uma distribuição mais uniforme de matéria ou energia.
Exemplo\(\PageIndex{1}\): Redistribuição de matéria durante um processo espontâneo
Descreva como a matéria é redistribuída quando os seguintes processos espontâneos ocorrem:
- Um sólido sublima.
- Um gás se condensa.
- Uma gota de corante alimentar adicionada a um copo de água forma uma solução com cor uniforme.
Solução

Figura\(\PageIndex{5}\) :( crédito a: modificação da obra de Jenny Downing; crédito b: modificação da obra de “Fuzzy Gerdes” /Flickr; crédito c: modificação da obra de Sahar Atwa)
- (a) A sublimação é a conversão de um sólido (densidade relativamente alta) em um gás (densidade muito menor). Esse processo produz uma dispersão muito maior da matéria, já que as moléculas ocuparão um volume muito maior após a transição do sólido para o gás.
- (b) A condensação é a conversão de um gás (densidade relativamente baixa) em um líquido (densidade muito maior). Esse processo produz uma dispersão muito menor da matéria, já que as moléculas ocuparão um volume muito menor após a transição do sólido para o gás.
- (c) O processo em questão é a diluição. As moléculas de corante alimentar ocupam inicialmente um volume muito menor (a gota da solução de corante) do que ocupam quando o processo é concluído (no copo cheio de água). O processo, portanto, implica uma maior dispersão da matéria. O processo também pode produzir uma dispersão mais uniforme da matéria, já que o estado inicial do sistema envolve duas regiões de diferentes concentrações de corante (alta na gota, zero na água) e o estado final do sistema contém uma única concentração de corante por toda parte.
Exercício\(\PageIndex{1}\)
Descreva como a matéria e/ou a energia são redistribuídas quando você esvazia um recipiente de ar comprimido em uma sala.
Resposta:
Este também é um processo de diluição, análogo ao exemplo (c). Isso implica uma dispersão maior e mais uniforme da matéria, pois o ar comprimido no recipiente pode se expandir para o ar de baixa pressão da sala.
Resumo
Os processos químicos e físicos têm uma tendência natural de ocorrer em uma direção sob certas condições. Um processo espontâneo ocorre sem a necessidade de uma entrada contínua de energia de alguma fonte externa, enquanto um processo não espontâneo exige isso. Sistemas que passam por um processo espontâneo podem ou não experimentar um ganho ou perda de energia, mas eles experimentarão uma mudança na forma como a matéria e/ou energia é distribuída dentro do sistema.
Glossário
- processo não espontâneo
- processo que requer entrada contínua de energia de uma fonte externa
- mudança espontânea
- processo que ocorre sem uma entrada contínua de energia de uma fonte externa


