35.2: Como os neurônios se comunicam
- Page ID
- 182179
Habilidades para desenvolver
- Descreva a base do potencial da membrana em repouso
- Explicar os estágios de um potencial de ação e como os potenciais de ação são propagados
- Explicar as semelhanças e diferenças entre sinapses químicas e elétricas
- Descreva a potenciação e a depressão a longo
Todas as funções desempenhadas pelo sistema nervoso — desde um simples reflexo motor até funções mais avançadas, como tomar uma memória ou tomar uma decisão — exigem que os neurônios se comuniquem entre si. Enquanto os humanos usam palavras e linguagem corporal para se comunicar, os neurônios usam sinais elétricos e químicos. Assim como uma pessoa em um comitê, um neurônio geralmente recebe e sintetiza mensagens de vários outros neurônios antes de “tomar a decisão” de enviar a mensagem para outros neurônios.
Transmissão do impulso nervoso dentro de um neurônio
Para que o sistema nervoso funcione, os neurônios devem ser capazes de enviar e receber sinais. Esses sinais são possíveis porque cada neurônio tem uma membrana celular carregada (uma diferença de voltagem entre o interior e o exterior), e a carga dessa membrana pode mudar em resposta às moléculas de neurotransmissores liberadas por outros neurônios e estímulos ambientais. Para entender como os neurônios se comunicam, é preciso primeiro entender a base da carga basal ou da membrana “em repouso”.
Membranas com carga neuronal
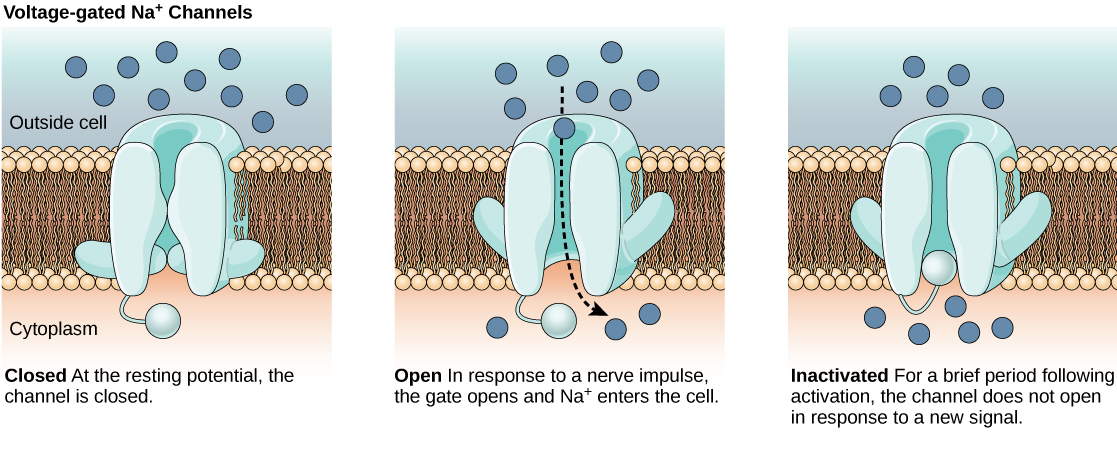
A membrana lipídica bicamada que envolve um neurônio é impermeável a moléculas ou íons carregados. Para entrar ou sair do neurônio, os íons devem passar por proteínas especiais chamadas canais iônicos que atravessam a membrana. Os canais de íons têm configurações diferentes: abertos, fechados e inativos, conforme ilustrado na Figura\(\PageIndex{1}\). Alguns canais iônicos precisam ser ativados para se abrirem e permitirem que os íons entrem ou saiam da célula. Esses canais iônicos são sensíveis ao meio ambiente e podem mudar sua forma de acordo. Os canais iônicos que alteram sua estrutura em resposta às mudanças de tensão são chamados de canais iônicos dependentes de voltagem. Os canais iônicos dependentes de voltagem regulam as concentrações relativas de diferentes íons dentro e fora da célula. A diferença na carga total entre o interior e o exterior da célula é chamada de potencial de membrana.
Link para o aprendizado
Este vídeo discute a base do potencial da membrana em repouso.
Potencial de membrana de descanso
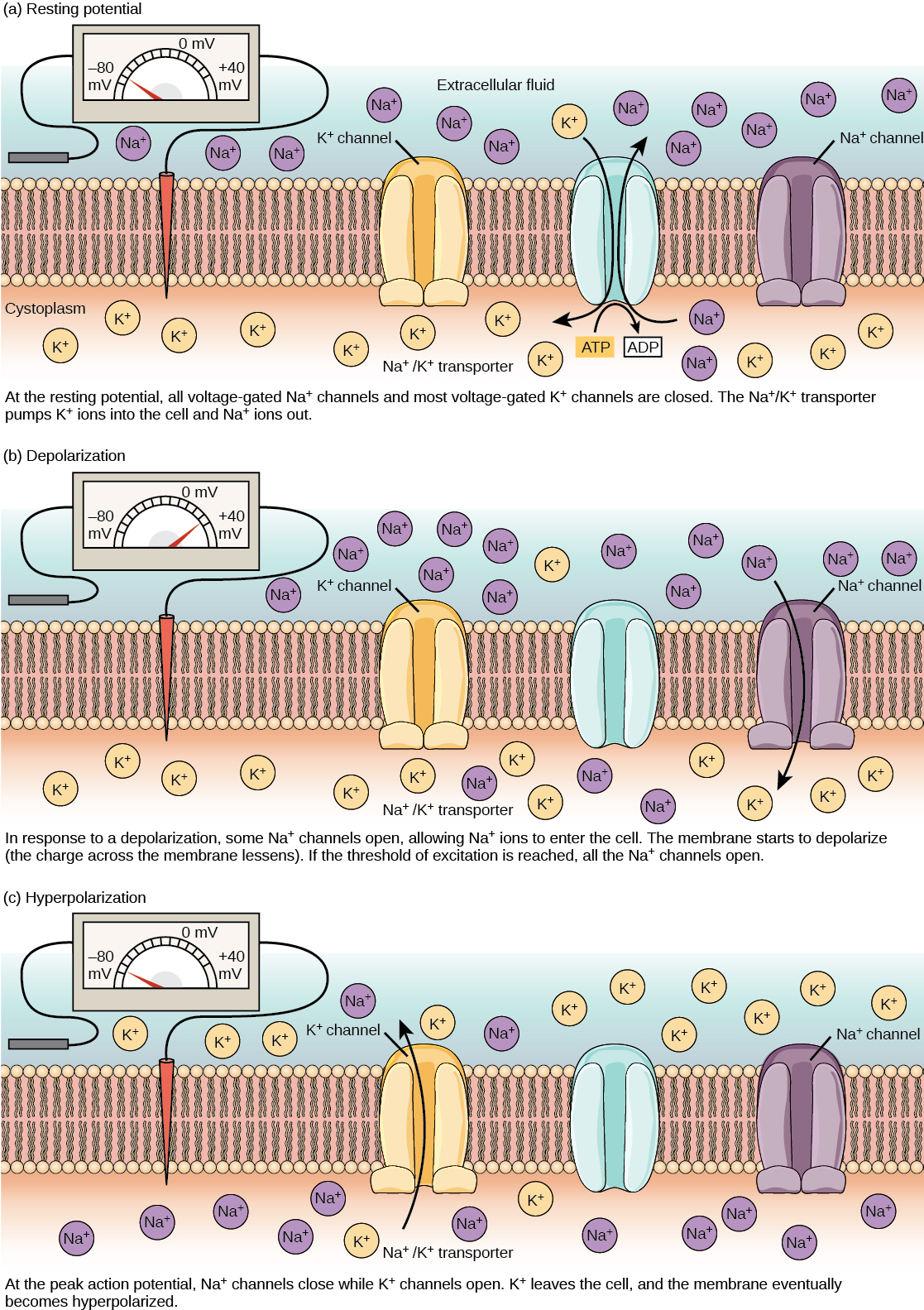
Um neurônio em repouso tem carga negativa: o interior de uma célula é aproximadamente 70 milivolts mais negativo do que o externo (−70 mV, observe que esse número varia de acordo com o tipo de neurônio e a espécie). Essa voltagem é chamada de potencial de membrana em repouso; é causada por diferenças nas concentrações de íons dentro e fora da célula. Se a membrana fosse igualmente permeável a todos os íons, cada tipo de íon fluiria pela membrana e o sistema alcançaria o equilíbrio. Como os íons não podem simplesmente atravessar a membrana à vontade, existem diferentes concentrações de vários íons dentro e fora da célula, conforme mostrado na tabela abaixo. A diferença no número de íons de potássio carregados positivamente (K +) dentro e fora da célula domina o potencial da membrana em repouso (Figura\(\PageIndex{2}\)). Quando a membrana está em repouso, os íons K+ se acumulam dentro da célula devido a um movimento líquido com o gradiente de concentração. O potencial negativo da membrana em repouso é criado e mantido pelo aumento da concentração de cátions fora da célula (no fluido extracelular) em relação ao interior da célula (no citoplasma). A carga negativa dentro da célula é criada pela membrana celular ser mais permeável ao movimento do íon potássio do que ao movimento do íon sódio. Nos neurônios, os íons potássio são mantidos em altas concentrações dentro da célula, enquanto os íons de sódio são mantidos em altas concentrações fora da célula. A célula possui canais de vazamento de potássio e sódio que permitem que os dois cátions se difundam em seu gradiente de concentração. No entanto, os neurônios têm muito mais canais de vazamento de potássio do que canais de vazamento de sódio. Portanto, o potássio se difunde para fora da célula em uma taxa muito mais rápida do que o sódio vaza. Como mais cátions estão saindo da célula do que estão entrando, isso faz com que o interior da célula seja carregado negativamente em relação ao exterior da célula. As ações da bomba de sódio e potássio ajudam a manter o potencial de repouso, uma vez estabelecido. Lembre-se de que as bombas de sódio e potássio trazem dois íons K + para a célula enquanto removem três íons Na + por ATP consumido. À medida que mais cátions são expelidos da célula do que absorvidos, o interior da célula permanece carregado negativamente em relação ao fluido extracelular. Deve-se notar que os íons de cálcio (Cl —) tendem a se acumular fora da célula porque são repelidos por proteínas carregadas negativamente dentro do citoplasma.
| Íon | Concentração extracelular (mM) | Concentração intracelular (mM) | Proporção externa/interna |
|---|---|---|---|
| Não + | 145 | 12 | 12 |
| K + | 4 | 155 | 0,026 |
| Cl − | 120 | 4 | 30 |
| Ânions orgânicos (A−) | — | 100 |
potencial de ação
Um neurônio pode receber entrada de outros neurônios e, se essa entrada for forte o suficiente, enviar o sinal para os neurônios a jusante. A transmissão de um sinal entre neurônios geralmente é transmitida por uma substância química chamada neurotransmissor. A transmissão de um sinal dentro de um neurônio (do dendrito ao terminal do axônio) é realizada por uma breve reversão do potencial da membrana em repouso chamada potencial de ação. Quando as moléculas do neurotransmissor se ligam aos receptores localizados nos dendritos de um neurônio, os canais iônicos se abrem. Nas sinapses excitatórias, essa abertura permite que íons positivos entrem no neurônio e resulta na despolarização da membrana — uma diminuição na diferença de voltagem entre o interior e o exterior do neurônio. Um estímulo de uma célula sensorial ou de outro neurônio despolariza o neurônio alvo até seu potencial limite (-55 mV). Os canais Na+ na colina do axônio se abrem, permitindo que íons positivos entrem na célula (Figura\(\PageIndex{3}\) e Figura\(\PageIndex{4}\)). Quando os canais de sódio se abrem, o neurônio se despolariza completamente até um potencial de membrana de cerca de +40 mV. Os potenciais de ação são considerados um evento do tipo “tudo ou nada”, pois, uma vez atingido o potencial limiar, o neurônio sempre se despolariza completamente. Quando a despolarização estiver concluída, a célula agora deve “redefinir” a voltagem da membrana de volta ao potencial de repouso. Para fazer isso, os canais Na + fecham e não podem ser abertos. Isso inicia o período refratário do neurônio, no qual ele não pode produzir outro potencial de ação porque seus canais de sódio não se abrirão. Ao mesmo tempo, os canais K + dependentes de voltagem se abrem, permitindo que K + saia da célula. Quando os íons K + saem da célula, o potencial da membrana mais uma vez se torna negativo. A difusão de K+ para fora da célula, na verdade, hiperpolariza a célula, na medida em que o potencial de membrana se torna mais negativo do que o potencial normal de repouso da célula. Nesse ponto, os canais de sódio retornarão ao estado de repouso, o que significa que estão prontos para se abrir novamente se o potencial da membrana exceder novamente o potencial limite. Eventualmente, os íons K + extras se difundem para fora da célula através dos canais de vazamento de potássio, trazendo a célula de seu estado hiperpolarizado, de volta ao seu potencial de membrana de repouso.
Conexão artística
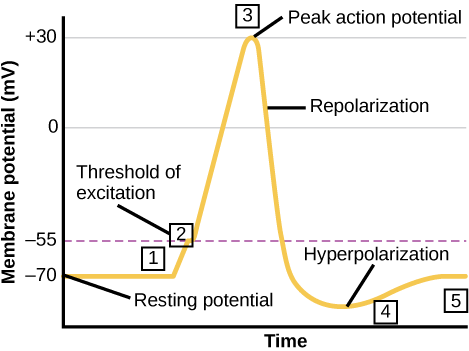
Os bloqueadores dos canais de potássio, como a amiodarona e a procainamida, que são usados para tratar a atividade elétrica anormal no coração, chamada de disritmia cardíaca, impedem o movimento de K + através de canais K + dependentes de voltagem. Qual parte do potencial de ação você esperaria que os canais de potássio afetassem?
Link para o aprendizado
Este vídeo apresenta uma visão geral do potencial de ação.
Mielina e a propagação do potencial de ação
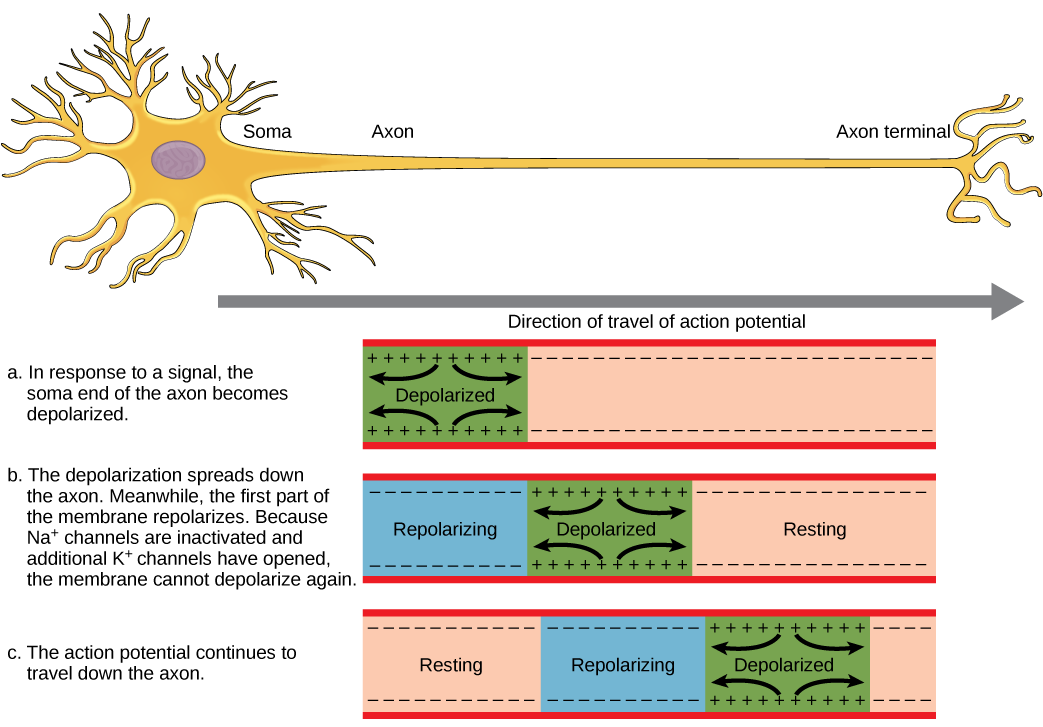
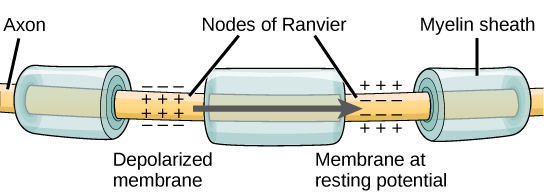
Para que um potencial de ação comunique informações a outro neurônio, ele deve viajar ao longo do axônio e alcançar os terminais do axônio, onde pode iniciar a liberação do neurotransmissor. A velocidade de condução de um potencial de ação ao longo de um axônio é influenciada pelo diâmetro do axônio e pela resistência do axônio ao vazamento de corrente. A mielina atua como um isolante que impede que a corrente saia do axônio; isso aumenta a velocidade de condução do potencial de ação. Em doenças desmielinizantes, como a esclerose múltipla, a condução do potencial de ação diminui porque a corrente vaza de áreas axonais previamente isoladas. Os nódulos de Ranvier, ilustrados na Figura,\(\PageIndex{5}\) são lacunas na bainha de mielina ao longo do axônio. Esses espaços não mielinizados têm cerca de um micrômetro de comprimento e contêm canais de Na + e K + dependentes de tensão. O fluxo de íons através desses canais, particularmente os canais Na +, regenera o potencial de ação repetidamente ao longo do axônio. Esse “salto” do potencial de ação de um nó para o outro é chamado de condução saltatória. Se os nós de Ranvier não estivessem presentes ao longo de um axônio, o potencial de ação se propagaria muito lentamente, pois os canais Na + e K + teriam que regenerar continuamente os potenciais de ação em cada ponto ao longo do axônio, em vez de em pontos específicos. Os nós de Ranvier também economizam energia para o neurônio, pois os canais só precisam estar presentes nos nós e não ao longo de todo o axônio.
Transmissão sináptica
A sinapse ou “lacuna” é o local onde a informação é transmitida de um neurônio para outro. As sinapses geralmente se formam entre os terminais do axônio e as espinhas dendríticas, mas isso não é universalmente verdadeiro. Existem também sinapses de corpo axônio para axônio, dendrito para dendrito e axônio para célula. O neurônio que transmite o sinal é chamado de neurônio pré-sináptico, e o neurônio que recebe o sinal é chamado de neurônio pós-sináptico. Observe que essas designações são relativas a uma sinapse específica — a maioria dos neurônios é pré-sináptica e pós-sináptica. Existem dois tipos de sinapses: química e elétrica.
Sinapse química
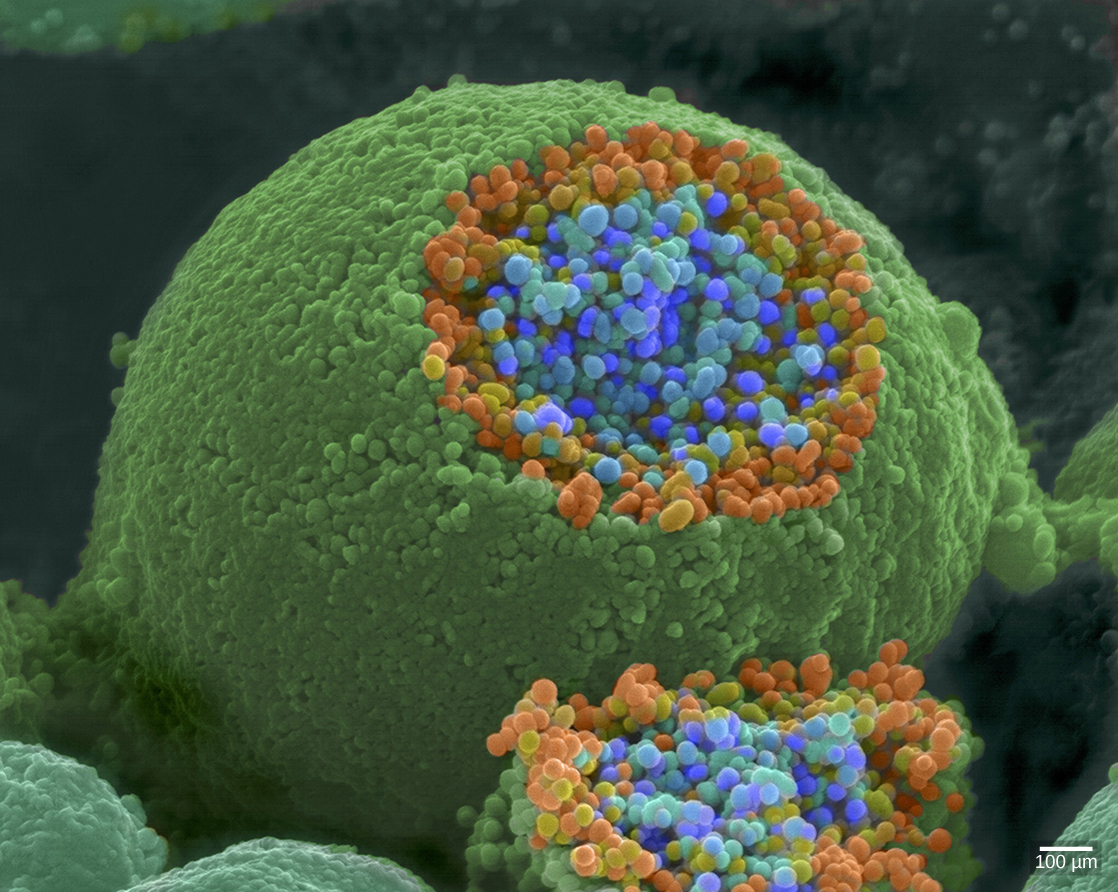
Quando um potencial de ação atinge o terminal do axônio, ele despolariza a membrana e abre canais de Na + dependentes de voltagem. Os íons Na + entram na célula, despolarizando ainda mais a membrana pré-sináptica. Essa despolarização faz com que canais de Ca 2+ dependentes de voltagem se abram. Os íons de cálcio que entram na célula iniciam uma cascata de sinalização que faz com que pequenas vesículas ligadas à membrana, chamadas vesículas sinápticas, contendo moléculas de neurotransmissores se fundam com a membrana pré-sináptica. As vesículas sinápticas são mostradas na Figura\(\PageIndex{6}\), que é uma imagem de um microscópio eletrônico de varredura.
A fusão de uma vesícula com a membrana pré-sináptica faz com que o neurotransmissor seja liberado na fenda sináptica, o espaço extracelular entre as membranas pré-sináptica e pós-sináptica, conforme ilustrado na Figura\(\PageIndex{7}\). O neurotransmissor se difunde pela fenda sináptica e se liga às proteínas receptoras na membrana pós-sináptica.
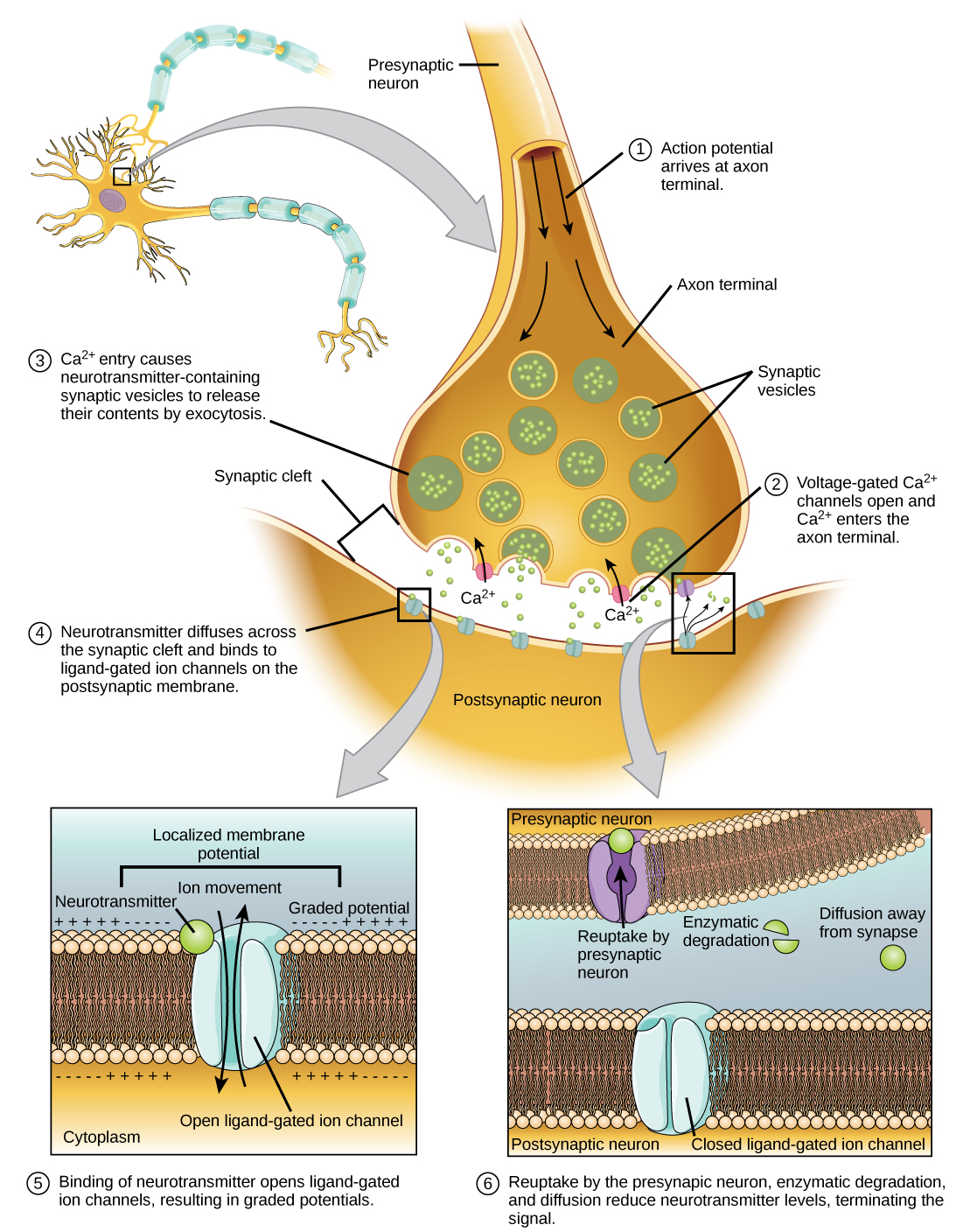
A ligação de um neurotransmissor específico faz com que canais iônicos específicos, neste caso canais dependentes de ligantes, na membrana pós-sináptica se abram. Os neurotransmissores podem ter efeitos excitatórios ou inibitórios na membrana pós-sináptica, conforme detalhado na tabela abaixo. Por exemplo, quando a acetilcolina é liberada na sinapse entre um nervo e um músculo (chamada de junção neuromuscular) por um neurônio pré-sináptico, ela faz com que os canais de Na+ pós-sinápticos se abram. Na + entra na célula pós-sináptica e faz com que a membrana pós-sináptica se despolarize. Essa despolarização é chamada de potencial pós-sináptico excitatório (EPSP) e torna o neurônio pós-sináptico mais propenso a disparar um potencial de ação. A liberação de neurotransmissores nas sinapses inibitórias causa potenciais pós-sinápticos inibitórios (IPSPs), uma hiperpolarização da membrana pré-sináptica. Por exemplo, quando o neurotransmissor GABA (ácido gama-aminobutírico) é liberado de um neurônio pré-sináptico, ele se liga e abre os canais de Cl. Os íons Cl entram na célula e hiperpolarizam a membrana, tornando o neurônio menos propenso a disparar um potencial de ação.
Uma vez que a neurotransmissão tenha ocorrido, o neurotransmissor deve ser removido da fenda sináptica para que a membrana pós-sináptica possa “reiniciar” e estar pronta para receber outro sinal. Isso pode ser feito de três maneiras: o neurotransmissor pode se difundir para longe da fenda sináptica, pode ser degradado por enzimas na fenda sináptica ou pode ser reciclado (às vezes chamado de recaptação) pelo neurônio pré-sináptico. Vários medicamentos atuam nessa etapa da neurotransmissão. Por exemplo, alguns medicamentos administrados a pacientes com Alzheimer atuam inibindo a acetilcolinesterase, a enzima que degrada a acetilcolina. Essa inibição da enzima aumenta essencialmente a neurotransmissão nas sinapses que liberam acetilcolina. Uma vez liberada, a acetilcolina permanece na fenda e pode se ligar e se desligar continuamente aos receptores pós-sinápticos.
| Neurotransmissor | Exemplo | Localização |
|---|---|---|
| Acetilcolina | — | CNS e/ou PNS |
| Amina biogênica | Dopamina, serotonina, norepinefrina | CNS e/ou PNS |
| Aminoácido | Glicina, glutamato, aspartato, ácido gama-aminobutírico | CNS |
| Neuropeptídeo | Substância P, endorfinas | CNS e/ou PNS |
Sinapse elétrica
Embora as sinapses elétricas sejam menos numerosas do que as sinapses químicas, elas são encontradas em todos os sistemas nervosos e desempenham papéis importantes e únicos. O modo de neurotransmissão nas sinapses elétricas é bem diferente daquele nas sinapses químicas. Em uma sinapse elétrica, as membranas pré-sináptica e pós-sináptica estão muito próximas e, na verdade, estão fisicamente conectadas por proteínas do canal, formando junções lacunas. As junções entre lacunas permitem que a corrente passe diretamente de uma célula para a próxima. Além dos íons que transportam essa corrente, outras moléculas, como o ATP, podem se difundir pelos poros da junção de grande lacuna.
Existem diferenças importantes entre sinapses químicas e elétricas. Como as sinapses químicas dependem da liberação de moléculas de neurotransmissores das vesículas sinápticas para transmitir seu sinal, há um atraso de aproximadamente um milissegundo entre o momento em que o potencial axônico atinge o terminal pré-sináptico e quando o neurotransmissor leva à abertura dos canais iônicos pós-sinápticos. . Além disso, essa sinalização é unidirecional. A sinapses elétricas, por outro lado, é virtualmente instantânea (o que é importante para as sinapses envolvidas nos reflexos principais), e algumas sinapses elétricas são bidirecionais. As sinapses elétricas também são mais confiáveis, pois têm menos probabilidade de serem bloqueadas e são importantes para sincronizar a atividade elétrica de um grupo de neurônios. Por exemplo, acredita-se que as sinapses elétricas no tálamo regulem o sono de ondas lentas, e a interrupção dessas sinapses pode causar convulsões.
Soma do sinal
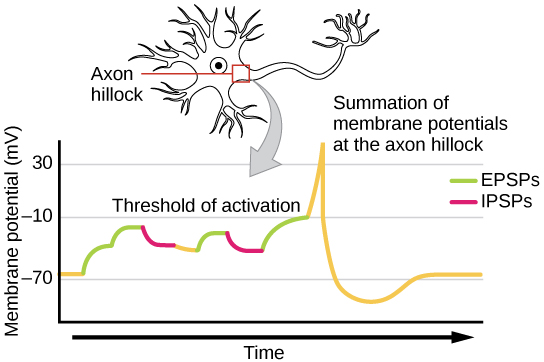
Às vezes, um único EPSP é forte o suficiente para induzir um potencial de ação no neurônio pós-sináptico, mas muitas vezes várias entradas pré-sinápticas devem criar EPSPs ao mesmo tempo para que o neurônio pós-sináptico seja suficientemente despolarizado para disparar um potencial de ação. Esse processo é chamado de soma e ocorre na colina do axônio, conforme ilustrado na Figura\(\PageIndex{8}\). Além disso, um neurônio geralmente tem entradas de muitos neurônios pré-sinápticos - alguns excitatórios e outros inibitórios - então os IPSPs podem cancelar os EPSPs e vice-versa. É a mudança líquida na tensão da membrana pós-sináptica que determina se a célula pós-sináptica atingiu o limite de excitação necessário para disparar um potencial de ação. Juntos, a soma sináptica e o limite de excitação atuam como um filtro para que o “ruído” aleatório no sistema não seja transmitido como informação importante.
Conexão diária: interface cérebro-computador
A esclerose lateral amiotrófica (ELA, também chamada de Doença de Lou Gehrig) é uma doença neurológica caracterizada pela degeneração dos neurônios motores que controlam os movimentos voluntários. A doença começa com enfraquecimento muscular e falta de coordenação e acaba destruindo os neurônios que controlam a fala, a respiração e a deglutição; no final, a doença pode levar à paralisia. Nesse ponto, os pacientes precisam da ajuda das máquinas para poderem respirar e se comunicar. Várias tecnologias especiais foram desenvolvidas para permitir que pacientes “presos” se comuniquem com o resto do mundo. Uma tecnologia, por exemplo, permite que os pacientes digitem frases sacudindo a bochecha. Essas frases podem então ser lidas em voz alta por um computador.
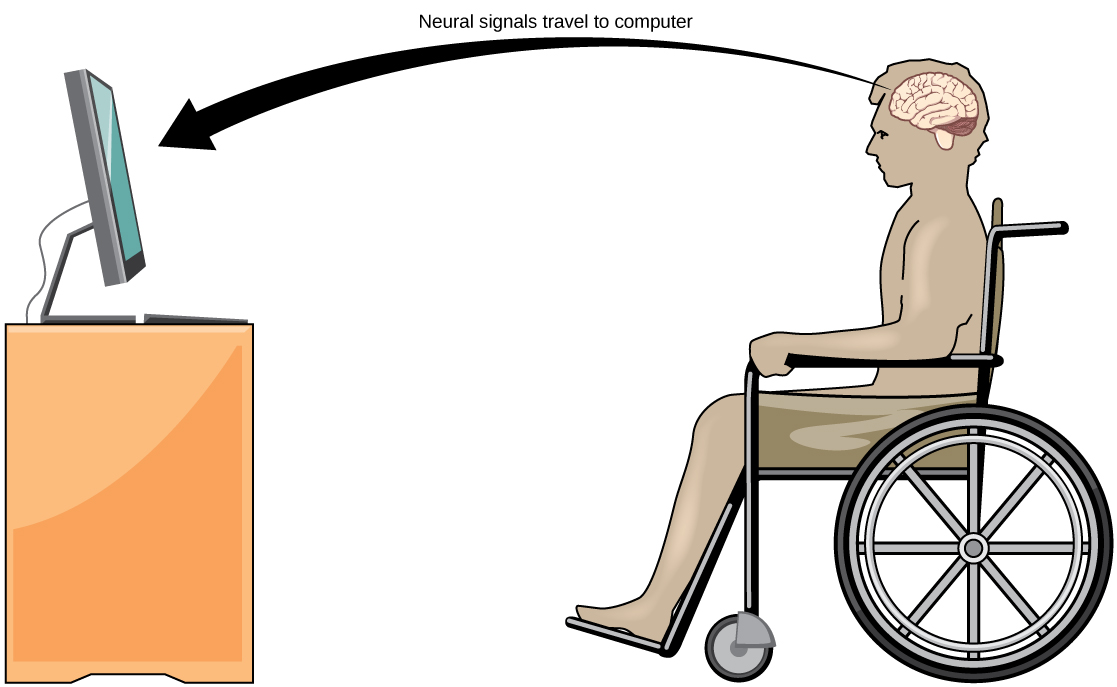
Uma linha de pesquisa relativamente nova para ajudar pacientes paralisados, incluindo aqueles com ELA, a se comunicar e manter um grau de autossuficiência é chamada de tecnologia de interface cérebro-computador (BCI) e é ilustrada na Figura\(\PageIndex{9}\). Essa tecnologia parece algo saído da ficção científica: ela permite que pacientes paralisados controlem um computador usando apenas seus pensamentos. Existem várias formas de BCI. Algumas formas usam gravações de EEG de eletrodos colados no crânio. Essas gravações contêm informações de grandes populações de neurônios que podem ser decodificadas por um computador. Outras formas de BCI requerem a implantação de uma série de eletrodos menores que um selo postal na área do braço e da mão do córtex motor. Essa forma de BCI, embora mais invasiva, é muito poderosa, pois cada eletrodo pode registrar potenciais de ação reais de um ou mais neurônios. Esses sinais são então enviados para um computador, que foi treinado para decodificar o sinal e transmiti-lo a uma ferramenta, como um cursor na tela do computador. Isso significa que um paciente com ELA pode usar o e-mail, ler a Internet e se comunicar com outras pessoas pensando em mover a mão ou o braço (mesmo que o paciente paralisado não consiga fazer esse movimento corporal). Avanços recentes permitiram que uma paciente paralisada e trancada que sofreu um derrame há 15 anos controlasse um braço robótico e até mesmo se alimentasse com café usando a tecnologia BCI.
Apesar dos incríveis avanços na tecnologia BCI, ela também tem limitações. A tecnologia pode exigir muitas horas de treinamento e longos períodos de concentração intensa para o paciente; também pode exigir cirurgia cerebral para implantar os dispositivos.
Link para o aprendizado
Assista a este vídeo em que uma mulher paralisada usa um braço robótico controlado pelo cérebro para levar uma bebida à boca, entre outras imagens da tecnologia de interface cérebro-computador em ação.
Plasticidade sináptica
As sinapses não são estruturas estáticas. Eles podem ser enfraquecidos ou fortalecidos. Eles podem ser quebrados e novas sinapses podem ser criadas. A plasticidade sináptica permite essas mudanças, todas necessárias para o funcionamento do sistema nervoso. De fato, a plasticidade sináptica é a base do aprendizado e da memória. Dois processos em particular, a potencialização de longo prazo (LTP) e a depressão de longo prazo (LTD) são formas importantes de plasticidade sináptica que ocorrem nas sinapses no hipocampo, uma região do cérebro envolvida no armazenamento de memórias.
Potenciação de longo prazo (LTP)
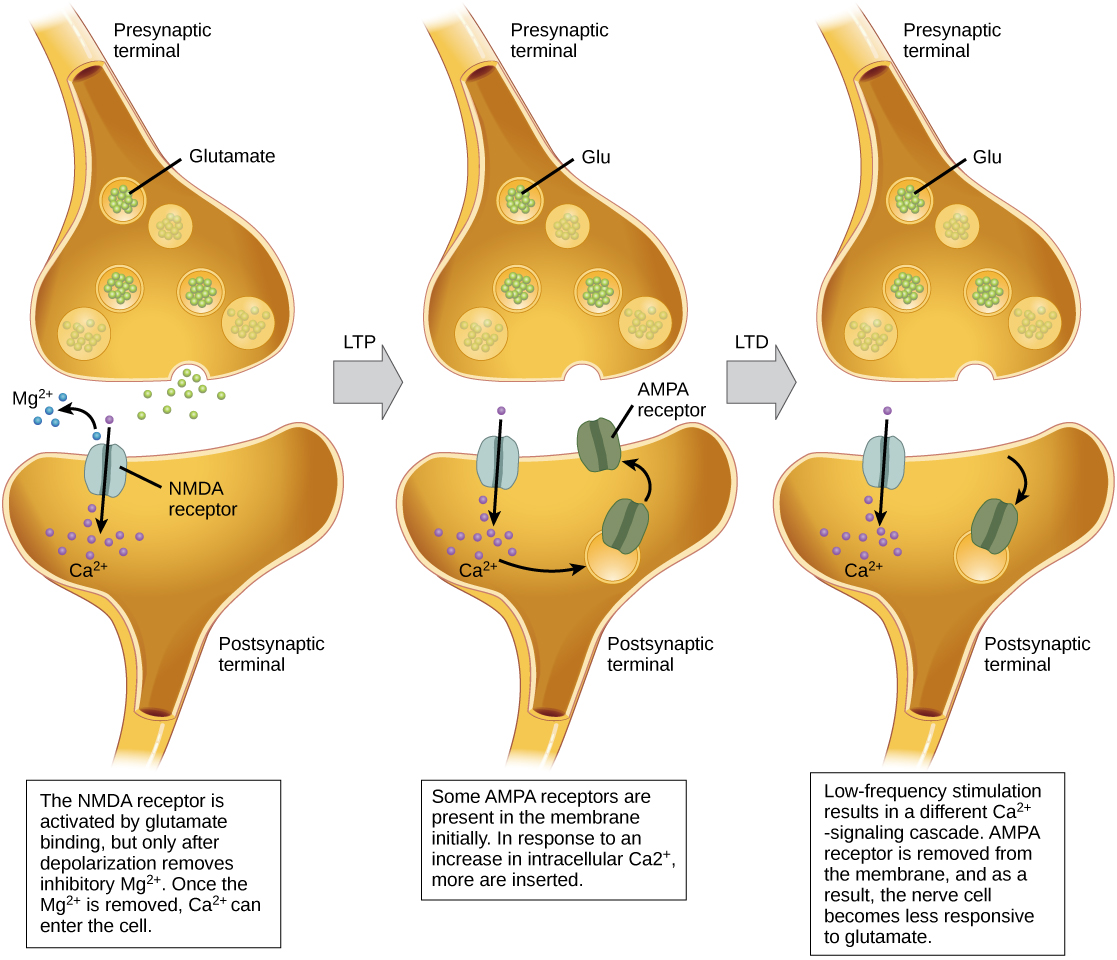
A potenciação de longo prazo (LTP) é um fortalecimento persistente de uma conexão sináptica. O LTP é baseado no princípio Hebbian: células que disparam juntas se conectam. Existem vários mecanismos, nenhum totalmente compreendido, por trás do fortalecimento sináptico observado com o LTP. Um mecanismo conhecido envolve um tipo de receptor de glutamato pós-sináptico, chamado receptores NMDA (N-metil-D-aspartato), mostrado na Figura\(\PageIndex{10}\). Esses receptores são normalmente bloqueados por íons de magnésio; no entanto, quando o neurônio pós-sináptico é despolarizado por várias entradas pré-sinápticas em rápida sucessão (seja de um neurônio ou de vários neurônios), os íons de magnésio são expulsos, permitindo que os íons Ca passem para a célula pós-sináptica. Em seguida, os íons Ca 2+ que entram na célula iniciam uma cascata de sinalização que faz com que um tipo diferente de receptor de glutamato, chamado de receptores AMPA (ácido α-amino-3-hidroxi-5-metil-4-isoxazolepropiônico), seja inserido na membrana pós-sináptica, uma vez que os receptores AMPA ativados permitem a entrada de íons positivos a célula. Portanto, da próxima vez que o glutamato for liberado da membrana pré-sináptica, ele terá um efeito excitatório maior (EPSP) na célula pós-sináptica, pois a ligação do glutamato a esses receptores AMPA permitirá que mais íons positivos entrem na célula. A inserção de receptores AMPA adicionais fortalece a sinapse e significa que o neurônio pós-sináptico tem maior probabilidade de disparar em resposta à liberação do neurotransmissor pré-sináptico. Algumas drogas de abuso cooptam a via LTP, e esse fortalecimento sináptico pode levar ao vício.
Depressão de longo prazo (LTD)
A depressão de longo prazo (LTD) é essencialmente o inverso da LTP: é um enfraquecimento de longo prazo de uma conexão sináptica. Um mecanismo conhecido por causar LTD também envolve receptores AMPA. Nessa situação, o cálcio que entra pelos receptores NMDA inicia uma cascata de sinalização diferente, que resulta na remoção dos receptores AMPA da membrana pós-sináptica, conforme ilustrado na Figura\(\PageIndex{10}\). A diminuição dos receptores de AMPA na membrana torna o neurônio pós-sináptico menos responsivo ao glutamato liberado pelo neurônio pré-sináptico. Embora possa parecer contra-intuitivo, o LTD pode ser tão importante para o aprendizado e a memória quanto o LTP. O enfraquecimento e a poda de sinapses não utilizadas permitem que conexões sem importância sejam perdidas e tornam as sinapses submetidas ao LTP muito mais fortes em comparação.
Resumo
Os neurônios têm membranas carregadas porque existem diferentes concentrações de íons dentro e fora da célula. Os canais iônicos dependentes de voltagem controlam o movimento dos íons para dentro e para fora de um neurônio. Quando uma membrana neuronal é despolarizada até pelo menos o limiar de excitação, um potencial de ação é acionado. O potencial de ação é então propagado ao longo de um axônio mielinizado até os terminais do axônio. Em uma sinapse química, o potencial de ação causa a liberação de moléculas de neurotransmissores na fenda sináptica. Por meio da ligação aos receptores pós-sinápticos, o neurotransmissor pode causar potenciais pós-sinápticos excitatórios ou inibitórios ao despolarizar ou hiperpolarizar, respectivamente, a membrana pós-sináptica. Nas sinapses elétricas, o potencial de ação é comunicado diretamente à célula pós-sináptica por meio de junções gap - proteínas de grandes canais que conectam as membranas pré e pós-sinápticas. As sinapses não são estruturas estáticas e podem ser fortalecidas e enfraquecidas. Dois mecanismos de plasticidade sináptica são a potencialização a longo prazo e a depressão a longo prazo.
Conexões artísticas
Figura\(\PageIndex{3}\): Os bloqueadores dos canais de potássio, como a amiodarona e a procainamida, usados para tratar a atividade elétrica anormal no coração, chamada de disritmia cardíaca, impedem o movimento do K+ através dos canais K + dependentes da voltagem. Qual parte do potencial de ação você esperaria que os canais de potássio afetassem?
- Resposta
-
Os bloqueadores dos canais de potássio retardam a fase de repolarização, mas não têm efeito na despolarização.
Glossário
- potencial de ação
- mudança momentânea autopropagável no potencial elétrico de uma membrana de neurônio (ou músculo)
- despolarização
- mudança no potencial da membrana para um valor menos negativo
- potencial pós-sináptico excitatório (EPSP)
- despolarização de uma membrana pós-sináptica causada por moléculas neurotransmissoras liberadas de uma célula pré-sináptica
- hiperpolarização
- mudança no potencial da membrana para um valor mais negativo
- potencial inibitório pós-sináptico (IPSP)
- hiperpolarização de uma membrana pós-sináptica causada por moléculas neurotransmissoras liberadas de uma célula pré-sináptica
- depressão de longo prazo (LTD)
- diminuição prolongada no acoplamento sináptico entre uma célula pré e pós-sináptica
- potenciação de longo prazo (LTP)
- aumento prolongado no acoplamento sináptico entre uma célula pré e pós-sináptica
- potencial de membrana
- diferença no potencial elétrico entre o interior e o exterior de uma célula
- período refratário
- período após um potencial de ação quando é mais difícil ou impossível que um potencial de ação seja acionado; causado pela inativação dos canais de sódio e ativação de canais adicionais de potássio da membrana
- condução saltatória
- “salto” de um potencial de ação ao longo de um axônio de um nó de Ranvier para o próximo
- soma
- processo de múltiplas entradas pré-sinápticas criando EPSPs ao mesmo tempo para que o neurônio pós-sináptico seja suficientemente despolarizado para disparar um potencial de ação
- fenda sináptica
- espaço entre as membranas pré-sináptica e pós-sináptica
- vesícula sináptica
- estrutura esférica que contém um neurotransmissor
- limiar de excitação
- nível de despolarização necessário para que um potencial de ação acenda


