8.4: Spin de elétrons
- Page ID
- 183148
Ao final desta seção, você poderá:
- Expresse o estado de um elétron em um átomo de hidrogênio em termos de cinco números quânticos
- Use números quânticos para calcular a magnitude e a direção do spin e do momento magnético de um elétron
- Explicar a estrutura fina e hiperfina do espectro de hidrogênio em termos de interações magnéticas dentro do átomo de hidrogênio
Nesta seção, consideramos os efeitos do spin do elétron. Spin introduz dois números quânticos adicionais ao nosso modelo do átomo de hidrogênio. Ambos foram descobertos observando a estrutura fina dos espectros atômicos. O spin é uma característica fundamental de todas as partículas, não apenas dos elétrons, e é análogo ao giro intrínseco de corpos estendidos em torno de seus próprios eixos, como a rotação diária da Terra.
O spin é quantizado da mesma maneira que o momento angular orbital. Foi descoberto que a magnitude do momento angular de rotação intrínseco\(S\) de um elétron é dada por
\[S = \sqrt{s(s + 1)}\hbar, \nonumber \]
onde\(s\) é definido como o número quântico de spin. Isso é semelhante à quantização de\(L\), exceto que o único valor permitido\(s\) para um elétron é\(s = 1/2\). Diz-se que o elétron é uma “meia partícula de spin”. O número quântico da projeção de spin\(m_s\) está associado aos componentes z do spin, expressos por
\[S_z = m_s\hbar. \label{eq2} \]
Em geral, os números quânticos permitidos são
\[m_s = -s, -s + 1, . . ., 0, . . ., +s - 1, s. \nonumber \]
Para o caso especial de um elétron (\(s = 1/2\)),
\[m_s = -\frac{1}{2} \text{ or } \frac{1}{2}. \nonumber \]
As direções de rotação intrínseca são quantizadas, assim como eram para o momento angular orbital. O\(m_s = -1/2\) estado é chamado de estado “spin-down” e tem um componente z de spin\(s_z = -1/2\), o\(m_s = +1/2\) estado é chamado de estado “spin-up” e tem um componente z de spin,\(s_z = +1/2\). Esses estados são mostrados na Figura\(\PageIndex{1}\).
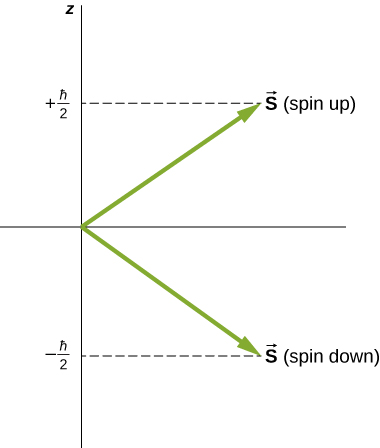
O momento de dipolo magnético intrínseco de um elétron também\(\mu_e\) pode ser expresso em termos do número quântico de spin. Em analogia com o momento angular orbital, a magnitude do momento magnético do elétron é
\[\mu_s = \left(\frac{e}{2m_e}\right)S. \nonumber \]
De acordo com a teoria especial da relatividade, esse valor é baixo por um fator de 2. Assim, na forma vetorial, o momento magnético do spin é
\[\vec{\mu} = \left(\frac{e}{m_e}\right)\vec{S}. \nonumber \]
O componente z do momento magnético é (da Equação\ ref {eq2})
\[\begin{align} \mu_z &= - \left(\frac{e}{m_e}\right) S_z \\[5pt] &= - \left(\frac{e}{m_e}\right) m_s \hbar. \end{align} \nonumber \]
O número quântico da projeção de spin tem apenas dois valores (\(m_s = \pm1/2\)), então o componente z do momento magnético também tem apenas dois valores:
\[\mu_z = \pm \left(\frac{e}{2m_e}\right) = \pm \mu_B\hbar, \nonumber \]
onde\(\mu_B\) está um magneton de Bohr. Um elétron é magnético, então esperamos que o elétron interaja com outros campos magnéticos. Consideramos dois casos especiais: a interação de um elétron livre com um campo magnético externo (não uniforme) e um elétron em um átomo de hidrogênio com um campo magnético produzido pelo momento angular orbital do elétron.
Elétron em um campo externo
O experimento Stern-Gerlach fornece evidências experimentais de que os elétrons têm momento angular de spin. O experimento passa um fluxo de átomos de prata (Ag) através de um campo magnético externo não uniforme. O átomo de Ag tem um momento angular orbital de zero e contém um único elétron não pareado na camada externa. Portanto, o momento angular total do átomo de Ag é inteiramente devido ao spin do elétron externo (\(s = 1/2\)). Devido ao spin do elétron, os átomos de Ag agem como pequenos ímãs à medida que passam pelo campo magnético. Esses “ímãs” têm duas orientações possíveis, que correspondem aos estados de rotação para cima e para baixo do elétron. O campo magnético desvia os átomos de rotação ascendente em uma direção e os átomos giratórios em outra direção. Isso produz duas bandas distintas em uma tela (Figura\(\PageIndex{2}\)).
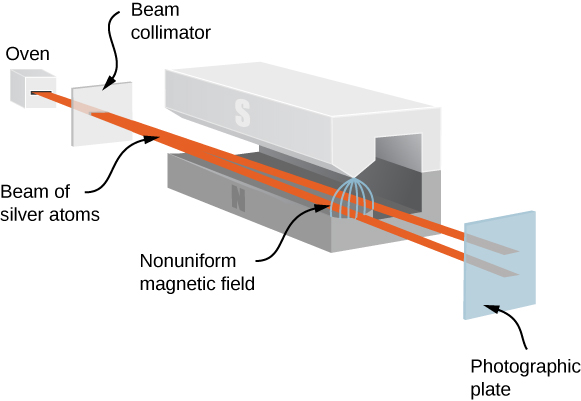
De acordo com as previsões clássicas, o momento angular (e, portanto, o momento magnético) do átomo de Ag pode apontar em qualquer direção, então espera-se, em vez disso, uma mancha contínua na tela. As duas bandas resultantes do experimento Stern-Gerlach fornecem um suporte surpreendente para as ideias da mecânica quântica.
Visite PhET Explorations: Stern-Gerlach Experiment para saber mais sobre o experimento Stern-Gerlach.
Um átomo de hidrogênio no estado fundamental é colocado em um campo magnético externo uniforme (\(B = 1.5 \, T\)). Determine a frequência da radiação produzida em uma transição entre os estados de spin-up e spin-down do elétron.
Estratégia
O número quântico da projeção de spin é\(m_s = \pm 1/2\), então o componente z do momento magnético é
\[\mu_z = \pm \left(\frac{e}{2m_e} \right) = \pm \mu_B \hbar. \nonumber \]
A energia potencial associada à interação entre o momento magnético do elétron e o campo magnético externo é
\[\begin{align*} U &= - \mu_z B \\[5pt] &= \mp \mu_BB. \end{align*} \nonumber \]
A frequência da luz emitida é proporcional à diferença de energia (\(\Delta E\)) entre esses dois estados.
Solução
A diferença de energia entre esses estados é\(\Delta E = 2\mu_BB\), então a frequência da radiação produzida é
\[\begin{align*} f = \dfrac{\Delta E}{h} &= \frac{2\mu_BB}{h} \\[5pt] &= \frac{2\left(5.79 \times \frac{10^{-5} eV}{T}\right)(1.5 \, T)}{4.136 \times 10^{-15} eV \cdot s} \\[5pt] &= 4.2 \times 10^{10} \, \frac{cycles}{s}. \end{align*} \nonumber \]
Significância
O momento magnético do elétron se acopla ao campo magnético externo. A energia desse sistema é diferente se o elétron está alinhado ou não com o próton. A frequência da radiação produzida por uma transição entre esses estados é proporcional à diferença de energia. Se dobrarmos a intensidade do campo magnético, mantendo todas as outras coisas constantes, a frequência da radiação dobra e seu comprimento de onda é reduzido pela metade.
Se o experimento Stern-Gerlach produzisse quatro bandas distintas em vez de duas, o que poderia ser concluído sobre o número quântico de spin da partícula carregada?
- Responda
-
\(s = 3/2 <\)
Acoplamento Spin-Orbit (estrutura fina)
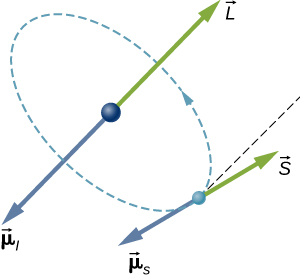
Em um átomo de hidrogênio, o momento magnético do elétron pode interagir com o campo magnético produzido pelo momento angular orbital do elétron, um fenômeno chamado acoplamento spin-órbita. Os vetores de momento angular orbital (\(\vec{L}\)), momento magnético orbital (\(\vec{\mu}\)), momento angular de spin (\(\vec{S}\)) e momento magnético de spin (\(\vec{\mu}_s\)) são mostrados juntos na Figura\(\PageIndex{3}\).
Assim como os níveis de energia de um átomo de hidrogênio podem ser divididos por um campo magnético externo, o mesmo acontece com os níveis de energia de um átomo de hidrogênio divididos pelos campos magnéticos internos do átomo. Se o momento magnético do elétron e o momento magnético orbital do elétron forem antiparalelos, a energia potencial da interação magnética é relativamente alta, mas quando esses momentos são paralelos, a energia potencial é relativamente pequena. A transição de cada um desses dois estados para um nível de energia mais baixo resulta na emissão de um fóton de frequência ligeiramente diferente. Ou seja, o acoplamento spin-orbita “divide” a linha espectral esperada de um elétron sem spin. A estrutura fina do espectro do hidrogênio é explicada pelo acoplamento spin-órbita.
Acoplamento de Spin Eletrônico e Spin Nuclear (Estrutura Hiperfina)
Assim como um elétron, um próton tem spin 1/2 e tem um momento magnético. (De acordo com a teoria nuclear, esse momento é devido ao movimento orbital dos quarks dentro do próton.) A estrutura hiperfina do espectro de hidrogênio é explicada pela interação entre o momento magnético do próton e o momento magnético do elétron, uma interação conhecida como acoplamento spin-spin. A energia do sistema elétron-próton é diferente dependendo se os momentos estão ou não alinhados. As transições entre esses estados (transições spin-flip) resultam na emissão de um fóton com comprimento de onda de\(\lambda = 21\) cm (na faixa do rádio). A linha de 21 cm na espectroscopia atômica é uma “impressão digital” do gás hidrogênio. Os astrônomos exploram essa linha espectral para mapear os braços espirais das galáxias, que são compostas principalmente de hidrogênio (Figura\(\PageIndex{4}\)).

Uma especificação completa do estado de um elétron em um átomo de hidrogênio requer cinco números quânticos: n, l, m, s\(m_s\) e. Os nomes, símbolos e valores permitidos desses números quânticos estão resumidos na Tabela\(\PageIndex{4}\).
| Nome | Símbolo | Valores permitidos |
|---|---|---|
| Número quântico principal | n | 1, 2, 3,... |
| Momento angular | l | 0, 1, 2,... n — 1 |
| Projeção de momento angular | m | \(0, \pm 1, \pm 2, . . . \pm l\) |
| Girar | s | 1/2 (elétrons) |
| Projeção de rotação | \(m_s\) | \(- 1/2, \, +1/2\) |
Observe que os números quânticos intrínsecos introduzidos nesta seção (\(s\)e\(m_s\)) são válidos para muitas partículas, não apenas para elétrons. Por exemplo, quarks dentro de um núcleo atômico também são meias-partículas de spin. Como veremos mais adiante, os números quânticos ajudam a classificar as partículas subatômicas e a entrar em modelos científicos que tentam explicar como o universo funciona.


