22.4 : Mycoses respiratoires
- Page ID
- 187752
Objectifs d'apprentissage
- Identifier les champignons les plus courants pouvant provoquer des infections des voies respiratoires
- Comparez les principales caractéristiques de maladies fongiques spécifiques des voies respiratoires
Les agents pathogènes fongiques sont omniprésents dans l'environnement. Des études sérologiques ont démontré que la plupart des personnes ont été exposées à des agents pathogènes respiratoires fongiques au cours de leur vie. Pourtant, les infections symptomatiques causées par ces microbes sont rares chez les personnes en bonne santé. Cela démontre l'efficacité des défenses de notre système respiratoire. Dans cette section, nous examinerons certains des champignons qui peuvent provoquer des infections respiratoires.
Histoplasmose
L'histoplasmose est une maladie fongique du système respiratoire qui survient le plus souvent dans la vallée du Mississippi aux États-Unis et dans certaines parties de l'Amérique centrale et du Sud, de l'Afrique, de l'Asie et de l'Australie. L'agent causal, Histoplasma capsulatum, est un champignon dimorphe. Ce microbe se développe sous forme de moisissure filamenteuse dans l'environnement, mais se présente sous forme de levure bourgeonnante lors d'infections humaines. Le principal réservoir de cet agent pathogène est le sol, en particulier dans les endroits riches en excréments de chauves-souris ou d'oiseaux.
L'histoplasmose est acquise par inhalation de spores microconidiales présentes dans l'air ; cette maladie ne se transmet pas d'homme à humain. L'incidence de l'exposition à l'histoplasmose est élevée dans les zones endémiques, 60 à 90 % de la population présentant des anticorps anti-histoplasmose, selon la localité1 ; cependant, relativement peu de personnes exposées au champignon présentent réellement des symptômes. Les personnes les plus susceptibles d'être touchées sont les très jeunes enfants, les personnes âgées et les personnes immunodéprimées.
À bien des égards, l'évolution de cette maladie est similaire à celle de la tuberculose. Après inhalation, les spores pénètrent dans les poumons et sont phagocytées par des macrophages alvéolaires. Les cellules fongiques survivent ensuite et se multiplient au sein de ces phagocytes (voir Figure 5.3.2). Les infections focales provoquent la formation de lésions granulomateuses, qui peuvent entraîner des calcifications ressemblant aux complexes de Ghon de la tuberculose, même dans les cas asymptomatiques. Tout comme la tuberculose, l'histoplasmose peut devenir chronique et une réactivation peut se produire, ainsi qu'une dissémination vers d'autres parties du corps (par exemple, le foie ou la rate).
Les signes et symptômes de l'histoplasmose pulmonaire incluent de la fièvre, des maux de tête et une faiblesse accompagnée d'une gêne thoracique. Le diagnostic initial repose souvent sur des radiographies pulmonaires et des cultures cultivées sur des milieux sélectifs fongiques tels que la gélose au dextrose de Sabouraud. La coloration par anticorps par fluorescence directe et la coloration Giemsa peuvent également être utilisées pour détecter ce pathogène. De plus, des tests sérologiques, y compris un test de fixation du complément et de sensibilité à l'histoplasmine, peuvent être utilisés pour confirmer le diagnostic. Dans la plupart des cas, ces infections sont spontanément résolutives et aucun traitement antifongique n'est nécessaire. Toutefois, en cas de maladie disséminée, les agents antifongiques amphotéricine B et kétoconazole sont efficaces ; l'itraconazole peut être efficace chez les patients immunodéprimés, chez lesquels la maladie peut être plus grave.
Exercice\(\PageIndex{1}\)
- Dans quels environnements une personne est-elle plus susceptible d'être infectée par l'histoplasmose ?
- Identifiez au moins deux similitudes entre l'histoplasmose et la tuberculose.
Coccidioïdomycose
L'infection par le champignon dimorphe Coccidioides immitis provoque une coccidioïdomycose. Comme le microbe est endémique dans la vallée de San Joaquin en Californie, la maladie est parfois appelée fièvre de la vallée. Une espèce apparentée qui cause des infections similaires se trouve dans les régions semi-arides et arides du sud-ouest des États-Unis, du Mexique et de l'Amérique centrale et du Sud. 2
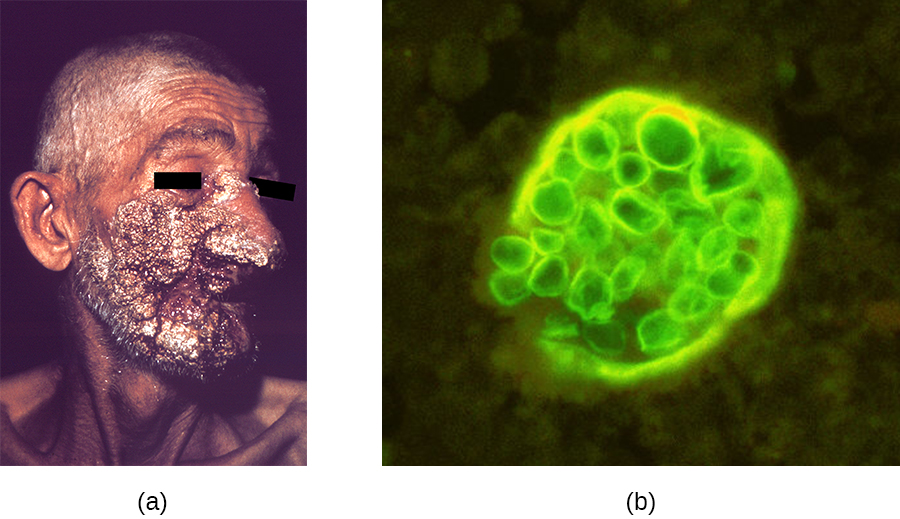
Comme l'histoplasmose, la coccidioïdomycose est acquise par inhalation de spores fongiques, en l'occurrence des arthrospores formées par fragmentation des hyphes. Une fois dans le corps, le champignon se différencie en sphérules remplies d'endospores. La plupart des infections à C. immitis sont asymptomatiques et spontanément résolutives. Cependant, l'infection peut être très grave chez les patients immunodéprimés. Les endospores peuvent être transportées dans le sang, disséminant l'infection et entraînant la formation de lésions granulomateuses sur le visage et le nez (Figure\(\PageIndex{1}\)). Dans les cas graves, d'autres organes importants peuvent être infectés, entraînant de graves complications telles qu'une méningite mortelle.
La coccidioïdomycose peut être diagnostiquée en cultivant des échantillons cliniques. C. immitis pousse facilement sur des milieux fongiques de laboratoire, tels que la gélose au dextrose de Sabouraud, à 35 °C (95 °F). La culture du champignon est cependant assez dangereuse. C. immitis est l'un des agents pathogènes fongiques les plus infectieux connus et est capable de provoquer des infections contractées en laboratoire. En effet, jusqu'en 2012, cet organisme était considéré comme un « agent sélectif » du bioterrorisme et classé comme microbe BSL-3. Les tests sérologiques pour la production d'anticorps sont plus souvent utilisés pour le diagnostic. Bien que les cas bénins ne nécessitent généralement aucune intervention, les infections disséminées peuvent être traitées par des antifongiques intraveineux tels que l'amphotéricine B.
Orientation clinique : résolution
Les tests RIDT négatifs de John n'excluent pas la grippe, car les résultats faussement négatifs sont courants, mais l'infection à Legionella doit tout de même être traitée par antibiothérapie et constitue la maladie la plus grave. Le pronostic de John est bon, à condition que le médecin trouve une antibiothérapie à laquelle l'infection réagit.
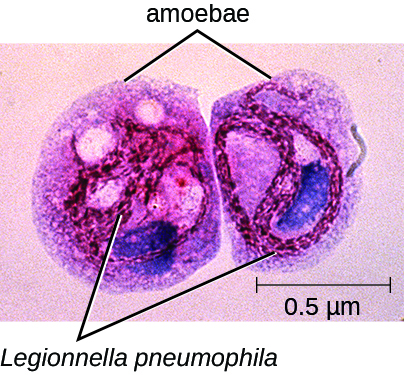
Pendant que John suivait un traitement, trois des employés du magasin de bricolage se sont également présentés à la clinique avec des symptômes très similaires. Tous trois étaient âgés de plus de 55 ans et présentaient de l'antigène Legionella dans leurs urines ; L. pneumophila a également été isolé dans leurs expectorations. Une équipe du service de santé a été envoyée au magasin de bricolage pour identifier la source probable de ces infections. Leur enquête a révélé qu'environ 3 semaines plus tôt, le système de climatisation du magasin, situé à l'endroit où les employés déjeunaient, faisait l'objet de travaux de maintenance. L. pneumophila a été isolé à partir des serpentins de refroidissement du système de climatisation et L. pneumophila intracellulaire a également été observé dans des amibes dans des échantillons d'eau condensée provenant des serpentins de refroidissement (Figure\(\PageIndex{2}\)). Les amibes protègent la bactérie Legionella et sont connues pour améliorer leur pathogénicité. 3
À la suite des infections, le magasin a ordonné un nettoyage complet du système de climatisation et a mis en place un programme d'entretien régulier pour empêcher la croissance de biofilms dans la tour de refroidissement. Ils ont également passé en revue les pratiques de leurs autres installations.
Après un mois de repos à la maison, John s'est suffisamment rétabli de son infection pour retourner au travail, tout comme les trois autres employés du magasin. Cependant, John a souffert de léthargie et de douleurs articulaires pendant plus d'un an après son traitement.
Blastomycose
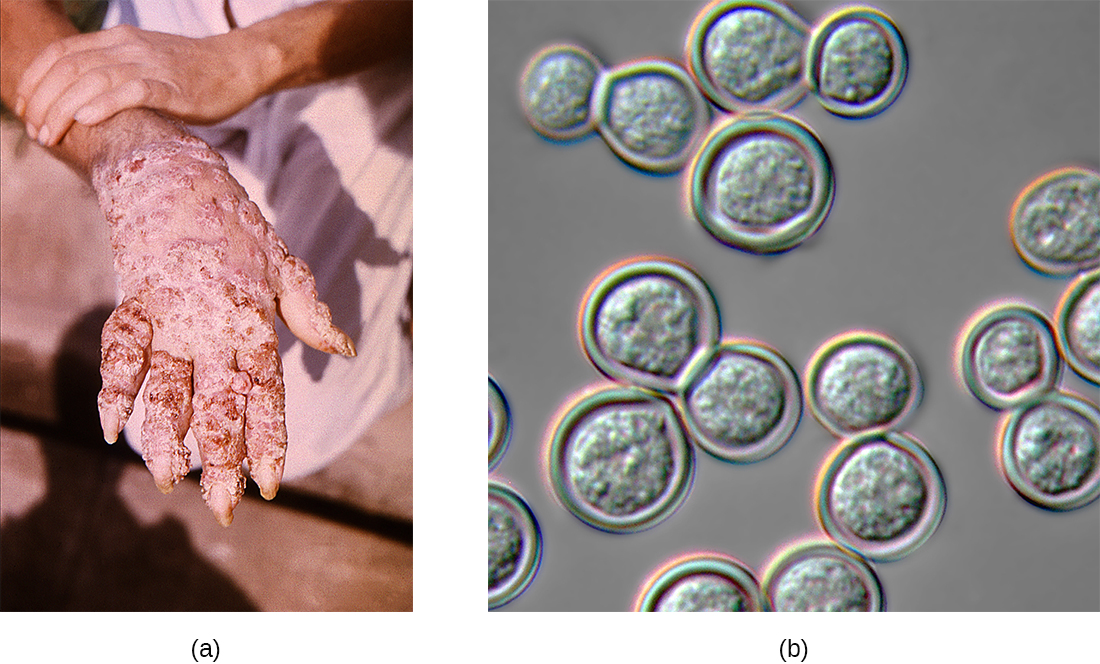
La blastomycose est une maladie rare causée par un autre champignon dimorphe, le Blastomyces dermatitidis. Comme Histoplasma et Coccidioides, Blastomyces utilise le sol comme réservoir et les spores fongiques peuvent être inhalées à partir du sol perturbé. La forme pulmonaire de blastomycose provoque généralement de légers symptômes semblables à ceux de la grippe et se résorbe spontanément. Elle peut toutefois se disséminer chez les personnes immunodéprimées, entraînant une maladie cutanée chronique accompagnée de lésions sous-cutanées du visage et des mains (Figure\(\PageIndex{3}\)). Ces lésions cutanées finissent par devenir croustillantes et décolorées et peuvent entraîner des cicatrices déformantes. La blastomycose systémique est rare, mais si elle n'est pas traitée, elle est toujours fatale.
Le diagnostic préliminaire de la blastomycose pulmonaire peut être posé en observant les formes caractéristiques des levures bourgeonnantes dans les échantillons de crachats. Des tests antigéniques urinaires disponibles dans le commerce sont désormais également disponibles. Les tests de confirmation supplémentaires incluent des tests sérologiques tels que les tests d'immunodiffusion ou l'EIA. La plupart des cas de blastomycose répondent bien aux traitements à l'amphotéricine ou au kétoconazole.
Mucormycose
Divers champignons de l'ordre des Mucorales provoquent la mucormycose, une maladie fongique rare. Il s'agit notamment des moules à pain, tels que Rhizopus et Mucor ; les espèces les plus fréquemment associées sont Rhizopus arrhizus (oryzes) (voir Figure 5.3.4). Ces champignons peuvent coloniser de nombreux tissus différents chez les patients immunodéprimés, mais ils infectent souvent la peau, les sinus ou les poumons.
Bien que la plupart des personnes soient régulièrement exposées aux agents responsables de la mucormycose, les infections chez les personnes en bonne santé sont rares. L'exposition aux spores provenant de l'environnement se fait généralement par inhalation, mais les spores peuvent également infecter la peau par le biais d'une plaie ou du tractus gastro-intestinal si elles sont ingérées. La mucormycose respiratoire touche principalement les personnes immunodéprimées, telles que les patients atteints d'un cancer ou ceux qui ont subi une greffe. 4
Une fois les spores inhalées, les champignons se développent en étendant les hyphes dans les tissus de l'hôte. Des infections peuvent survenir dans les voies respiratoires supérieures et inférieures. La mucormycose rhinocérébrale est une infection des sinus et du cerveau ; les symptômes incluent des maux de tête, de la fièvre, un gonflement du visage, une congestion et une nécrose tissulaire provoquant des lésions noires dans la cavité buccale. La mucormycose pulmonaire est une infection des poumons dont les symptômes incluent de la fièvre, de la toux, des douleurs thoraciques et un essoufflement. Dans les cas graves, les infections peuvent se disséminer et toucher le système nerveux central, entraînant le coma et la mort. 5
Le diagnostic de la mucormycose peut s'avérer difficile. À l'heure actuelle, aucun test sérologique ou basé sur la PCR n'est disponible pour identifier ces infections. Les échantillons de biopsie tissulaire doivent être examinés pour détecter la présence de pathogènes fongiques. Les agents responsables sont cependant souvent difficiles à distinguer des autres champignons filamenteux. Les infections sont généralement traitées par l'administration intraveineuse d'amphotéricine B, et les infections superficielles sont éliminées par un débridement chirurgical. Les patients étant souvent immunodéprimés, des infections secondaires virales et bactériennes se développent fréquemment. Les taux de mortalité varient en fonction du site de l'infection, du champignon responsable et d'autres facteurs, mais une étude récente a révélé un taux de mortalité global de 54 %. 6
Exercice\(\PageIndex{2}\)
- Comparez les modes de transmission de la coccidioïdomycose, de la blastomycose et de la mucormycose.
- Quelles sont, en général, les plus graves : les formes pulmonaires ou disséminées de ces infections ?
Aspergillose
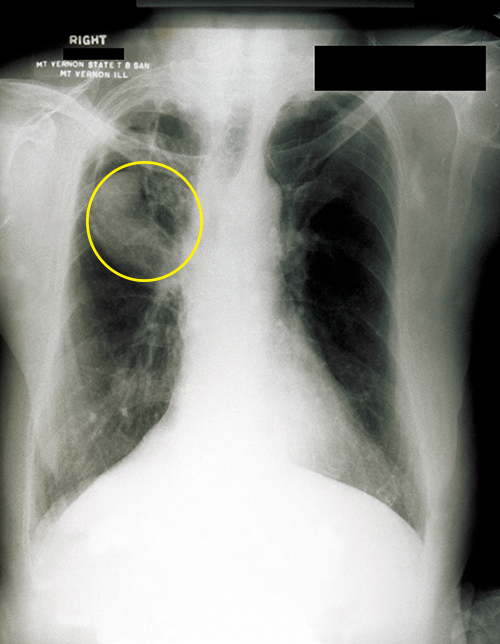
L'aspergillus est un champignon filamenteux courant présent dans les sols et les débris organiques. Presque tout le monde a été exposé à cette moisissure, mais très peu de personnes tombent malades. Toutefois, chez les patients immunodéprimés, l'Aspergillus peut s'installer et provoquer une aspergillose. L'inhalation de spores peut provoquer des réactions allergiques semblables à celles de l'asthme. Les symptômes incluent généralement un essoufflement, une respiration sifflante, une toux, un écoulement nasal et des maux de tête. Des boules fongiques, ou aspergillomes, peuvent se former lorsque des colonies d'hyphes s'accumulent dans les poumons (Figure\(\PageIndex{4}\)). Les hyphes fongiques peuvent envahir les tissus de l'hôte, provoquant une hémorragie pulmonaire et une toux sanglante. Dans les cas graves, la maladie peut évoluer vers une forme disséminée souvent fatale. La mort résulte le plus souvent d'une pneumonie ou d'une hémorragie cérébrale.
Le diagnostic en laboratoire nécessite généralement des radiographies pulmonaires et un examen microscopique d'échantillons de tissus et de liquides respiratoires. Des tests sérologiques sont disponibles pour identifier les antigènes d'Aspergillus. De plus, un test cutané peut être effectué pour déterminer si le patient a été exposé au champignon. Ce test est similaire au test cutané à la tuberculine de Mantoux utilisé pour la tuberculose. L'aspergillose est traitée avec des agents antifongiques intraveineux, notamment l'itraconazole et le voriconazole. Les symptômes allergiques peuvent être gérés à l'aide de corticostéroïdes, car ces médicaments inhibent le système immunitaire et réduisent l'inflammation. Toutefois, dans les infections disséminées, les corticostéroïdes doivent être interrompus pour permettre l'apparition d'une réponse immunitaire protectrice.
Pneumocystis Pneumonie
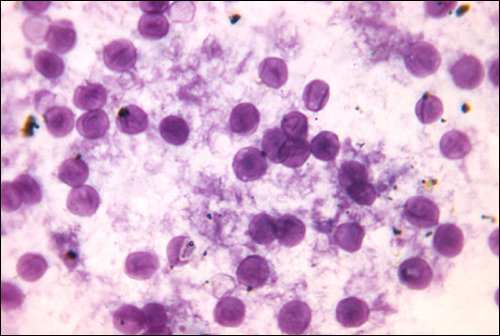
Un type de pneumonie appelé pneumonie à pneumocystis (PCP) est causé par Pneumocystis jirovecii. Autrefois considéré comme un protozoaire, cet organisme s'appelait auparavant P. carinii, mais il a été reclassé en tant que champignon et renommé sur la base d'analyses biochimiques et génétiques. La pneumocystose est l'une des principales causes de pneumonie chez les patients atteints du syndrome d'immunodéficience acquise (SIDA) et peut être observée chez d'autres patients fragilisés et prématurés. L'infection respiratoire entraîne de la fièvre, de la toux et un essoufflement. Le diagnostic de ces infections peut être difficile. L'organisme est généralement identifié par un examen microscopique d'échantillons de tissus et de liquides prélevés dans les poumons (Figure\(\PageIndex{5}\)). Un test basé sur la PCR est disponible pour détecter P. jirovecii chez les patients asymptomatiques atteints du SIDA. Le meilleur traitement pour ces infections est l'association triméthoprime-sulfaméthoxazole (TMP/SMZ). Ces sulfamides ont souvent des effets indésirables, mais leurs avantages l'emportent sur ces risques. Si elles ne sont pas traitées, les infections à PCP sont souvent mortelles.
Cryptococcose
L'infection par la levure encapsulée Cryptococcus neoformans provoque une cryptococcose. Ce champignon est omniprésent dans le sol et peut être isolé des excréments d'oiseaux. Les personnes immunodéprimées sont infectées par inhalation de basidiospores présentes dans les aérosols. L'épaisse capsule polysaccharidique qui entoure ces microbes leur permet d'éviter leur élimination par le macrophage alvéolaire. Les premiers symptômes de l'infection incluent de la fièvre, de la fatigue et une toux sèche. Chez les patients immunodéprimés, les infections pulmonaires se propagent souvent au cerveau. La méningite qui en résulte provoque des maux de tête, une sensibilité à la lumière et de la confusion. Si elles ne sont pas traitées, ces infections sont souvent mortelles.
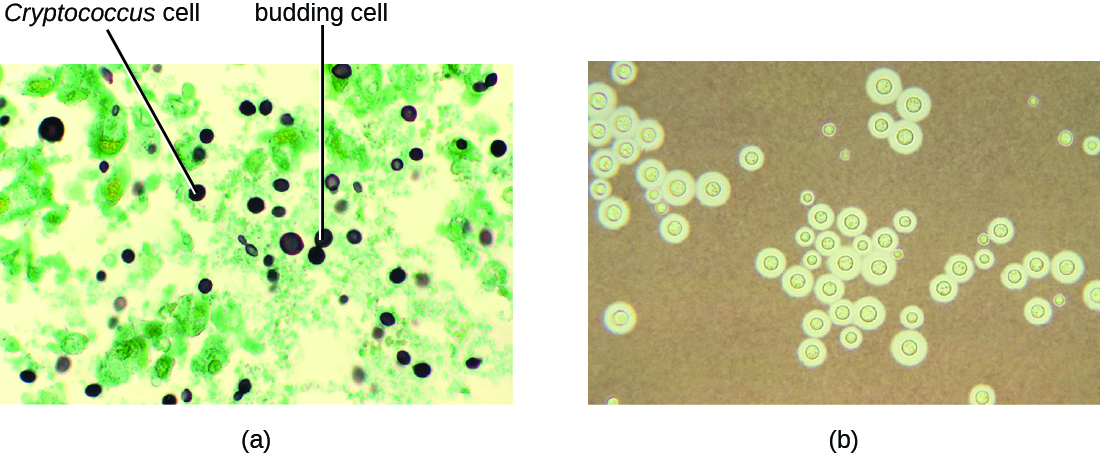
Les infections à cryptocoques sont souvent diagnostiquées sur la base d'un examen microscopique des tissus pulmonaires ou du liquide céphalo-rachidien. Des préparations à base d'encre de Chine (Figure\(\PageIndex{6}\)) peuvent être utilisées pour visualiser les capsules étendues qui entourent les cellules de levure. Des tests sérologiques sont également disponibles pour confirmer le diagnostic. L'amphotéricine B, en association avec la flucytosine, est généralement utilisée pour le traitement initial des infections pulmonaires. L'amphotéricine B est un médicament antifongique à large spectre qui cible les membranes des cellules fongiques. Il peut également avoir un impact négatif sur les cellules hôtes et produire des effets secondaires. C'est pourquoi les cliniciens doivent soigneusement équilibrer les risques et les avantages des traitements chez ces patients. Comme il est difficile d'éradiquer les infections cryptococciques, les patients doivent généralement prendre du fluconazole jusqu'à 6 mois après le traitement par l'amphotéricine B et la flucytosine pour éliminer le champignon. Les infections cryptococciques sont plus fréquentes chez les personnes immunodéprimées, comme celles atteintes du sida. Ces patients ont généralement besoin d'un traitement suppresseur à vie pour contrôler cette infection fongique.
Exercice\(\PageIndex{3}\)
- Quelles sont les populations les plus à risque de développer une pneumonie à pneumocystis ou une cryptococcose ?
- Pourquoi ces infections sont-elles mortelles si elles ne sont pas traitées ?
Maladies fongiques des voies respiratoires
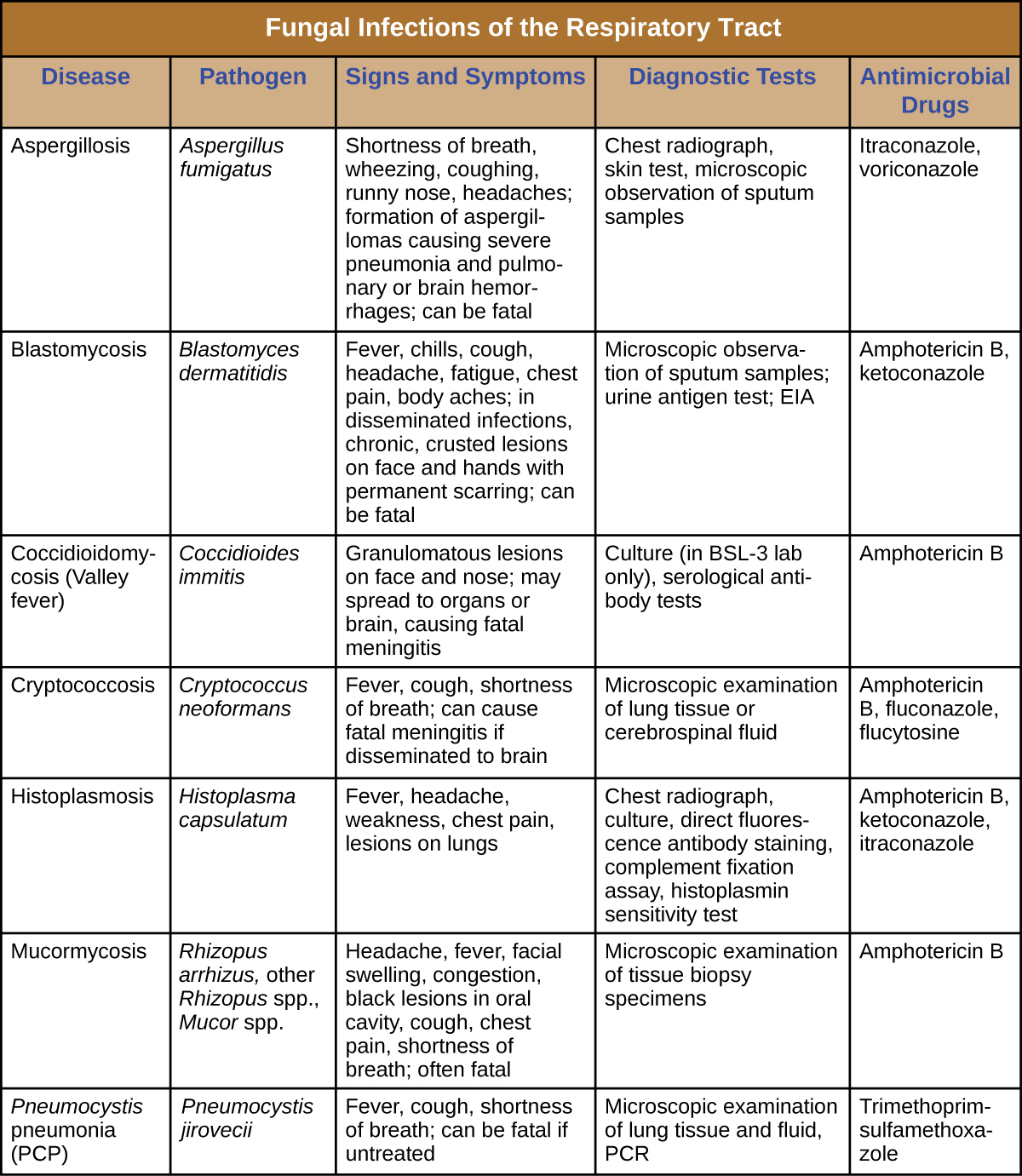
La plupart des mycoses respiratoires sont causées par des champignons qui peuplent l'environnement. Ces infections sont généralement transmises par inhalation de spores fongiques et ne peuvent pas être transmises entre humains. De plus, les personnes en bonne santé ne sont généralement pas sensibles à l'infection, même lorsqu'elles y sont exposées ; les champignons sont suffisamment virulents pour établir l'infection chez les patients atteints du VIH, du sida ou d'une autre maladie qui compromet les défenses immunitaires. La figure\(\PageIndex{7}\) résume les caractéristiques des mycoses respiratoires importantes.
Concepts clés et résumé
- Les agents pathogènes fongiques provoquent rarement des maladies respiratoires chez les personnes en bonne santé, mais l'inhalation de spores fongiques peut provoquer une pneumonie grave et des infections systémiques chez les patients immunodéprimés.
- Les médicaments antifongiques tels que l'amphotéricine B peuvent contrôler la plupart des infections respiratoires fongiques.
- L'histoplasmose est causée par une moisissure qui pousse dans un sol riche en excréments d'oiseaux ou de chauves-souris. Peu de personnes exposées tombent malades, mais les personnes vulnérables sont vulnérables. Les cellules infectieuses ressemblant à de la levure se développent à l'intérieur des phagocytes.
- La coccidioïdomycose est également contractée à partir du sol et, chez certaines personnes, peut provoquer des lésions sur le visage. Les cas extrêmes peuvent infecter d'autres organes et entraîner la mort.
- La blastomycose, une maladie rare causée par un champignon du sol, provoque généralement une légère infection pulmonaire mais peut se propager chez les personnes immunodéprimées. Les cas systémiques sont mortels s'ils ne sont pas traités.
- La mucormycose est une maladie rare causée par des champignons de l'ordre des Mucorales. Elle touche principalement les personnes immunodéprimées. L'infection implique la croissance des hyphes dans les tissus infectés et peut entraîner la mort dans certains cas.
- L'aspergillose, causée par le champignon du sol Aspergillus, infecte les personnes immunodéprimées. Les boules hyphales peuvent nuire à la fonction pulmonaire et la croissance des hyphes dans les tissus peut provoquer des dommages. Les formes disséminées peuvent entraîner la mort.
- La pneumonie à pneumocystis est causée par le champignon P. jirovecii. La maladie touche les patients atteints du SIDA et d'autres personnes immunodéprimées. Les traitements aux sulfamides ont des effets secondaires, mais les cas non traités peuvent être mortels.
- La cryptococcose est causée par Cryptococcus neoformans. Les infections pulmonaires peuvent se déplacer vers le cerveau et provoquer une méningite, qui peut être fatale.
Notes
- 1 NE Manos et coll. « Variation géographique de la prévalence de la sensibilité à l'histoplasmine. » Dis Chest 29, n° 6 (1956) :649—668.
- 2 rue Hospenthal. « Coccioïdomycose. » Medscape. 2015. http://emedicine.medscape.com/article/215978-overview. Consulté le 7 juillet 2016.
- 3 HY Lau et NJ Ashbolt. « Le rôle des biofilms et des protozoaires dans la pathogenèse de la légionelle : implications pour l'eau potable ». Journal of Applied Microbiology 107 no 2 (2009) :368—378.
- 4 centres pour le contrôle et la prévention des maladies. « Maladies fongiques. Définition de la mucormycose. » 2015 http://www.cdc.gov/fungal/diseases/m...efinition.html. Consulté le 7 juillet 2016.
- 5 centres pour le contrôle et la prévention des maladies. « Maladies fongiques. Symptômes de la mucormycose. » 2015 http://www.cdc.gov/fungal/diseases/m... /symptoms.html. Consulté le 7 juillet 2016.
- 6 MM Roden et coll. « Épidémiologie et évolution de la zygomycose : examen de 929 cas signalés ». Maladies infectieuses cliniques 41 no 5 (2005) :634—653.


