17.3 : Défenses cellulaires
- Page ID
- 187591
Objectifs d'apprentissage
- Identifier et décrire les composants du sang
- Expliquer le processus de formation des éléments du sang formés (hématopoïèse)
- Décrire les caractéristiques des éléments formés présents dans le sang périphérique, ainsi que leurs fonctions respectives au sein du système immunitaire inné
Dans la section précédente, nous avons discuté de certains des médiateurs chimiques présents dans le plasma, la partie liquide du sang. La partie non liquide du sang est constituée de différents types d'éléments formés, appelés ainsi parce qu'ils sont tous formés à partir des mêmes cellules souches que celles présentes dans la moelle osseuse. Les trois principales catégories d'éléments formés sont : les globules rouges (GR), également appelés érythrocytes ; les plaquettes, également appelées thrombocytes ; et les globules blancs (WBC), également appelés leucocytes.
Les globules rouges sont principalement responsables du transport de l'oxygène vers les tissus. Les plaquettes sont des fragments cellulaires qui participent à la formation de caillots sanguins et à la réparation des tissus. Plusieurs types de globules blancs participent à divers mécanismes non spécifiques d'immunité innée et adaptative. Dans cette section, nous nous concentrerons principalement sur les mécanismes innés de différents types de WBC.
Hématopoïèse
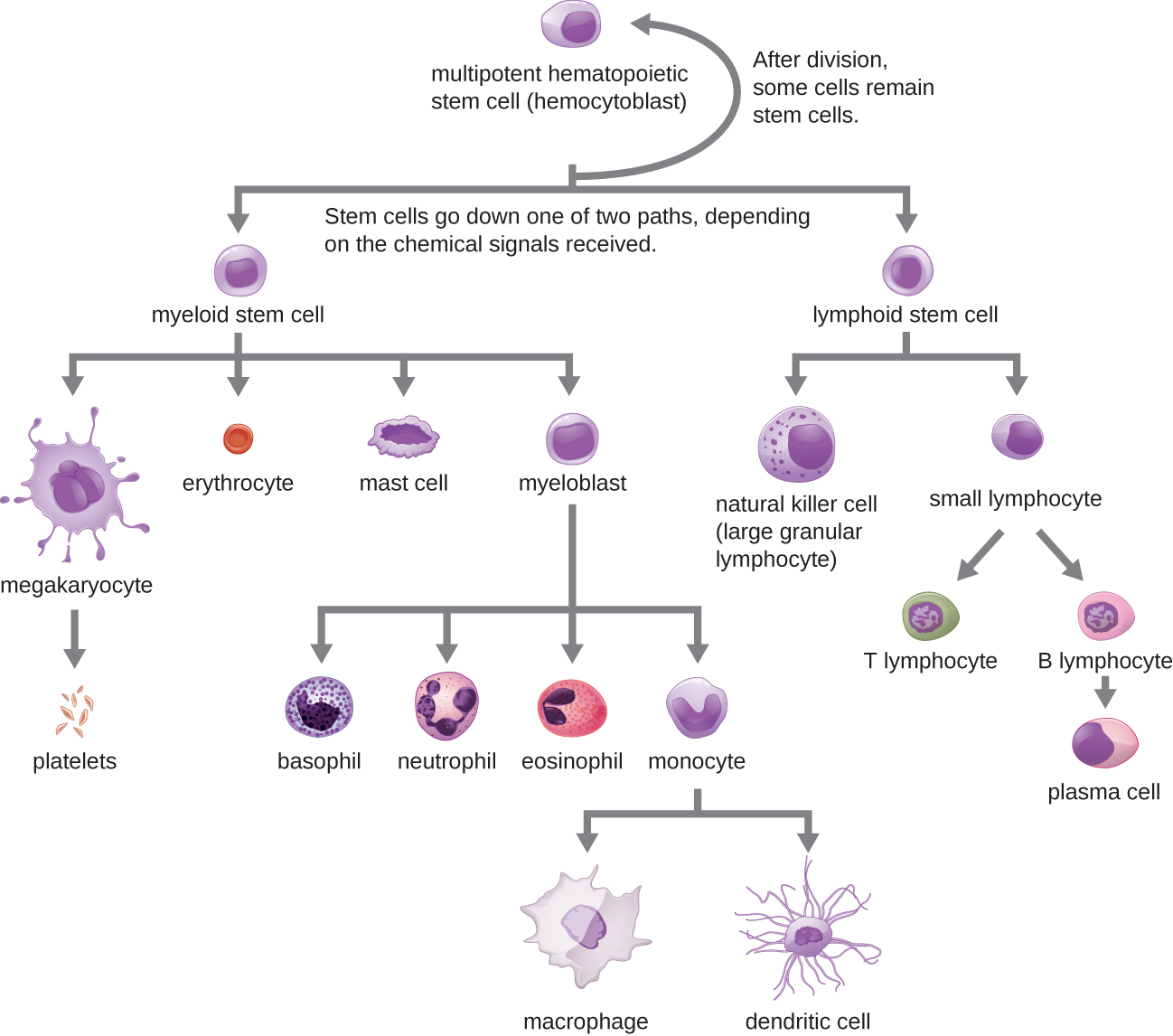
Tous les éléments du sang formés proviennent de cellules souches hématopoïétiques pluripotentes (CSH) présentes dans la moelle osseuse. Au fur et à mesure que les CSH se reproduisent dans la moelle osseuse, les cellules individuelles reçoivent différents signaux de l'organisme qui contrôlent leur développement et leur maturation. En conséquence, les CSH se différencient en différents types de cellules sanguines qui, une fois matures, circulent dans le sang périphérique. Ce processus de différenciation, appelé hématopoïèse, est illustré plus en détail sur la Figure\(\PageIndex{1}\).
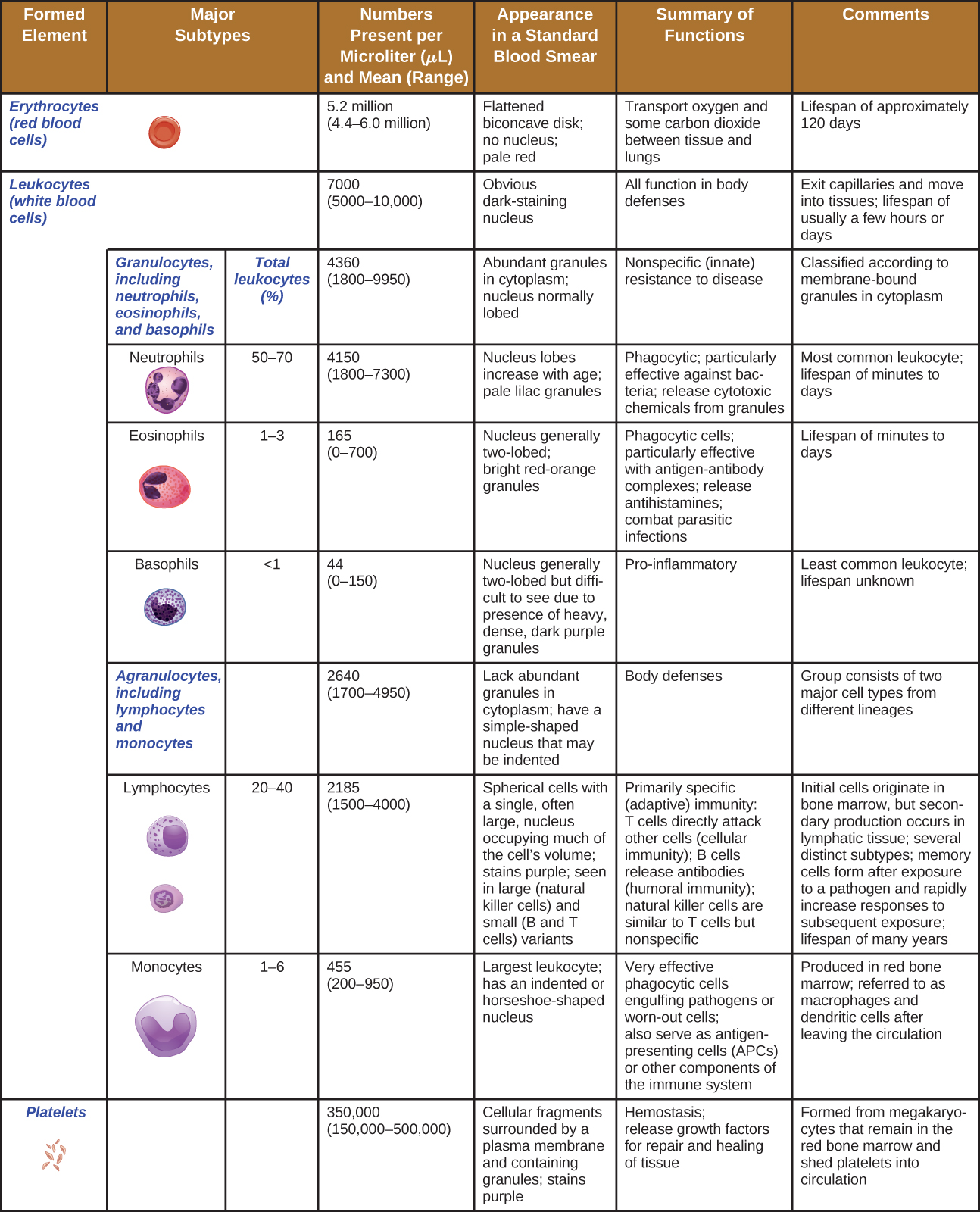
En termes de nombre, la grande majorité des CSH deviennent des érythrocytes. Des nombres beaucoup plus petits deviennent des leucocytes et des plaquettes. Les leucocytes peuvent être subdivisés en granulocytes, caractérisés par de nombreux granules visibles dans le cytoplasme, et en agranulocytes, dépourvus de granules. La figure\(\PageIndex{2}\) fournit une vue d'ensemble des différents types d'éléments formés, y compris leur nombre relatif, leur fonction principale et leur durée de vie.
Granulocytes
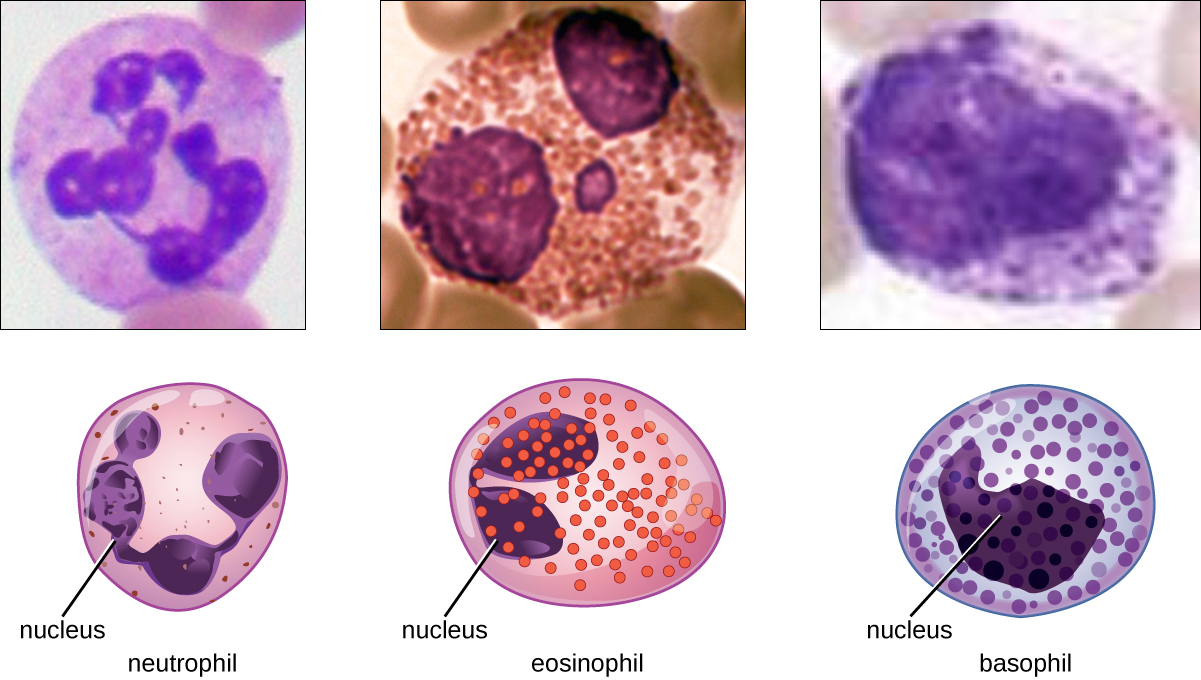
Les différents types de granulocytes peuvent être distingués les uns des autres lors d'un frottis sanguin par l'apparence de leurs noyaux et par le contenu de leurs granules, qui leur confèrent des traits, des fonctions et des propriétés colorantes différents. Les neutrophiles, également appelés neutrophiles polymorphonucléaires (PMN), ont un noyau de trois à cinq lobes et de petits granules nombreux de couleur lilas. Chaque lobe du noyau est relié par un mince fil de matériau aux autres lobes. Les éosinophiles ont moins de lobes dans le noyau (généralement 2 à 3) et des granules plus gros qui se colorent en orange rougeâtre. Les basophiles ont un noyau à deux lobes et de gros granules qui se colorent en bleu foncé ou en violet (Figure\(\PageIndex{3}\)).
Neutrophiles (PMN)
Les neutrophiles (PMN) sont fréquemment impliqués dans l'élimination et la destruction des bactéries extracellulaires. Ils sont capables de migrer à travers les parois des vaisseaux sanguins vers les zones d'infection bactérienne et de lésions tissulaires, où ils recherchent et tuent les bactéries infectieuses. Les granulés de PMN contiennent une variété de défensines et d'enzymes hydrolytiques qui les aident à détruire les bactéries par phagocytose (décrite plus en détail dans Reconnaissance des agents pathogènes et phagocytose). De plus, lorsque de nombreux neutrophiles sont introduits dans une zone infectée, ils peuvent être stimulés pour libérer des substances toxiques des molécules dans les tissus environnants pour mieux éliminer les agents infectieux. C'est ce qu'on appelle la dégranulation.
Un autre mécanisme utilisé par les neutrophiles est celui des pièges extracellulaires (TNE) neutrophiles, qui sont des mailles extrudées de chromatine étroitement associées aux protéines et composants des granulés antimicrobiens. La chromatine est de l'ADN auquel sont associées des protéines (généralement des protéines histones, autour desquelles l'ADN s'enroule pour s'organiser et se regrouper au sein d'une cellule). En créant et en libérant un maillage ou une structure de type réseau de chromatine associée à des protéines antimicrobiennes, les neutrophiles peuvent lancer une attaque hautement concentrée et efficace contre les agents pathogènes voisins. Les protéines fréquemment associées aux TNE comprennent la lactoferrine, la gélatinase, la cathepsine G et la myéloperoxydase. Chacun possède un moyen différent de promouvoir l'activité antimicrobienne, aidant ainsi les neutrophiles à éliminer les agents pathogènes. Les protéines toxiques présentes dans les TNE peuvent détruire certaines cellules de l'organisme ainsi que les agents pathogènes envahissants. Cependant, ces dommages collatéraux peuvent être réparés une fois que le risque d'infection a été éliminé.
Lorsque les neutrophiles combattent une infection, on peut observer une accumulation visible de leucocytes, de débris cellulaires et de bactéries sur le site de l'infection. Cette accumulation est ce que nous appelons le pus (également appelé écoulement ou drainage purulent ou suppuratif). La présence de pus indique que les défenses immunitaires ont été activées contre une infection ; historiquement, certains médecins pensaient que l'induction de la formation de pus pouvait en fait favoriser la cicatrisation des plaies. La pratique consistant à promouvoir le « pus louable » (par exemple en enveloppant une plaie dans de la laine grasse imbibée de vin) remonte à l'ancien médecin Galen au IIe siècle après JC et a été pratiquée sous différentes formes jusqu'au XVIIe siècle (bien qu'elle n'ait pas été universellement acceptée). Aujourd'hui, cette méthode n'est plus pratiquée car on sait maintenant qu'elle n'est pas efficace. Bien qu'une petite quantité de pus puisse indiquer une forte réponse immunitaire, l'induction artificielle de la formation de pus ne favorise pas la guérison.
Éosinophiles
Les éosinophiles sont des granulocytes qui protègent contre les protozoaires et les helminthes ; ils jouent également un rôle dans les réactions allergiques. Les granules d'éosinophiles, qui absorbent facilement l'éosine, un colorant rougeâtre acide, contiennent de l'histamine, des enzymes de dégradation et un composé connu sous le nom de protéine basique majeure (MBP) (Figure\(\PageIndex{3}\)). Le MBP se lie aux glucides de surface des parasites, et cette liaison est associée à une perturbation de la membrane cellulaire et de la perméabilité de la membrane.
Basophiles
Les basophiles possèdent des granules cytoplasmiques de tailles variées et sont nommés pour leur capacité à absorber le colorant basique bleu de méthylène (Figure\(\PageIndex{3}\)). Leur stimulation et leur dégranulation peuvent résulter de multiples événements déclencheurs. Les fragments du complément activé C3a et C5a, produits dans les cascades d'activation des protéines du complément, agissent comme des anaphylatoxines en induisant la dégranulation des basophiles et des réponses inflammatoires. Ce type de cellule joue un rôle important dans les réactions allergiques et autres réactions impliquant une inflammation. L'un des composants les plus abondants des granules de basophiles est l'histamine, qui est libérée avec d'autres facteurs chimiques lorsque le basophile est stimulé. Ces produits chimiques peuvent avoir un effet chimiotactique et peuvent aider à combler les espaces entre les cellules des vaisseaux sanguins. D'autres mécanismes de déclenchement des basophiles nécessitent l'aide d'anticorps, comme indiqué dans Lymphocytes B et immunité humorale.
Mastocytes
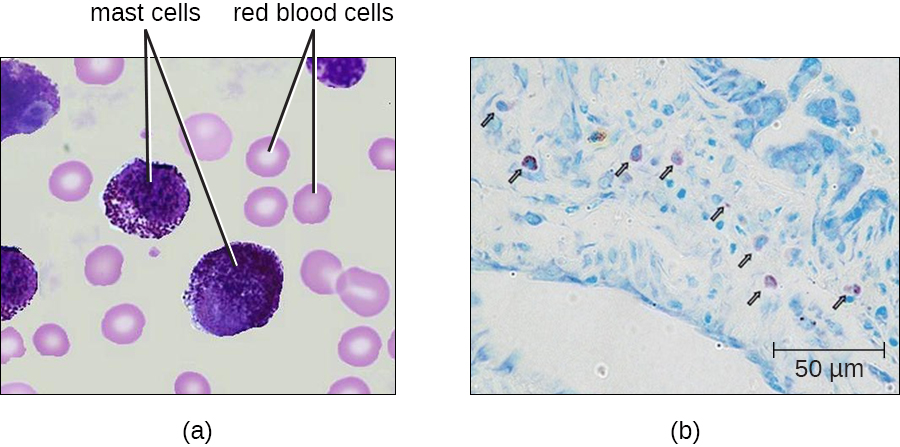
L'hématopoïèse donne également naissance à des mastocytes, qui semblent être dérivés de la même cellule progénitrice myéloïde courante que les neutrophiles, les éosinophiles et les basophiles. Sur le plan fonctionnel, les mastocytes sont très similaires aux basophiles, car ils contiennent bon nombre des mêmes composants dans leurs granules (par exemple, l'histamine) et jouent un rôle similaire dans les réponses allergiques et autres réactions inflammatoires. Cependant, contrairement aux basophiles, les mastocytes quittent le sang en circulation et se trouvent le plus souvent dans les tissus. Ils sont souvent associés aux vaisseaux sanguins et aux nerfs ou se trouvent à proximité de surfaces qui interagissent avec l'environnement extérieur, telles que la peau et les muqueuses de diverses régions du corps (Figure\(\PageIndex{4}\)).
Exercice\(\PageIndex{1}\)
- Décrivez les granules et les noyaux des neutrophiles, des éosinophiles, des basophiles et des mastocytes.
- Nommez trois mécanismes antimicrobiens des neutrophiles
Orientation clinique : 3e partie
Les tests d'Angela se révèlent négatifs pour tous les allergènes courants, et ses échantillons de crachats ne contiennent aucune présence anormale de microbes pathogènes ou de niveaux élevés de membres du microbiote respiratoire normal. Elle a toutefois des taux élevés de cytokines inflammatoires dans son sang.
Le gonflement de ses voies respiratoires n'a toujours pas répondu au traitement aux antihistaminiques ou aux corticostéroïdes. Des analyses sanguines supplémentaires montrent qu'Angela a un nombre de globules blancs légèrement élevé mais un taux d'anticorps normal. De plus, elle a un taux inférieur à la normale de la protéine C4 du complément.
Exercice\(\PageIndex{2}\)
- Que révèlent ces nouvelles informations sur la cause du rétrécissement des voies respiratoires d'Angela ?
- Quelles sont les conditions susceptibles d'entraîner de faibles niveaux de protéines du complément ?
Agranulocytes
Comme leur nom l'indique, les agranulocytes sont dépourvus de granules visibles dans le cytoplasme. Les agranulocytes peuvent être classés en lymphocytes ou en monocytes (Figure\(\PageIndex{2}\)). Parmi les lymphocytes se trouvent des cellules tueuses naturelles, qui jouent un rôle important dans les défenses immunitaires innées non spécifiques. Les lymphocytes incluent également les lymphocytes B et les lymphocytes T, qui sont abordés dans le chapitre suivant car ils jouent un rôle central dans les défenses immunitaires adaptatives spécifiques. Les monocytes se différencient en macrophages et en cellules dendritiques, que l'on appelle collectivement le système phagocytaire mononucléaire.
Cellules tueuses naturelles
La plupart des lymphocytes sont principalement impliqués dans la réponse immunitaire adaptative spécifique et seront donc abordés dans le chapitre suivant. Les cellules tueuses naturelles (cellules NK) constituent une exception ; ces lymphocytes mononucléaires utilisent des mécanismes non spécifiques pour reconnaître et détruire les cellules anormales d'une manière ou d'une autre. Les cellules cancéreuses et les cellules infectées par des virus sont deux exemples d'anomalies cellulaires ciblées par les cellules NK. La reconnaissance de telles cellules implique un processus complexe d'identification de marqueurs moléculaires inhibiteurs et activateurs à la surface de la cellule cible. Les marqueurs moléculaires qui constituent le complexe majeur d'histocompatibilité (CMH) sont exprimés par les cellules saines comme une indication de « soi ». Ce point sera abordé plus en détail dans le chapitre suivant. Les cellules NK sont capables de reconnaître les marqueurs MHC normaux à la surface des cellules saines, et ces marqueurs MHC servent de signal inhibiteur empêchant l'activation des cellules NK. Cependant, les cellules cancéreuses et les cellules infectées par des virus diminuent ou éliminent activement l'expression des marqueurs du CMH à leur surface. Lorsque ces marqueurs du MHC sont diminués ou absents, la cellule NK interprète cela comme une anomalie et une cellule en détresse. Il s'agit d'une partie du processus d'activation des cellules NK (Figure\(\PageIndex{5}\)). Les cellules NK sont également activées en se liant à des molécules moléculaires activantes sur la cellule cible. Ces molécules moléculaires activantes incluent des molécules « auto-modifiées » ou « non personnelles ». Lorsqu'une cellule NK reconnaît une diminution des molécules normales inhibitrices du MHC et une augmentation des molécules activatrices à la surface d'une cellule, la cellule NK sera activée pour éliminer la cellule en détresse.
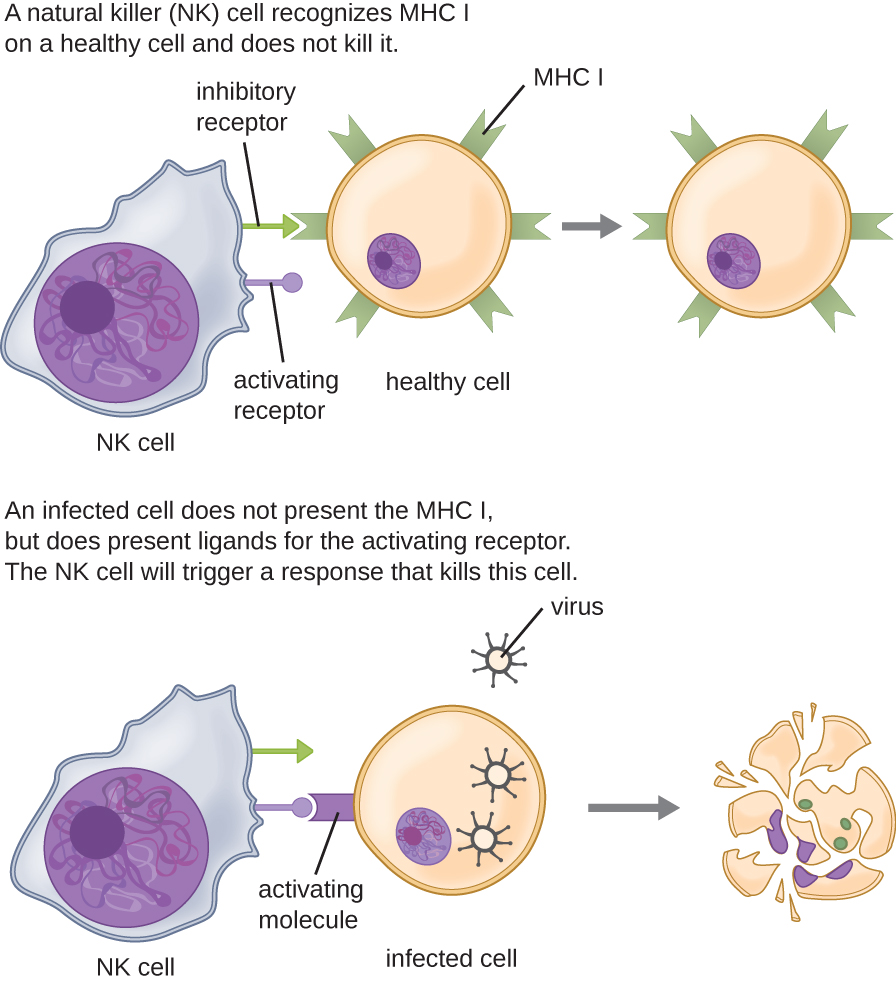
Une fois qu'une cellule est reconnue comme cible, la cellule NK peut utiliser différents mécanismes pour tuer sa cible. Par exemple, il peut exprimer des protéines membranaires cytotoxiques et des cytokines qui stimulent l'apoptose ou le suicide cellulaire contrôlé de la cellule cible. Les cellules NK peuvent également utiliser la cytotoxicité médiée par la perforine pour induire l'apoptose dans les cellules cibles. Ce mécanisme repose sur deux toxines libérées par les granules du cytoplasme de la cellule NK : la perforine, une protéine qui crée des pores dans la cellule cible, et les granzymes, des protéases qui pénètrent par les pores dans le cytoplasme de la cellule cible, où elles déclenchent une cascade d'activation protéique menant à l'apoptose. La cellule NK se lie à la cellule cible anormale, libère sa charge utile destructrice et se détache de la cellule cible. Alors que la cellule cible subit une apoptose, la cellule NK synthétise davantage de perforine et de protéases à utiliser sur sa prochaine cible.
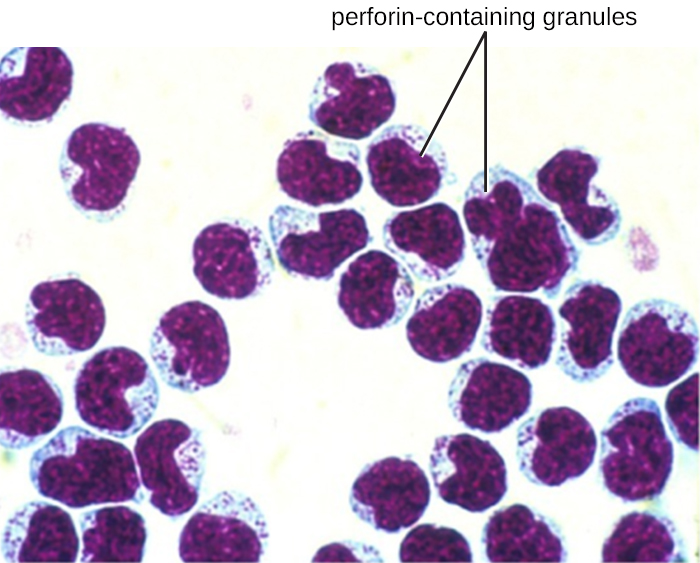
Les cellules NK contiennent ces composés toxiques sous forme de granules dans leur cytoplasme. Une fois colorés, les granulés sont azurophiles et peuvent être visualisés au microscope optique (Figure\(\PageIndex{6}\)). Même si elles contiennent des granules, les cellules NK ne sont pas considérées comme des granulocytes car leurs granules sont beaucoup moins nombreux que ceux trouvés dans les vrais granulocytes. De plus, les cellules NK ont une lignée différente de celle des granulocytes, provenant de cellules souches lymphoïdes plutôt que myéloïdes (Figure\(\PageIndex{1}\)).
Monocytes
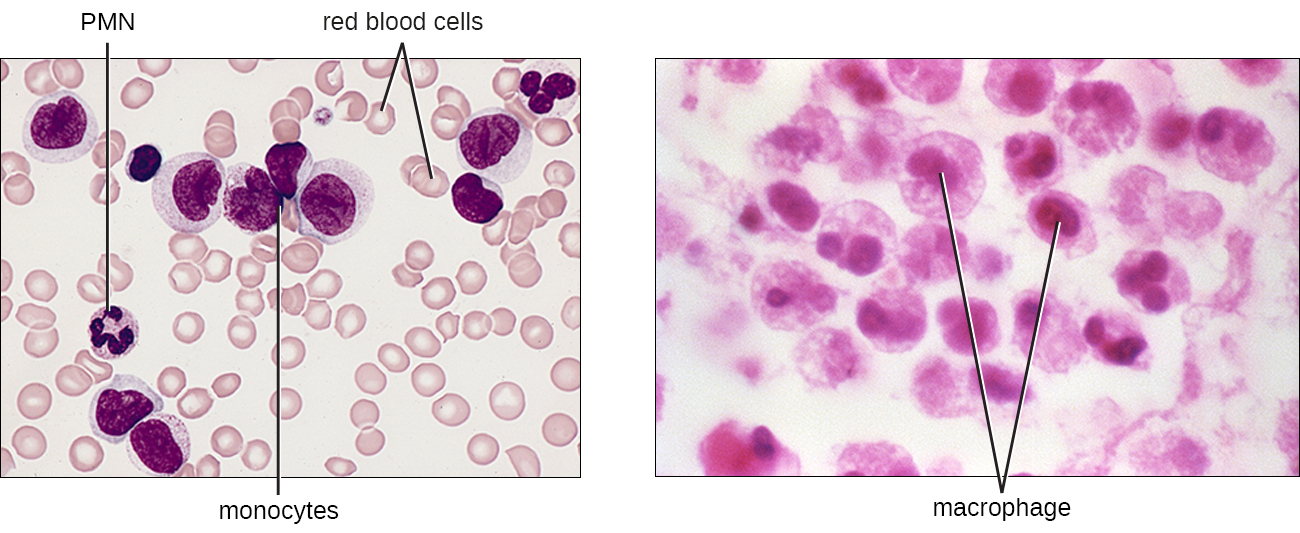
Les monocytes, qui sont les plus gros globules blancs, ont un noyau dépourvu de lobes et ils sont également dépourvus de granules dans le cytoplasme (Figure\(\PageIndex{7}\)). Néanmoins, ce sont des phagocytes efficaces qui engloutissent les agents pathogènes et les cellules apoptotiques pour aider à combattre les infections.
Lorsque les monocytes quittent la circulation sanguine et pénètrent dans un tissu corporel spécifique, ils se différencient en phagocytes spécifiques aux tissus appelés macrophages et cellules dendritiques. Ce sont des résidents particulièrement importants des tissus lymphoïdes, ainsi que des sites et organes non lymphoïdes. Les macrophages et les cellules dendritiques peuvent rester longtemps dans les tissus corporels. Les macrophages présents dans des tissus corporels spécifiques développent des caractéristiques adaptées au tissu en question. Non seulement ils fournissent une protection immunitaire aux tissus dans lesquels ils résident, mais ils soutiennent également le fonctionnement normal des cellules tissulaires voisines grâce à la production de cytokines. Les macrophages reçoivent des noms spécifiques aux tissus, et quelques exemples de macrophages spécifiques aux tissus sont répertoriés dans le tableau\(\PageIndex{1}\). Les cellules dendritiques sont d'importantes sentinelles présentes dans la peau et les muqueuses, qui sont des portes d'entrée pour de nombreux agents pathogènes. Les monocytes, les macrophages et les cellules dendritiques sont tous hautement phagocytaires et d'importants promoteurs de la réponse immunitaire par leur production et leur libération de cytokines. Ces cellules constituent un pont essentiel entre les réponses immunitaires innées et adaptatives, comme indiqué dans la section suivante ainsi que dans le chapitre suivant.
| Tissu | Macrophage |
|---|---|
| Cerveau et système nerveux central | Cellules microgliales |
| Foie | Cellules de Kupffer |
| Poumons | Macrophages alvéolaires (cellules à poussière) |
| Cavité péritonéale | Macrophages péritonéaux |
Exercice\(\PageIndex{3}\)
- Décrivez les signaux qui activent les cellules tueuses naturelles.
- Quelle est la différence entre les monocytes et les macrophages ?
Concepts clés et résumé
- Les éléments formés dans le sang comprennent les globules rouges (érythrocytes), les globules blancs (leucocytes) et les plaquettes (thrombocytes). Parmi ceux-ci, les leucocytes sont principalement impliqués dans la réponse immunitaire.
- Tous les éléments formés proviennent de la moelle osseuse sous forme de cellules souches (CSH) qui se différencient par hématopoïèse.
- Les granulocytes sont des leucocytes caractérisés par un noyau lobé et des granules dans le cytoplasme. Il s'agit notamment des neutrophiles (PMN), des éosinophiles et des basophiles.
- Les neutrophiles sont les leucocytes les plus nombreux dans le sang et ils combattent principalement les infections bactériennes.
- Les éosinophiles ciblent les infections parasitaires. Les éosinophiles et les basophiles sont impliqués dans les réactions allergiques. Les deux libèrent de l'histamine et d'autres composés pro-inflammatoires de leurs granules lors de la stimulation.
- Les mastocytes fonctionnent de la même manière que les basophiles, mais ils peuvent être trouvés dans des tissus extérieurs à la circulation sanguine.
- Les cellules tueuses naturelles (NK) sont des lymphocytes qui reconnaissent et tuent les cellules anormales ou infectées en libérant des protéines qui déclenchent l'apoptose.
- Les monocytes sont de gros leucocytes mononucléaires qui circulent dans le sang. Ils peuvent quitter la circulation sanguine et s'installer dans les tissus corporels, où ils se différencient et deviennent des macrophages et des cellules dendritiques spécifiques aux tissus.


