2.6 : Composés moléculaires et ioniques
- Page ID
- 193945
- Définir les composés ioniques et moléculaires (covalents)
- Prédire le type de composé formé à partir des éléments en fonction de leur emplacement dans le tableau périodique
- Déterminer les formules pour les composés ioniques simples
Dans les réactions chimiques ordinaires, le noyau de chaque atome (et donc l'identité de l'élément) reste inchangé. Les électrons peuvent toutefois être ajoutés aux atomes par transfert depuis d'autres atomes, perdus par transfert vers d'autres atomes ou partagés avec d'autres atomes. Le transfert et le partage des électrons entre les atomes régissent la chimie des éléments. Lors de la formation de certains composés, les atomes gagnent ou perdent des électrons et forment des particules chargées électriquement appelées ions (Figure\(\PageIndex{1}\)).
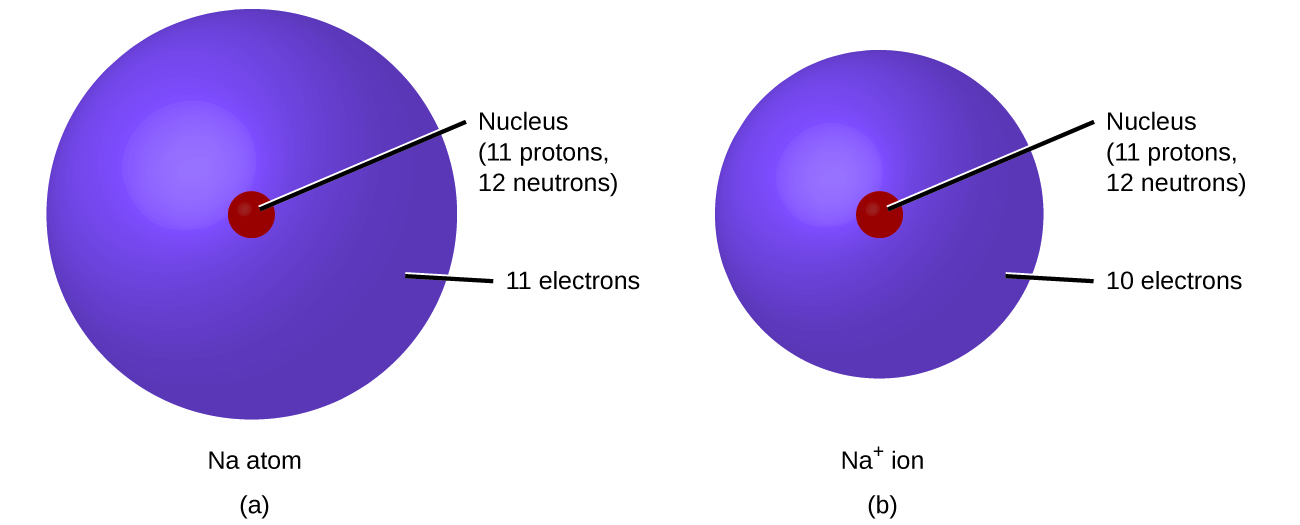
Vous pouvez utiliser le tableau périodique pour prédire si un atome formera un anion ou un cation, et vous pouvez souvent prédire la charge de l'ion résultant. Les atomes de nombreux métaux du groupe principal perdent suffisamment d'électrons pour leur laisser le même nombre d'électrons qu'un atome du gaz rare précédent. À titre d'illustration, un atome d'un métal alcalin (groupe 1) perd un électron et forme un cation avec une charge 1+ ; un métal alcalino-terreux (groupe 2) perd deux électrons et forme un cation avec une charge 2+, etc. Par exemple, un atome de calcium neutre, composé de 20 protons et de 20 électrons, perd facilement deux électrons. Il en résulte un cation contenant 20 protons, 18 électrons et une charge 2+. Il possède le même nombre d'électrons que les atomes du gaz rare précédent, l'argon, et est symbolisé Ca 2 +. Le nom d'un ion métallique étant le même que celui de l'atome métallique à partir duquel il se forme, le Ca 2 + est appelé ion calcium.
Lorsque les atomes d'éléments non métalliques forment des ions, ils gagnent généralement suffisamment d'électrons pour leur donner le même nombre d'électrons qu'un atome du gaz rare suivant dans le tableau périodique. Les atomes du groupe 17 gagnent un électron et forment des anions avec une charge 1− ; les atomes du groupe 16 gagnent deux électrons et forment des ions avec une charge 2−, et ainsi de suite. Par exemple, l'atome de brome neutre, qui possède 35 protons et 35 électrons, peut gagner un électron pour lui fournir 36 électrons. Il en résulte un anion avec 35 protons, 36 électrons et une charge de 1. Il possède le même nombre d'électrons que les atomes du gaz noble suivant, le krypton, et est symbolisé Br −. (Une discussion de la théorie soutenant le statut privilégié du nombre d'électrons des gaz rares reflétée dans ces règles prédictives pour la formation d'ions est fournie dans un chapitre ultérieur de ce texte.)
Notez l'utilité du tableau périodique pour prédire la formation et la charge ioniques probables (Figure\(\PageIndex{2}\)). En se déplaçant de l'extrême gauche vers la droite sur le tableau périodique, les éléments du groupe principal ont tendance à former des cations dont la charge est égale au numéro du groupe. C'est-à-dire que les éléments du groupe 1 forment des ions 1+ ; les éléments du groupe 2 forment des ions 2+, etc. En se déplaçant de l'extrême droite vers la gauche du tableau périodique, les éléments forment souvent des anions avec une charge négative égale au nombre de groupes déplacés vers la gauche à partir des gaz rares. Par exemple, les éléments du groupe 17 (il reste un groupe parmi les gaz rares) forment des ions 1− ; les éléments du groupe 16 (il reste deux groupes) forment des ions 2−, et ainsi de suite. Cette tendance peut être utilisée comme guide dans de nombreux cas, mais sa valeur prédictive diminue lorsque l'on se déplace vers le centre du tableau périodique. En fait, les métaux de transition et certains autres métaux présentent souvent des charges variables qui ne sont pas prévisibles compte tenu de leur position dans le tableau. Par exemple, le cuivre peut former des ions avec une charge 1+ ou 2+, et le fer peut former des ions avec une charge 2+ ou 3+.
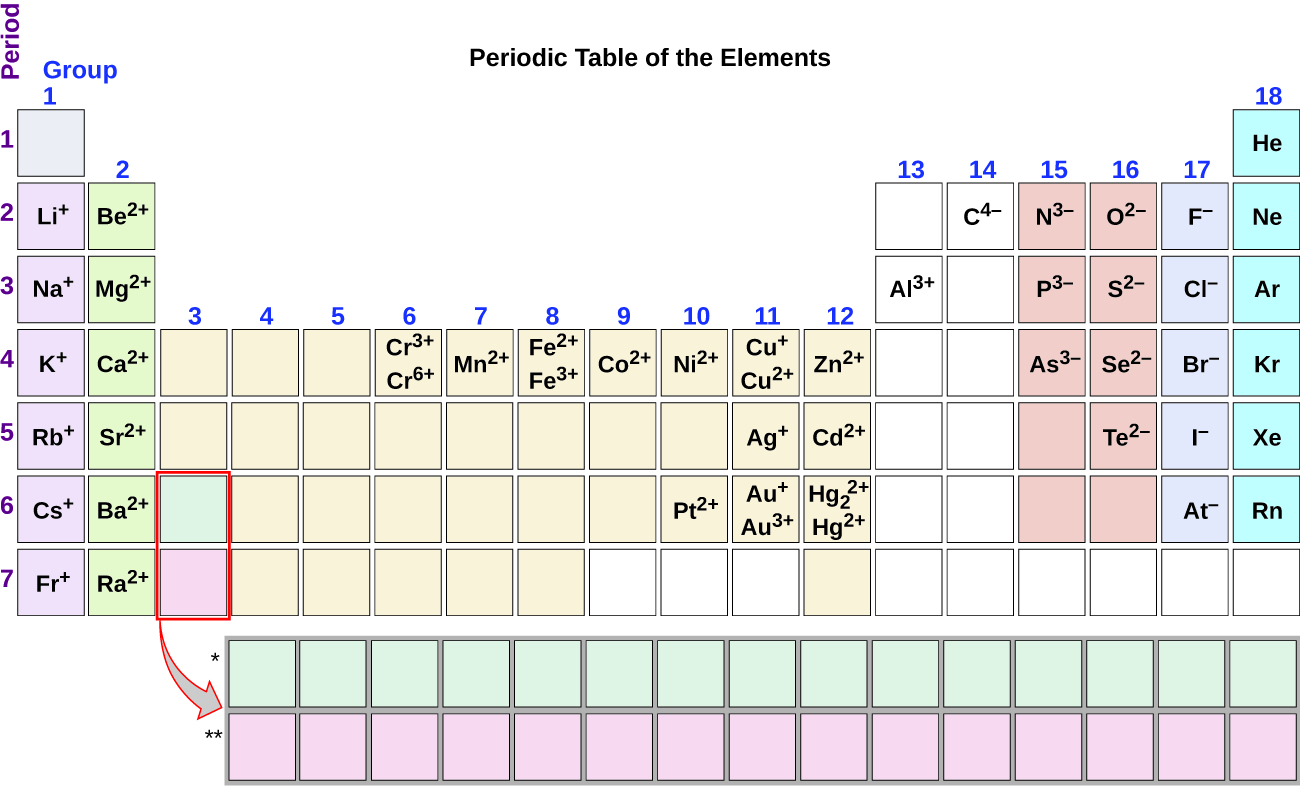
Un ion présent dans certains composés utilisés comme antitranspirants contient 13 protons et 10 électrons. Quel est son symbole ?
Solution
Comme le nombre de protons reste inchangé lorsqu'un atome forme un ion, le numéro atomique de l'élément doit être 13. Sachant cela, nous pouvons utiliser le tableau périodique pour identifier l'élément comme étant Al (aluminium). L'atome d'Al a perdu trois électrons et possède donc trois charges positives (13) de plus qu'il n'en a (10). Il s'agit du cation aluminium, Al 3 +.
Donnez le symbole et le nom de l'ion composé de 34 protons et de 36 électrons.
- Réponse
-
Se 2 −, l'ion séléniure
Le magnésium et l'azote réagissent pour former un composé ionique. Prédisez qui forme un anion, qui forme un cation, et les charges de chaque ion. Écrivez le symbole de chaque ion et nommez-les.
Solution
La position du magnésium dans le tableau périodique (groupe 2) nous indique qu'il s'agit d'un métal. Les métaux forment des ions positifs (cations). Un atome de magnésium doit perdre deux électrons pour avoir le même nombre d'électrons qu'un atome du gaz rare précédent, le néon. Ainsi, un atome de magnésium formera un cation avec deux électrons de moins que les protons et une charge de 2+. Le symbole de l'ion est Mg 2 +, appelé ion magnésium.
La position de l'azote dans le tableau périodique (groupe 15) révèle qu'il s'agit d'un non-métal. Les substances non métalliques forment des ions négatifs (anions). Un atome d'azote doit gagner trois électrons pour avoir le même nombre d'électrons qu'un atome du gaz rare suivant, le néon. Ainsi, un atome d'azote formera un anion contenant trois électrons de plus que des protons et une charge de 3−. Le symbole de l'ion est N 3−, appelé ion nitrure.
L'aluminium et le carbone réagissent pour former un composé ionique. Prédisez qui forme un anion, qui forme un cation, et les charges de chaque ion. Écrivez le symbole de chaque ion et nommez-les.
- Réponse
-
Al formera un cation avec une charge de 3+ : Al 3 +, un ion aluminium. Le carbone formera un anion avec une charge de 4− : C 4−, un ion carbure.
Les ions dont nous avons discuté jusqu'à présent sont appelés ions monatomiques, c'est-à-dire que ce sont des ions formés à partir d'un seul atome. On trouve également de nombreux ions polyatomiques. Ces ions, qui agissent comme des unités discrètes, sont des molécules chargées électriquement (un groupe d'atomes liés ayant une charge globale). Certains des ions polyatomiques les plus importants sont répertoriés dans le tableau\(\PageIndex{1}\). Les oxyanions sont des ions polyatomiques qui contiennent un ou plusieurs atomes d'oxygène. À ce stade de votre étude de la chimie, vous devez mémoriser les noms, les formules et les charges des ions polyatomiques les plus courants. Comme vous les utiliserez à plusieurs reprises, ils vous seront bientôt familiers.
| Nom | Formule | Acide apparenté | Formule |
|---|---|---|---|
| ammonium | \(\ce{NH4+}\) | ||
| hydronium | \(\ce{H_3O^+}\) | ||
| oxyde | \(\ce{O^{2-}}\) | ||
| peroxyde | \(\ce{O_2^{2-}}\) | ||
| hydroxyde | \(\ce{OH^-}\) | ||
| acétate | \(\ce{CH_3COO^-}\) | acide acétique | \(\ce{CH_3COOH}\) |
| cyanure | \(\ce{CN^-}\) | acide cyanhydrique | \(\ce{HCN}\) |
| azide | \(\ce{N_3^-}\) | acide hydrazoïque | \(\ce{HN_3}\) |
| carbonate | \(\ce{CO_3^{2-}}\) | acide carbonique | \(\ce{H_2CO_3}\) |
| bicarbonate | \(\ce{HCO_3^-}\) | ||
| nitrate | \(\ce{NO_3^-}\) | acide nitrique | \(\ce{HNO_3}\) |
| nitrite | \(\ce{NO_2^-}\) | acide nitreux | \(\ce{HNO_2}\) |
| sulfate | \(\ce{SO_4^{2-}}\) | acide sulfurique | \(\ce{H_2SO_4}\) |
| sulfate d'hydrogène | \(\ce{HSO_4^-}\) | ||
| sulfite | \(\ce{SO_3^{2-}}\) | acide sulfureux | \(\ce{H_2SO_3}\) |
| sulfite d'hydrogène | \(\ce{HSO_3^-}\) | ||
| phosphate | \(\ce{PO_4^{3-}}\) | acide phosphorique | \(\ce{H_3PO_4}\) |
| phosphate d'hydrogène | \(\ce{HPO_4^{2-}}\) | ||
| phosphate dihydrogéné | \(\ce{H_2PO_4^-}\) | ||
| perchlorate | \(\ce{ClO_4^-}\) | acide perchlorique | \(\ce{HClO_4}\) |
| chlorate | \(\ce{ClO_3^-}\) | acide chlorique | \(\ce{HClO_3}\) |
| chlorite | \(\ce{ClO_2^-}\) | acide chloreux | \(\ce{HClO_2}\) |
| hypochlorite | \(\ce{ClO^-}\) | acide hypochloreux | \(\ce{HClO}\) |
| chromate | \(\ce{CrO_4^{2-}}\) | acide chromique | \(\ce{H_2CrO_4}\) |
| bichromate | \(\ce{Cr_2O_7^{2-}}\) | acide dichromique | \(\ce{H_2Cr_2O7}\) |
| permanganate | \(\ce{MnO_4^-}\) | acide permanganique | \(\ce{HMnO_4}\) |
Notez qu'il existe un système pour nommer certains ions polyatomiques ; -ate et -ite sont des suffixes désignant des ions polyatomiques contenant plus ou moins d'atomes d'oxygène. Per- (abréviation de « hyper ») et hypo- (qui signifie « sous ») sont des préfixes qui signifient respectivement plus d'atomes d'oxygène que -ate et moins d'atomes d'oxygène que -ite. Par exemple, le perchlorate est\(\ce{ClO4-}\), le chlorate est\(\ce{ClO3-}\), le chlorite est\(\ce{ClO2-}\) et l'hypochlorite est ClO −. Malheureusement, le nombre d'atomes d'oxygène correspondant à un suffixe ou à un préfixe donné n'est pas constant ; par exemple, le nitrate l'est\(\ce{NO3-}\) alors que le sulfate l'est\(\ce{SO4^{2-}}\). Cela sera abordé plus en détail dans le prochain module sur la nomenclature.
La nature des forces d'attraction qui maintiennent les atomes ou les ions ensemble au sein d'un composé est à la base de la classification des liaisons chimiques. Lorsque des électrons sont transférés et que des ions se forment, des liaisons ioniques se forment. Les liaisons ioniques sont des forces d'attraction électrostatiques, c'est-à-dire les forces d'attraction subies entre des objets de charge électrique opposée (dans ce cas, des cations et des anions). Lorsque les électrons sont « partagés » et que des molécules se forment, des liaisons covalentes se forment. Les liaisons covalentes sont les forces d'attraction entre les noyaux chargés positivement des atomes liés et une ou plusieurs paires d'électrons situées entre les atomes. Les composés sont classés comme ioniques ou moléculaires (covalents) sur la base des liaisons qu'ils contiennent.
Composés ioniques
Lorsqu'un élément composé d'atomes qui perdent facilement des électrons (un métal) réagit avec un élément composé d'atomes qui gagnent facilement des électrons (un élément non métallique), un transfert d'électrons se produit généralement, produisant des ions. Le composé formé par ce transfert est stabilisé par les attractions électrostatiques (liaisons ioniques) entre les ions de charge opposée présents dans le composé. Par exemple, lorsque chaque atome de sodium d'un échantillon de métal sodique (groupe 1) donne un électron pour former un cation sodium, Na +, et que chaque atome de chlore d'un échantillon de chlore gazeux (groupe 17) accepte un électron pour former un anion chlorure, Cl −, le composé résultant, NaCl, est composé de des ions sodium et des ions chlorure dans le rapport d'un ion Na + pour chaque ion Cl −. De même, chaque atome de calcium (groupe 2) peut donner deux électrons et en transférer un à chacun des deux atomes de chlore pour former du CaCl 2, qui est composé d'ions Ca 2 + et Cl − dans le rapport entre un ion Ca 2 + et deux ions Cl −.
Un composé qui contient des ions et qui est maintenu ensemble par des liaisons ioniques est appelé composé ionique. Le tableau périodique peut nous aider à reconnaître de nombreux composés ioniques : lorsqu'un métal est combiné à un ou plusieurs éléments non métalliques, le composé est généralement ionique. Ce guide fonctionne bien pour prédire la formation de composés ioniques pour la plupart des composés généralement rencontrés dans un cours d'introduction à la chimie. Cependant, ce n'est pas toujours vrai (par exemple, le chlorure d'aluminium, AlCl 3, n'est pas ionique).
Vous pouvez souvent reconnaître les composés ioniques en raison de leurs propriétés. Les composés ioniques sont des solides qui fondent généralement à des températures élevées et bouillent à des températures encore plus élevées. Par exemple, le chlorure de sodium fond à 801 °C et bout à 1413 °C. (À titre de comparaison, le composé moléculaire de l'eau fond à 0 °C et bout à 100 °C.) Sous forme solide, un composé ionique n'est pas électroconducteur car ses ions ne peuvent pas circuler (« électricité » est le flux de particules chargées). Cependant, lorsqu'il est fondu, il peut conduire l'électricité car ses ions peuvent se déplacer librement dans le liquide (Figure\(\PageIndex{3}\)).

Dans chaque composé ionique, le nombre total de charges positives des cations est égal au nombre total de charges négatives des anions. Ainsi, les composés ioniques sont globalement neutres sur le plan électrique, même s'ils contiennent des ions positifs et négatifs. Nous pouvons utiliser cette observation pour nous aider à écrire la formule d'un composé ionique. La formule d'un composé ionique doit avoir un rapport d'ions tel que les nombres de charges positives et négatives soient égaux.
Le saphir (Figure\(\PageIndex{4}\)) est principalement un composé d'aluminium et d'oxygène qui contient des cations d'aluminium, Al 3 +, et des anions oxygène, O 2−. Quelle est la formule de ce composé ?

Solution Comme le composé ionique doit être électriquement neutre, il doit avoir le même nombre de charges positives et négatives. Deux ions aluminium, chacun avec une charge de 3+, nous donneraient six charges positives, et trois ions oxyde, chacun avec une charge de 2−, nous donneraient six charges négatives. La formule serait Al 2 O 3.
Prédire la formule du composé ionique formé entre le cation sodium, Na +, et l'anion sulfure, S 2−.
- Réponse
-
Na 2 S
De nombreux composés ioniques contiennent des ions polyatomiques (Tableau\(\PageIndex{1}\)) sous forme de cation, d'anion ou des deux. Comme pour les composés ioniques simples, ces composés doivent également être neutres sur le plan électrique, de sorte que leurs formules puissent être prédites en traitant les ions polyatomiques comme des unités discrètes. Nous utilisons des parenthèses dans une formule pour indiquer un groupe d'atomes qui se comportent comme une unité. Par exemple, la formule du phosphate de calcium, l'un des minéraux de nos os, est le Ca 3 (PO 4) 2. Cette formule indique qu'il existe trois ions calcium (Ca 2 +) pour deux\(\left(\ce{PO4^{3-}}\right)\) groupes phosphates. Les\(\ce{PO4^{3-}}\) groupes sont des unités discrètes, chacune constituée d'un atome de phosphore et de quatre atomes d'oxygène, et ayant une charge globale de 3−. Le composé est électriquement neutre et sa formule indique un nombre total de trois atomes de Ca, de deux atomes de P et de huit atomes de O.
La poudre à pâte contient du dihydrogénophosphate de calcium, un composé ionique composé des ions Ca 2 + et\(\ce{H2PO4-}\). Quelle est la formule de ce composé ?
Solution
Les charges positives et négatives doivent être équilibrées et ce composé ionique doit être électriquement neutre. Ainsi, nous devons avoir deux charges négatives pour équilibrer la charge 2+ de l'ion calcium. Cela nécessite un rapport entre un ion Ca 2 + et deux\(\ce{H2PO4-}\) ions. Nous désignons cela en plaçant la formule de l'ion phosphate dihydrogène entre parenthèses et en ajoutant un indice 2. La formule est Ca (H 2 PO 4) 2.
Prédisez la formule du composé ionique formé entre l'ion lithium et l'ion peroxyde\(\ce{O2^2-}\) (Conseil : utilisez le tableau périodique pour prédire le signe et la charge de l'ion lithium.)
- Réponse
-
Li 2 O 2
Comme un composé ionique n'est pas composé de molécules uniques et distinctes, il se peut qu'il ne soit pas correctement symbolisé à l'aide d'une formule moléculaire. Les composés ioniques doivent plutôt être symbolisés par une formule indiquant le nombre relatif de leurs ions constitutifs. Pour les composés contenant uniquement des ions monoatomiques (tels que le NaCl) et pour de nombreux composés contenant des ions polyatomiques (tels que CaSO 4), ces formules ne sont que les formules empiriques présentées plus haut dans ce chapitre. Toutefois, les formules de certains composés ioniques contenant des ions polyatomiques ne sont pas des formules empiriques. Par exemple, le composé ionique oxalate de sodium est composé de Na + et d'\(\ce{C2O4^2-}\)ions combinés dans un rapport de 2:1, et sa formule est écrite comme Na 2 C 2 O 4. Les indices de cette formule ne sont pas les plus petits nombres entiers possibles, car chacun peut être divisé par 2 pour obtenir la formule empirique, NaCO 2. Il ne s'agit toutefois pas de la formule acceptée pour l'oxalate de sodium, car elle ne représente pas avec précision l'anion polyatomique du composé\(\ce{C2O4^2-}\).
Composés moléculaires
De nombreux composés ne contiennent pas d'ions mais se composent uniquement de molécules neutres et discrètes. Ces composés moléculaires (composés covalents) apparaissent lorsque les atomes partagent des électrons plutôt que de les transférer (gagner ou perdre). La liaison covalente est un concept important et étendu en chimie, qui sera traité de manière très détaillée dans un chapitre ultérieur de ce texte. Nous pouvons souvent identifier des composés moléculaires sur la base de leurs propriétés physiques. Dans des conditions normales, les composés moléculaires existent souvent sous forme de gaz, de liquides à bas point d'ébullition et de solides à bas point de fusion, bien qu'il existe de nombreuses exceptions importantes
Alors que les composés ioniques se forment généralement lorsqu'un métal et un non-métal se combinent, les composés covalents sont généralement formés par une combinaison de non-métaux. Ainsi, le tableau périodique peut nous aider à reconnaître de nombreux composés covalents. Bien que nous puissions utiliser la position des éléments d'un composé dans le tableau périodique pour prédire s'il est ionique ou covalent à ce stade de notre étude de la chimie, sachez qu'il s'agit d'une approche très simpliste qui ne tient pas compte d'un certain nombre d'exceptions intéressantes. Des nuances de gris existent entre les composés ioniques et moléculaires, et vous en apprendrez plus à ce sujet plus tard.
Prédisez si les composés suivants sont ioniques ou moléculaires :
- KI, le composé utilisé comme source d'iode dans le sel de table
- H 2 O 2, agent de blanchiment et désinfectant, le peroxyde d'hydrogène
- CHCl 3, le chloroforme anesthésique
- Li 2 CO 3, une source de lithium dans les antidépresseurs
Solution
- Le potassium (groupe 1) est un métal et l'iode (groupe 17) est un non-métal ; le KI devrait être ionique.
- L'hydrogène (groupe 1) est un non-métal et l'oxygène (groupe 16) est un non-métal ; on prévoit que le H 2 O 2 est moléculaire.
- Le carbone (groupe 14) est un non-métal, l'hydrogène (groupe 1) est un non-métal et le chlore (groupe 17) est un non-métal ; le CHCl 3 devrait être moléculaire.
- Le lithium (groupe 1) est un métal et le carbonate est un ion polyatomique ; le Li 2 CO 3 devrait être ionique.
À l'aide du tableau périodique, déterminez si les composés suivants sont ioniques ou covalents :
- DONC 2
- CAF 2
- N° 2 H 4
- Al 2 (ISO 4) 3
- Répondez à une
-
moléculaire
- Réponse b
-
ionique
- Réponse c
-
moléculaire
- Réponse d
-
ionique
Résumé
Les métaux (en particulier ceux des groupes 1 et 2) ont tendance à perdre le nombre d'électrons qui leur laisserait le même nombre d'électrons que dans le gaz rare précédent dans le tableau périodique. Par ce moyen, un ion chargé positivement est formé. De même, les éléments non métalliques (en particulier ceux des groupes 16 et 17 et, dans une moindre mesure, ceux du groupe 15) peuvent obtenir le nombre d'électrons nécessaires pour fournir aux atomes le même nombre d'électrons que dans le gaz rare suivant du tableau périodique. Ainsi, les éléments non métalliques ont tendance à former des ions négatifs. Les ions chargés positivement sont appelés cations et les ions chargés négativement sont appelés anions. Les ions peuvent être monatomiques (contenant un seul atome) ou polyatomiques (contenant plus d'un atome).
Les composés contenant des ions sont appelés composés ioniques. Les composés ioniques se forment généralement à partir de métaux et de non-métaux. Les composés qui ne contiennent pas d'ions, mais qui sont plutôt constitués d'atomes étroitement liés entre eux en molécules (groupes d'atomes non chargés qui se comportent comme une seule unité) sont appelés composés covalents. Les composés covalents se forment généralement à partir de deux ou plusieurs éléments non métalliques.
Lexique
- liaison covalente
- force d'attraction entre les noyaux des atomes d'une molécule et paires d'électrons entre les atomes
- composé covalent
- (également un composé moléculaire) composé de molécules formées par des atomes de deux éléments différents ou plus
- liaison ionique
- forces d'attraction électrostatiques entre les ions de charge opposée d'un composé ionique
- composé ionique
- composé composé de cations et d'anions combinés dans des rapports, produisant une substance électriquement neutre
- composé moléculaire
- (également un composé covalent) composé de molécules formées par des atomes de deux éléments différents ou plus
- ion monatomique
- ion composé d'un seul atome
- ion polyatomique
- ion composé de plus d'un atome
- oxyanion
- anion polyatomique composé d'un atome central lié à des atomes d'oxygène


