17.1: 病毒
- Page ID
- 198917
没有人确切知道病毒何时出现或来自何处,因为病毒不会留下化石等历史足迹。 现代病毒被认为是沿着各自进化路径从各种来源提取的点点滴的核酸的马赛克。 病毒是脱细胞、寄生的实体,由于不被认为是活的,因此不归入任何结构域。 它们没有质膜、内部细胞器或代谢过程,也不会分裂。 相反,它们感染宿主细胞,并利用宿主的复制过程产生后代病毒颗粒。 病毒感染所有形式的生物,包括细菌、古细菌、真菌、植物和动物。 生物会生长、代谢和繁殖。 病毒会复制,但要做到这一点,它们完全依赖宿主细胞。 它们不会代谢或生长,而是以成熟的形式组装而成。

病毒是多种多样的。 它们的结构、复制方法、靶宿主甚至宿主细胞各不相同。 尽管大多数生物多样性可以通过进化史来理解,例如物种如何适应条件和环境,但有关病毒起源和进化的许多信息仍然未知。
病毒如何复制
病毒是在开发出一种名为Chamberland-Pasteur过滤器的瓷过滤器之后首次发现的,该过滤器可以从任何液体样本中去除显微镜下可见的所有细菌。 1886年,阿道夫·迈耶(Adolph Meyer)证明,一种烟草植物病,即烟草花叶病,可以通过液体植物提取物从患病植物转移到健康植物。 1892年,德米特里·伊万诺夫斯基表明,即使张伯兰-巴斯德过滤器从提取物中去除了所有活细菌,这种疾病仍可能以这种方式传播。 尽管如此,许多年后才证明这些 “可过滤” 的传染病原体不仅是非常小的细菌,而且是一种新型的微小致病颗粒。
病毒体,单一病毒颗粒,非常小,大约 20—250 纳米(1 纳米 = 1/1,000,000 mm)。 这些单独的病毒颗粒是宿主细胞外病毒的传染形式。 与细菌(大约大100倍)不同,除了痘病毒家族的一些大型病毒体外,我们无法用光学显微镜看到病毒(图\(\PageIndex{2}\))。
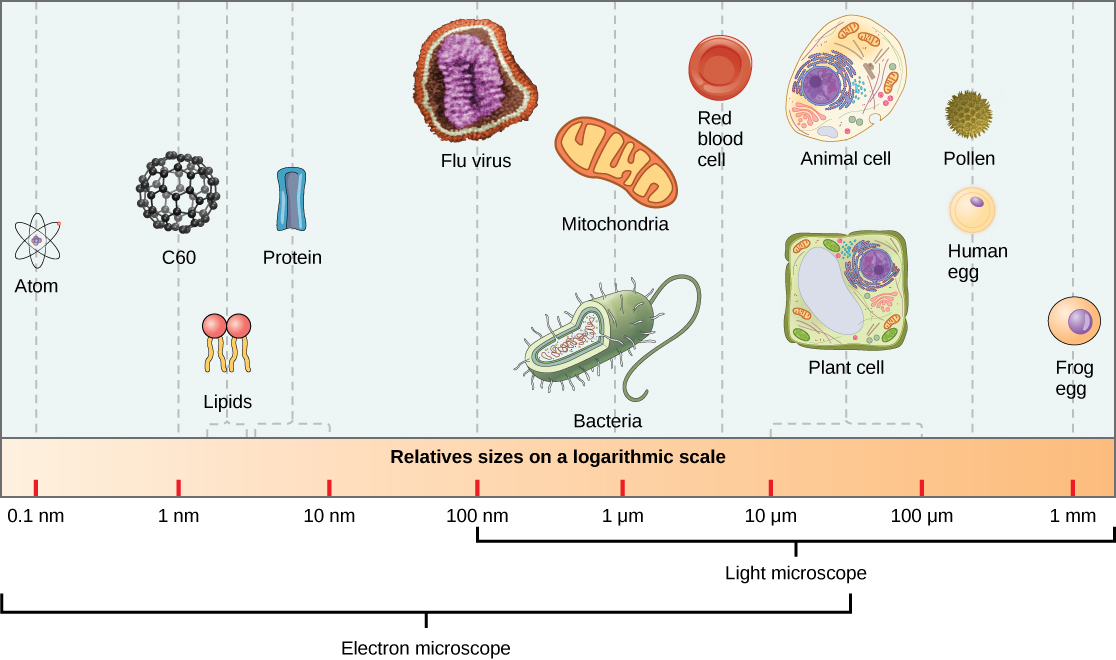
直到 20 世纪 40 年代电子显微镜的开发后,科学家们才第一次很好地了解了烟草花叶病毒(图\(\PageIndex{1}\))和其他病毒的结构。 病毒体的表面结构可以通过扫描和透射电子显微镜观察,而病毒的内部结构只能在透射电子显微镜的图像中观察(图\(\PageIndex{3}\))。
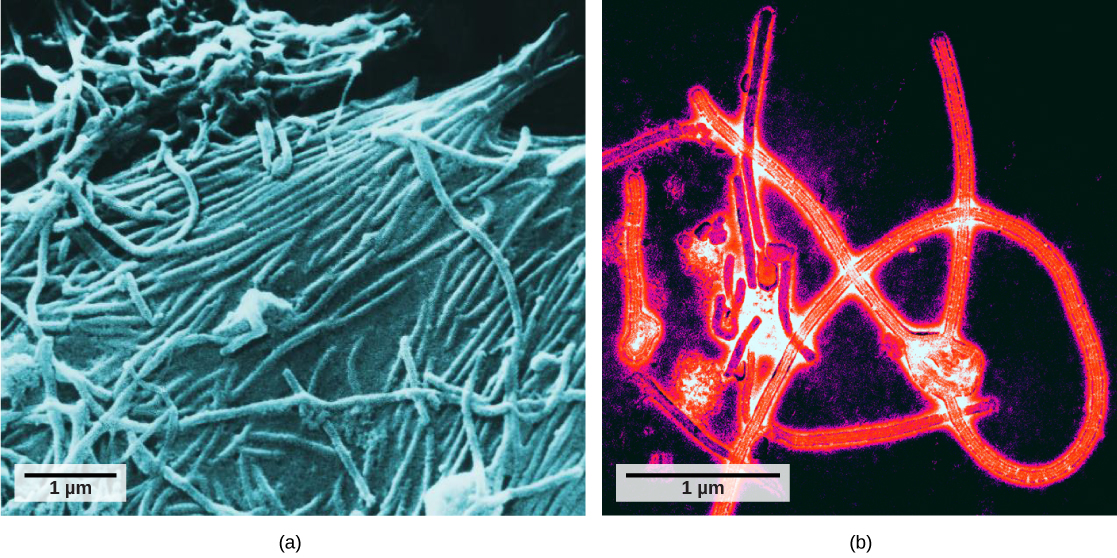
这项技术的使用使人们得以发现各种活生物体的许多病毒。 它们最初是按共同形态分组的,即它们的大小、形状和与众不同的结构。 后来,根据病毒所含核酸的类型(DNA或RNA)以及它们的核酸是单链还是双链对病毒组进行了分类。 最近,病毒复制周期的分子分析进一步完善了其分类。
病毒体由核酸核心、外部蛋白质涂层组成,有时还包括由源自宿主细胞的蛋白质和磷脂膜构成的外包膜。 病毒家族成员之间最明显的区别是它们的形态,这种形态非常多样化。 病毒复杂性的一个有趣特征是,宿主的复杂性与病毒体的复杂性无关。 在噬菌体中观察到一些最复杂的病毒体结构,噬菌体是感染最简单的活生物体细菌的病毒。
病毒有多种形状和大小,但每个病毒家族的形状和大小都是一致且不同的(图\(\PageIndex{4}\))。 所有病毒体都有一个核酸基因组,该基因组被一层称为衣壳的保护层所覆盖。 衣壳由称为衣壳的蛋白质亚基组成。 有些病毒衣壳是简单的多面体 “球体”,而另一些则在结构上相当复杂。 一些病毒衣壳周围的外部结构称为病毒包膜。 所有病毒都使用某种糖蛋白将细胞上称为病毒受体的分子附着在宿主细胞上。 病毒利用这些细胞表面分子,细胞将其用于其他目的,作为识别和感染特定细胞类型的一种方式。 例如,麻疹病毒在人体中使用一种细胞表面糖蛋白,这种糖蛋白通常在免疫反应中起作用,也可能在受精时发生精卵相互作用。 附着是病毒以后穿透细胞膜、注入病毒基因组并在细胞内完成复制的必要条件。
感染大肠杆菌的 T4 噬菌体是已知的最复杂的病毒体之一;T4 具有病毒用来附着在宿主细胞上的蛋白质尾部结构和存放其 DNA 的头部结构。
腺病毒是一种导致人类呼吸道疾病的非包膜动物病毒,它利用从其胶囊中伸出的蛋白质尖刺附着在宿主细胞上。 非包膜病毒还包括导致脊髓灰质炎(脊髓灰质炎病毒)、足底疣(乳头瘤病毒)和甲型肝炎(甲型肝炎病毒)的病毒。 非包膜病毒往往更强大,更有可能在恶劣的条件(例如肠道)下存活。
像艾滋病(获得性免疫缺陷综合征)的病原体 HIV(人类免疫缺陷病毒)这样的包膜病毒由核酸(HIV 为 RNA)和被磷脂双层包膜及其相关蛋白包围的衣壳蛋白组成(图\(\PageIndex{4}\))。 水痘、流感和腮腺炎就是由带有包膜的病毒引起的疾病的例子。 由于包膜的脆弱性,非包膜病毒比包膜病毒更能抵抗温度、pH 值和某些消毒剂的变化。
总体而言,病毒体的形状以及是否存在包膜几乎无法告诉我们病毒可能导致的疾病或它们可能感染哪些物种,但仍然是开始病毒分类的有用手段。
艺术连接
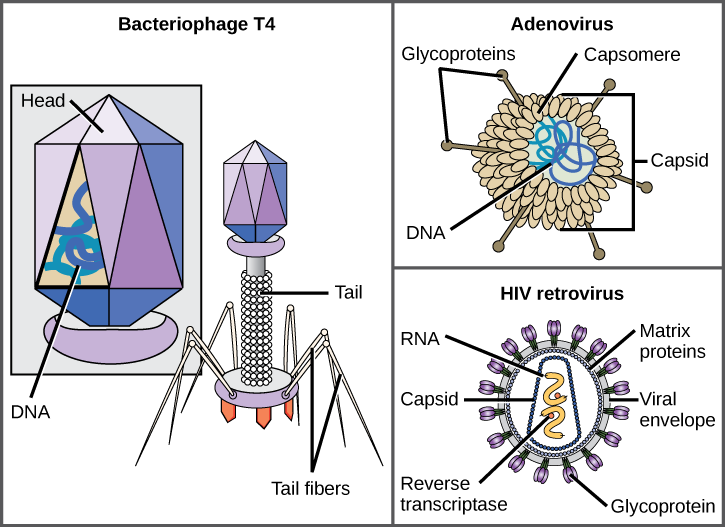
以下关于病毒结构的陈述中哪一项是正确的?
- 所有病毒都被包裹在病毒膜中。
- capsomere 由称为衣壳的小蛋白质亚基组成。
- DNA是所有病毒中的遗传物质。
- 糖蛋白帮助病毒附着在宿主细胞上。
与所有使用DNA作为遗传物质的活生物不同,病毒可能使用DNA或RNA作为其遗传物质。 病毒核心包含病毒的基因组或总遗传含量。 与细菌或真核生物相比,病毒基因组往往很小,仅包含编码病毒无法从宿主细胞获得的蛋白质的基因。 这种遗传物质可以是单链或双链。 它也可以是线性的或圆形的。 虽然大多数病毒都含有单片核酸,但其他病毒的基因组由多个片段组成。
DNA 病毒有一个 DNA 核心。 病毒 DNA 引导宿主细胞的复制蛋白合成病毒基因组的新拷贝,并将该基因组转录并转化为病毒蛋白。 DNA病毒会导致人类疾病,例如水痘、乙型肝炎以及一些性病,例如疱疹和尖锐湿疣。
RNA 病毒的核心中仅含有 RNA。 为了在宿主细胞中复制它们的基因组,RNA病毒的基因组对宿主细胞中找不到的酶进行编码。 RNA 聚合酶不如 DNA 聚合酶稳定,在转录过程中经常会出错。 因此,RNA病毒中的突变和核苷酸序列的变化比在DNA病毒中更频繁地发生。 这导致了RNA病毒更快的进化和变化。 例如,流感是一种RNA病毒这一事实是每年需要新的流感疫苗的原因之一。 由RNA病毒引起的人类疾病包括丙型肝炎、麻疹和狂犬病。
病毒可以看作是专性细胞内寄生虫。 病毒必须附着在活细胞上,被带入活细胞,制造其蛋白质并复制其基因组,并找到逃离细胞的方法,这样病毒才能感染其他细胞,最终感染其他个体。 病毒只能感染某些种类的宿主,只能感染该宿主内的某些细胞。 这种特异性的分子基础是,必须在宿主细胞表面找到一种特定的表面分子,即病毒受体,才能附着病毒。 此外,基于差异基因表达的不同细胞类型的代谢差异可能是病毒可能用来复制细胞的一个因素。 细胞必须制造出病毒所需的物质,例如病毒基因组本身没有基因的酶,否则病毒将无法使用该细胞复制。
病毒感染步骤
病毒必须 “接管” 细胞才能复制。 病毒复制周期可以在宿主细胞中产生显著的生化和结构变化,从而可能导致细胞损伤。 这些变化被称为细胞病变效应,可以改变细胞功能,甚至破坏细胞。 一些受感染的细胞,例如感染普通感冒病毒(鼻病毒)的细胞,会因裂解(破裂)或凋亡(程序性细胞死亡或 “细胞自杀”)而死亡,同时释放出所有后代病毒体。 病毒性疾病的症状源于对病毒的免疫反应(试图控制和消除体内病毒)和病毒造成的细胞损伤。 许多动物病毒,例如HIV(人类免疫缺陷病毒),通过一种称为萌芽的过程离开免疫系统的受感染细胞,在这种过程中,病毒体会单独离开细胞。 在萌芽过程中,细胞不会发生裂解,也不会立即被杀死。 但是,HIV感染的细胞受到的损害可能使这些细胞无法发挥免疫介质的作用,尽管这些细胞可以存活一段时间。 大多数生产性病毒感染在病毒复制周期中遵循相似的步骤:附着、穿透、脱皮、复制、组装和释放。
病毒通过衣壳中的附着蛋白或包膜中嵌入的蛋白质附着在宿主细胞膜上的特定受体位点。 附着是特异性的,通常病毒只会附着在一个或几个物种的细胞上,并且只会附着在具有适当受体的物种中的某些细胞类型上。
概念在行动
观看此视频,直观地解释流感是如何攻击人体的。
与动物病毒不同,噬菌体的核酸被裸体注射到宿主细胞中,将衣壳留在细胞外。 动植物病毒可以通过内吞作用进入细胞,在这种作用中,细胞膜包围并吞没整个病毒。 当病毒包膜与细胞膜直接融合时,一些包膜病毒会进入细胞。 一旦进入细胞,病毒衣壳就会降解,病毒核酸被释放,然后可用于复制和转录。
复制机制取决于病毒基因组。 DNA 病毒通常使用宿主细胞蛋白和酶来制造额外的 DNA,用于复制基因组或转录为信使 RNA (mRNA),然后用于蛋白质合成。 RNA 病毒,例如流感病毒,通常使用 RNA 核心作为合成病毒基因组 RNA 和 mRNA 的模板。 病毒 mRNA 被转化为病毒酶和衣壳蛋白,以组装新的病毒体(图\(\PageIndex{5}\))。 当然,这种模式也有例外。 如果宿主细胞不能提供病毒复制所需的酶,则病毒基因为直接合成缺失的蛋白质提供信息。 逆转录病毒,例如HIV,具有RNA基因组,必须对其进行逆转录才能产生DNA,然后将其插入宿主的DNA中。 为了将 RNA 转化为 DNA,逆转录病毒包含编码病毒特异性酶逆转录酶的基因,该酶将 RNA 模板转录为 DNA。 HIV自身会产生一些在宿主中找不到的酶,这一事实使研究人员得以开发出抑制这些酶的药物。 这些药物,包括逆转录酶抑制剂 AZT,通过在不影响宿主新陈代谢的情况下降低酶的活性来抑制 HIV 复制。
病毒复制的最后阶段是将新的病毒体释放到宿主生物体中,在那里它们能够感染相邻的细胞并重复复制周期。 有些病毒是在宿主细胞死亡时释放出来的,而其他病毒可以通过在膜中萌芽而离开受感染的细胞,而不会直接杀死细胞。
艺术连接
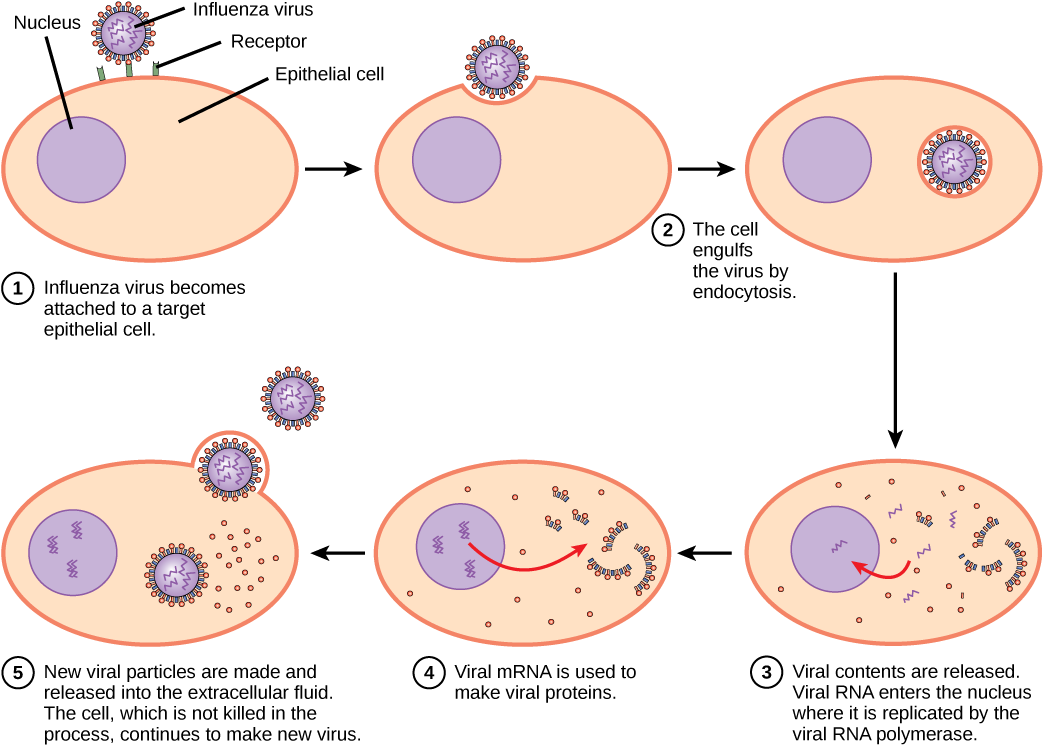
流感病毒包装在病毒包膜中,该包膜与质膜融合。 这样,病毒可以在不杀死宿主细胞的情况下离开宿主细胞。 病毒通过保持宿主细胞的存活会获得什么好处?
概念在行动
单击此病毒教程以识别结构、传播模式、复制等。
病毒与疾病
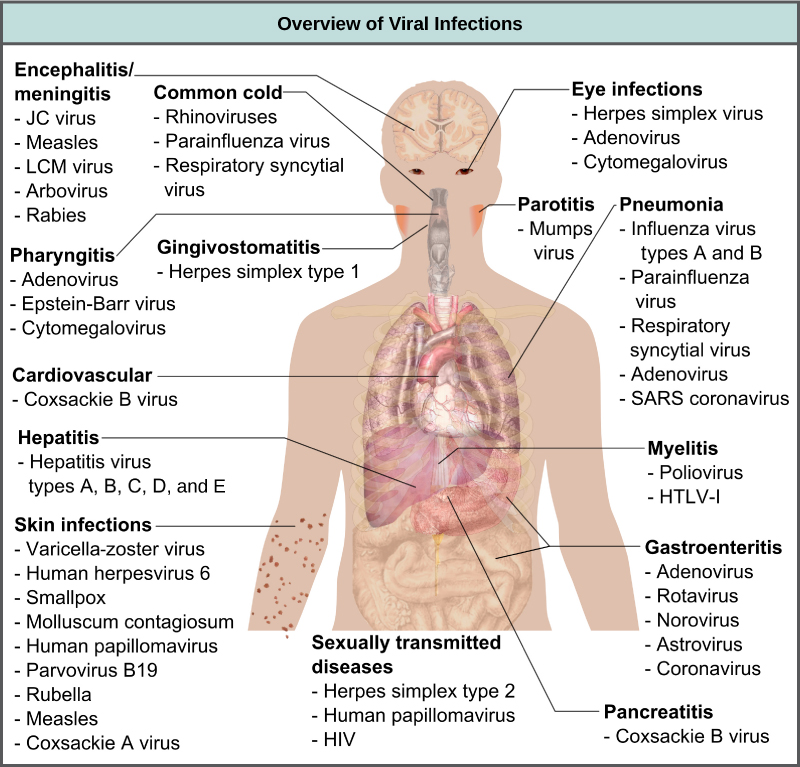
病毒在包括人类在内的动物身上引起各种疾病,从普通感冒到脑膜炎等潜在的致命疾病不等(图\(\PageIndex{6}\))。 这些疾病可以通过抗病毒药物或疫苗治疗,但是有些病毒,例如艾滋病毒,能够避免免疫反应和变异,从而对抗病毒药物产生耐药性。
预防疫苗
尽管我们的有效抗病毒药物(例如用于治疗HIV和流感的药物)的数量确实有限,但控制病毒性疾病的主要方法是接种疫苗,其目的是通过增强对病毒或病毒家族的免疫力来预防疫情。 疫苗可以使用弱化的活病毒、杀死的病毒或病毒的分子亚单位来制备。 通常,活病毒可以提高免疫力,但有可能以较低的频率引起疾病。 杀死的病毒疫苗和亚单位病毒都不会引起疾病,但通常会导致免疫效果较差或持续时间较长。
实验室设计的弱化活病毒疫苗几乎不会对接受者造成任何症状,同时使他们免疫未来的感染。 脊髓灰质炎是一种代表疫苗使用里程碑的疾病。 美国在20世纪50年代(杀死疫苗)和1960年代(活疫苗)的大规模免疫运动基本上根除了这种疾病,这种疾病导致儿童肌肉麻痹,并在区域疫情发生时引起了普通民众的恐惧。 脊髓灰质炎疫苗的成功为常规发放针对麻疹、腮腺炎、风疹、水痘和其他疾病的儿童疫苗铺平了道路。
活疫苗通常是通过在实验室的组织中或在与病毒在宿主中习惯的温度不同的温度下培养 “野生型”(致病)病毒来减弱(减弱)来制造的。 例如,病毒可能在试管中的细胞、鸟类胚胎或活体动物中生长。 对这些新细胞或温度的适应会诱发病毒基因组的突变,使它们在实验室中生长得更好,同时抑制它们在重新引入宿主中发现的疾病时引起疾病的能力。 因此,这些减毒的病毒仍然会引起感染,但它们的生长效果不佳,这使得免疫反应能够及时发展以预防重大疾病。 活疫苗通常比杀死的疫苗更有效,使用活疫苗的危险在于,这些病毒因背部突变而恢复致病形式的风险很低但很大。 当疫苗在宿主中发生突变以使其重新适应宿主并可能再次导致疾病,然后在疫情中传播给其他人时,就会发生背部突变。 这种情况最近在2007年发生在尼日利亚,脊髓灰质炎疫苗的突变导致了该国脊髓灰质炎的流行。
一些疫苗仍在持续开发中,因为与其他病毒或宿主细胞相比,某些病毒(例如流感和艾滋病毒)具有较高的突变率。 对于流感,表面分子基因的突变有助于病毒逃避在上一个流感季节可能获得的保护性免疫力,这使得个人每年都必须接种疫苗。 其他病毒,例如导致儿童疾病麻疹、腮腺炎和风疹的病毒,变异很小,以至于年复一年地使用相同的疫苗。
用于治疗的疫苗和抗病毒药物
在某些情况下,疫苗可用于治疗活动性病毒感染。 就狂犬病而言,狂犬病是一种通过感染狂犬病病毒的动物的唾液传播的致命神经系统疾病,该疾病从动物咬伤到进入中枢神经系统的进展可能持续两周或更长时间。 这足以让怀疑被狂犬病动物咬伤的人接种疫苗,疫苗接种增强的免疫反应足以防止病毒进入神经组织。 因此,该疾病的致命神经系统后果得以避免,个人只需要从感染的叮咬中恢复过来即可。 这种方法也被用于治疗埃博拉,埃博拉是影响人类的速度最快、最致命的病毒之一,尽管通常感染的人群有限。 埃博拉也是导致大猩猩死亡的主要原因。 这种病毒由蝙蝠和大猿传播,可在两周内导致70-90%的感染者死亡。 使用新开发的增强免疫反应的疫苗,有希望受影响个体的免疫系统能够更好地控制病毒,从而有可能降低死亡率。
治疗病毒感染的另一种方法是使用抗病毒药物。 这些药物治疗病毒性疾病的能力通常有限,但已被用于控制和减轻各种病毒性疾病的症状。 对于大多数病毒,这些药物通过阻断一种或多种蛋白质的作用来抑制病毒。 重要的是,靶向蛋白必须由病毒基因编码,并且这些分子不存在于健康的宿主细胞中。 通过这种方式,可以在不损害宿主的情况下抑制病毒的生长。 有大量的抗病毒药物可用于治疗感染,其中一些是针对特定病毒的特异性的,而另一些则可以影响多种病毒。
已经开发出用于治疗生殖器疱疹(II 型单纯疱疹)和流感的抗病毒药物。 对于生殖器疱疹,诸如阿昔洛韦之类的药物可以减少活动性病毒性疾病发作的次数和持续时间,在此期间,患者的皮肤细胞中出现病毒性病变。 由于病毒终身潜伏在人体的神经组织中,这种药物不能治愈,但可以使疾病的症状更易于控制。 对于流感,像达菲这样的药物可以将 “流感” 症状的持续时间缩短一到两天,但这种药物并不能完全预防症状。 其他抗病毒药物,例如利巴韦林,已被用于治疗各种病毒感染。
到目前为止,抗病毒药物最成功的用途是治疗逆转录病毒HIV,这种疾病如果不加以治疗,通常会在感染后的10-12年内致命。 抗HIV药物已经能够控制病毒的复制,以至于接受这些药物的人的存活时间比未经治疗的人长得多。
抗HIV药物在HIV复制周期的许多不同阶段抑制病毒复制。 已经开发出抑制HIV病毒包膜与宿主细胞质膜(融合抑制剂)融合、将HIV病毒基因组转化为双链DNA(逆转录酶抑制剂)、病毒DNA整合到宿主基因组(整合酶抑制剂)的药物病毒蛋白(蛋白酶抑制剂)的加工。
当这些药物中的任何一种单独使用时,病毒的高突变率使病毒能够迅速产生对药物的耐药性。 HIV治疗的突破是开发了高活性抗逆转录病毒疗法(HAART),该疗法涉及不同药物的混合物,有时被称为 “鸡尾酒” 药物。 通过在病毒复制周期的不同阶段攻击病毒,病毒很难同时对多种药物产生耐药性。 尽管如此,即使使用联合HAART疗法,人们仍然担心,随着时间的推移,该病毒会对这种疗法产生抗药性。 因此,正在不断开发新的抗艾滋病毒药物,希望继续与这种高度致命的病毒作斗争。
摘要
病毒是脱细胞实体,通常只能用电子显微镜看到。 它们的基因组含有DNA或RNA,它们使用宿主细胞的复制蛋白进行复制。 病毒多种多样,感染古细菌、细菌、真菌、植物和动物。 病毒由核酸核心组成,周围环绕着带有或没有外部脂质包膜的蛋白质衣壳。
活细胞内的病毒复制总是会导致细胞发生变化,有时会导致细胞死亡,有时会慢慢杀死受感染的细胞。 病毒复制周期有六个基本阶段:附着、渗透、脱皮、复制、组装和释放。 病毒感染可能是生产性的,会产生新的病毒体,也可以是非生产性的,这意味着病毒会留在细胞内而不产生新的病毒体。
病毒在人类中引起各种疾病。 这些疾病中有许多可以通过使用病毒疫苗来预防,病毒疫苗可以刺激针对病毒的保护性免疫而不会引起重大疾病。 病毒疫苗也可用于活性病毒感染,增强免疫系统控制或消灭病毒的能力。 靶向病毒基因的酶和其他蛋白质产物的抗病毒药物已经开发和使用,但成功参差不齐。 已使用抗HIV药物的组合来有效控制病毒,从而延长感染者的寿命。
艺术联系
图\(\PageIndex{4}\):以下关于病毒结构的陈述中哪一项是正确的?
答:所有病毒都被包裹在病毒膜中。
B. capsomere 由称为衣壳的小蛋白质亚基组成。
C. DNA是所有病毒的遗传物质。
D. 糖蛋白帮助病毒附着在宿主细胞上。
- 回答
-
D
图\(\PageIndex{5}\):流感病毒包装在病毒包膜中,该包膜与质膜融合。 这样,病毒可以在不杀死宿主细胞的情况下离开宿主细胞。 病毒通过保持宿主细胞的存活会获得什么好处?
- 回答
-
宿主细胞可以继续制造新的病毒颗粒。
词汇表
- 脱细胞的
- 缺少细胞
- 细胞凋亡
- 由细胞自身内部机制的诱导引起的细胞死亡,要么是多细胞生物发育的自然步骤,要么是其他环境因素,例如来自免疫系统细胞的信号
- 衰减
- 疫苗研发过程中病毒的减弱
- 衣壳
- 病毒核心的蛋白质涂层
- 细胞病变
- 造成细胞损伤
- 糖蛋白
- 附有碳水化合物分子的蛋白质分子
- 疫苗
- 病毒成分、病毒或其他产生免疫反应的因子的弱化溶液
- 病毒体
- 宿主细胞外的单个病毒颗粒
- 病毒包膜
- 一种包裹某些病毒的脂质双层


