10.3: 基因组学和蛋白质组学
- Page ID
- 199014
核酸的研究始于DNA的发现,后来发展到基因和小片段的研究,现在已发展到基因组学领域。 基因组学是对整个基因组的研究,包括全套基因、其核苷酸序列和组织以及它们在一个物种内部以及与其他物种的相互作用。 DNA测序技术使基因组学的进步成为可能。 正如信息技术催生了谷歌地图,它使我们能够获得有关全球各地的详细信息一样,基因组信息也被用来创建不同生物的DNA的相似图谱。
绘制基因组图
基因组映射是寻找每条染色体上基因位置的过程。 创建的地图与我们用来在街道上导航的地图相当。 遗传图谱是列出基因及其在染色体上的位置的插图。 遗传图谱提供了大局(类似于州际公路地图),并使用遗传标记(类似于地标)。 遗传标记是染色体上显示出与感兴趣特征的遗传联系的基因或序列。 遗传标记往往与目标基因一起遗传,衡量它们之间距离的一个标准是减数分裂期间的重组频率。 早期的遗传学家称之为这种关联分析。
物理图谱显示了染色体较小区域的私密细节(类似于详细的路线图)(图\(\PageIndex{1}\))。 物理图谱以核苷酸表示基因或遗传标记之间的物理距离。 建立完整的基因组图谱需要遗传连锁图谱和物理图谱。 拥有完整的基因组图谱使研究人员更容易研究单个基因。 人类基因组图谱帮助研究人员努力识别与癌症、心脏病和囊性纤维化等疾病有关的人类致病基因。 此外,基因组映射可用于帮助识别具有有益特征的生物,例如能够清除污染物甚至防止污染的微生物。 涉及植物基因组图谱的研究可能会产生提高作物产量的方法,或者开发出更能适应气候变化的植物。
![该图显示了一条带状带的人类染色体,上面有 Giemsa 染色体。 表带标有 Xp,短臂上标有数字,Xq 上标有数字,长臂上标有数字。 在一些波段中发现了某些基因。 右侧标有这些基因:范可尼贫血 B、Wiskott-Aldrich 综合征、Pelizaeus-Merzbacher 病、脆性 X 综合征和 G6PD 缺乏 [0]。](https://bio.libretexts.org/@api/deki/files/9384/Figure_10_03_01.jpg)
遗传图谱提供轮廓,物理图谱提供细节。 不难理解为什么这两种类型的基因组映射技术对于展示大局都很重要。 从每种技术中获得的信息组合用于研究基因组。 基因组映射用于研究的不同模型生物。 基因组映射仍在进行中,随着更先进技术的开发,预计会有更多的进步。 基因组映射类似于使用每条可用数据完成一个复杂的难题。 世界各地实验室生成的测绘信息被输入中央数据库,例如国家生物技术信息中心(NCBI)。 正在努力使研究人员和公众更容易获得信息。 正如我们使用全球定位系统而不是纸质地图在道路上导航一样,NCBI 允许我们使用基因组查看器工具来简化数据挖掘过程。
概念在行动

在线孟德尔人类遗产(OMIM)是一个可搜索的人类基因和遗传疾病的在线目录。 该网站显示了基因组图谱,还详细介绍了每种特征和疾病的历史和研究。 点击链接搜索特征(例如惯用手法)和遗传疾病(例如糖尿病)。
全基因组测序
尽管近年来医学取得了重大进展,但医生仍然对许多疾病感到困惑,研究人员正在使用全基因组测序来深入了解问题。 全基因组测序是确定整个基因组的DNA序列的过程。 当疾病的核心是遗传基础时,全基因组测序是一种暴力解决问题的方法。 现在有几个实验室提供对整个基因组进行测序、分析和解释的服务。
2010 年,全基因组测序被用来拯救一个小男孩,他的肠道里有多处神秘脓肿。 孩子做了几次结肠手术,都没有缓解。 最后,全基因组序列显示控制细胞凋亡(程序性细胞死亡)的途径存在缺陷。 骨髓移植被用来克服这种遗传疾病,从而治愈了这个男孩。 他是第一个使用全基因组测序成功诊断出来的人。
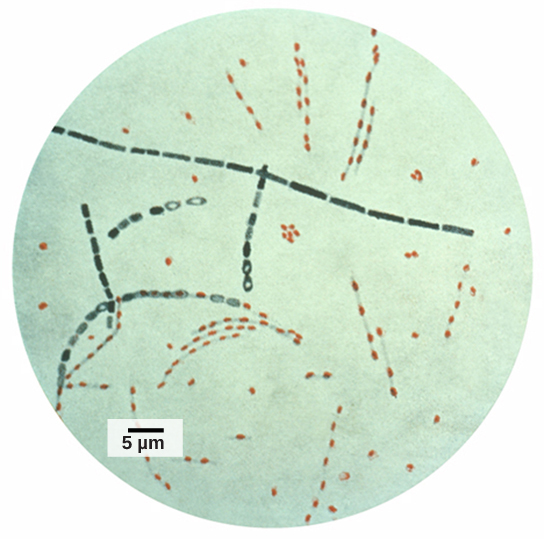
第一批要测序的基因组,例如属于病毒、细菌和酵母的基因组,在核苷酸数量方面要小于多细胞生物的基因组。 其他模型生物的基因组,例如老鼠(Mus musculus)、果蝇(果蝇 m elanogaster)和线虫(Caenorhabditis Elegans)现已为人所知。 大量的基础研究是在模型生物中进行的,因为这些信息可以应用于其他生物。 模型生物是一种作为模型进行研究的物种,以了解模型生物可以代表的其他物种中的生物过程。 例如,果蝇能够像人类一样代谢酒精,因此已经在果蝇中研究了影响酒精敏感性的基因,以了解人类对酒精敏感度的变化。 对整个基因组进行测序有助于这些模型生物的研究工作(图\(\PageIndex{2}\))。

第一个人类基因组序列于 2003 年发布。 已测序的全基因组数量稳步增加,现在包括数百个物种和数千个单独的人类基因组。
应用基因组学
DNA测序和全基因组测序项目的引入,特别是人类基因组计划,扩大了DNA序列信息的适用性。 基因组学现在被应用于各种领域,例如宏基因组学、药物基因组学和线粒体基因组学。 基因组学最常见的应用是了解和寻找疾病的治疗方法。
预测个人层面的疾病风险
预测疾病风险包括通过个体层面的基因组分析筛选和识别当前健康的个体。 在疾病发作之前,可以建议通过改变生活方式和药物进行干预。 但是,当问题是由单一基因突变引起时,这种方法最适用。 此类缺陷仅占发达国家发现的疾病的5%左右。 大多数常见疾病,例如心脏病,都是多因子或多基因的,这是指由两个或多个基因决定的表型特征以及饮食等环境因素。 2010年4月,斯坦福大学的科学家发表了对一个健康个体的基因组分析(斯坦福大学科学家斯蒂芬·奎克,他的基因组测序);该分析预测了他患各种疾病的倾向。 进行了风险评估,以分析Quake在55种不同疾病中的风险百分比。 发现了一种罕见的基因突变,表明他有突然心脏病发作的风险。 据预测,他患前列腺癌的风险为23%,患阿尔茨海默氏病的风险为1.4%。 科学家们使用数据库和几份出版物来分析基因组数据。 尽管基因组测序变得越来越便宜,分析工具也变得越来越可靠,但在人群层面上围绕基因组分析的伦理问题仍有待解决。 例如,此类数据是否可以合法地用于或多或少地收取保险费或影响信用评级?
全基因组关联研究
自2005年以来,有可能进行一种称为全基因组关联研究(GWAS)的研究。 GWAS 是一种识别个体之间可能参与致病的单核苷酸多态性 (SNP) 差异的方法。 该方法特别适用于可能受到整个基因组中一个或多个遗传变化影响的疾病。 使用家族史信息很难识别与这种疾病有关的基因。 GWAS 方法依赖于自 2002 年以来一直在开发的名为 “国际 HapMap 项目” 的遗传数据库。 HapMap 项目对来自世界各地的数百个个体的基因组进行了测序,并确定了单核苷酸多态性群体。 这些组包括染色体上彼此靠近的单核苷酸多态性,因此它们往往通过重组保持在一起。 该组团结在一起的事实意味着识别该组中的所有单核苷酸多态性只需要识别一个标志物单核苷酸多态性。 已鉴定出数百万个单核苷酸多态性,但是在其他尚未进行完整基因组测序的个体中鉴定它们要容易得多,因为只需要识别标志物单核苷酸多态性。
在 GWAS 的常见设计中,选择了两组个体;一组患有这种疾病,另一组没有。 每组中的个体在其他特征上进行匹配,以减少导致两组之间差异的混杂变量的影响。 例如,基因型可能有所不同,因为这两组主要来自世界的不同地方。 一旦选择了这些个体,并且他们的人数通常为一千或更多以供研究起作用,就会获得他们的DNA样本。 使用自动化系统对DNA进行分析,以确定两组之间特定单核苷酸多态性百分比的巨大差异。 该研究通常会检查DNA中一百万个或更多的单核苷酸多态性。 GWAS 的结果可以通过两种方式使用:遗传差异可用作未确诊个体对疾病易感性的标志;鉴定的特定基因可以作为研究该疾病的分子途径和潜在疗法的靶标。 发现与疾病的基因关联的一个分支是成立了提供所谓的 “个人基因组学” 的公司,这些公司将根据个人的单核苷酸多态性补体识别各种疾病的风险水平。 这些服务背后的科学存在争议。
由于 GWAS 寻找基因与疾病之间的关联,因此这些研究为其他病因研究提供了数据,而不是自己回答具体问题。 基因差异与疾病之间的关联并不一定意味着存在因果关系。 但是,一些研究提供了有关疾病遗传原因的有用信息。 例如,2005年的三项不同的研究确定了一种参与调节体内炎症的蛋白质的基因,该基因与一种称为年龄相关性黄斑变性的致病失明有关。 这为研究这种疾病的病因开辟了新的可能性。 已使用 GWAS 鉴定出大量与克罗恩病相关的基因,其中一些为该疾病的病因提出了新的假设机制。
药物基因组学
药物基因组学涉及根据来自个体基因组序列的信息评估药物的有效性和安全性。 个人基因组序列信息可用于根据个体患者的基因型开出最有效、毒性最小的药物。 研究基因表达的变化可以提供有关药物存在时基因转录谱的信息,这可以用作潜在毒性作用的早期指标。 例如,参与细胞生长和控制细胞死亡的基因在受到干扰时可能导致癌细胞的生长。 全基因组研究还可以帮助发现与药物毒性有关的新基因。 基因特征可能不完全准确,但在病理症状出现之前可以进一步检测。
宏基因组学
传统上,教授微生物学的观点是,最好在纯培养条件下研究微生物,这包括分离单一类型的细胞,然后在实验室培养。 由于微生物可以在几个小时内经历几代人,因此它们的基因表达谱很快就会适应新的实验室环境。 另一方面,许多物种不愿单独培养。 大多数微生物不是作为孤立的实体生活,而是生活在被称为生物膜的微生物群落中。 出于所有这些原因,纯培养并不总是研究微生物的最佳方法。 宏基因组学是对在环境利基中生长和相互作用的多个物种的集体基因组的研究。 宏基因组学可用于更快地识别新物种和分析污染物对环境的影响(图\(\PageIndex{3}\))。 宏基因组学技术现在也可以应用于高等真核生物群落,例如鱼类。
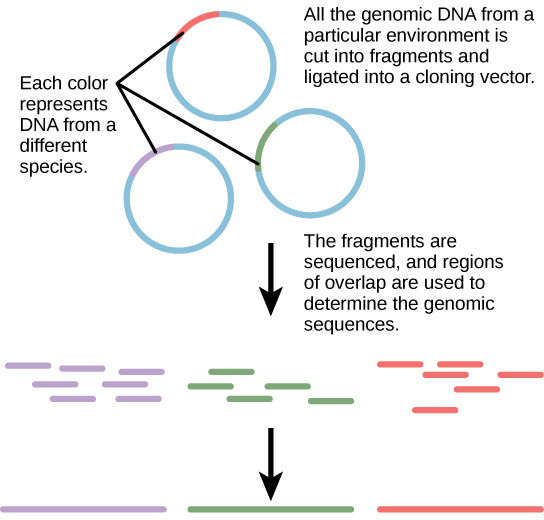
创造新的生物燃料
对微生物基因组学的了解被用来寻找更好的方法来利用藻类和蓝细菌中的生物燃料。 当今的主要燃料来源是煤炭、石油、木材和其他植物产品,例如乙醇。 尽管植物是可再生资源,但仍然需要寻找更多的替代可再生能源,以满足我们人口的能源需求。 微生物世界是编码新酶和产生新有机化合物的基因的最大资源之一,而且在很大程度上仍未开发。 这种丰富的遗传资源有可能提供新的生物燃料来源(图\(\PageIndex{4}\))。

线粒体基因组学
线粒体是含有自身DNA的细胞内细胞器。 线粒体DNA快速突变,通常用于研究进化关系。 使研究线粒体基因组变得有趣的另一个特征是,在大多数多细胞生物中,线粒体DNA是在受精过程中从母亲那里传递的。 因此,线粒体基因组学通常用于追踪家谱。
法医分析中的基因组学
从犯罪现场发现的脱氧核糖核酸样本中获得的信息和线索已被用作法庭案件的证据,遗传标记也被用于法医分析。 基因组分析在该领域也变得很有用。 2001 年,首次发布了基因组学在法医中的应用。 这是学术研究机构与联邦调查局的共同努力,旨在解决由美国邮政局运送的神秘炭疽病例(图\(\PageIndex{5}\))。 炭疽细菌被制成传染性粉末,并邮寄给新闻媒体和两名美国参议员。 粉末感染了打开或处理信件的行政人员和邮政工作人员。 五人死亡,17人因细菌而生病。 研究人员利用微生物基因组学确定所有邮件中都使用了特定的炭疽菌株;最终,该来源被追溯到马里兰州国家生物防御实验室的一位科学家。
农业中的基因组学
基因组学可以在一定程度上减少科学研究中涉及的试验和失败,从而提高农业作物产量的质量和数量(图\(\PageIndex{6}\))。 将性状与基因或基因特征联系起来有助于改善作物育种,从而产生具有最理想品质的杂种。 科学家使用基因组数据来确定理想的特征,然后将这些特征转移到不同的生物体中,以创建新的转基因生物,如前一个模块所述。 科学家们正在发现基因组学如何提高农业生产的质量和数量。 例如,科学家可以利用理想的特性来创造有用的产品或增强现有产品,例如使对干旱敏感的作物更耐旱季。

蛋白质组学
蛋白质是执行基因编码功能的基因的最终产物。 蛋白质由氨基酸组成,在细胞中起着重要作用。 所有酶(核酶除外)都是蛋白质,充当影响反应速率的催化剂。 蛋白质也是调节分子,有些是激素。 转运蛋白,例如血红蛋白,有助于将氧气输送到各个器官。 抵御外来颗粒的抗体也是蛋白质。 在患病状态下,由于遗传水平的变化或对特定蛋白质的直接影响,蛋白质功能可能会受到损害。
蛋白质组是由一种细胞类型产生的整套蛋白质。 蛋白质组可以利用基因组知识进行研究,因为基因编码 mRNA,而 mRNA 编码蛋白质。 对蛋白质组功能的研究称为蛋白质组学。 蛋白质组学是对基因组学的补充,在科学家想要检验他们基于基因的假设时很有用。 尽管多细胞生物体中的所有细胞都具有相同的基因集,但在不同组织中产生的蛋白质集是不同的,依赖于基因表达。 因此,基因组是恒定的,但蛋白质组各不相同,并且在生物体内是动态的。 此外,RNA可以交替拼接(剪切和粘贴以产生新的组合和新的蛋白质),许多蛋白质在翻译后会被修饰。 尽管基因组提供了蓝图,但最终的结构取决于几个因素,这些因素可能会改变生成蛋白质组的事件的进展。
正在研究患有特定疾病的患者的基因组和蛋白质组,以了解该疾病的遗传基础。 使用蛋白质组学方法研究的最突出的疾病是癌症(图\(\PageIndex{7}\))。 蛋白质组学方法被用来改善癌症的筛查和早期发现;这是通过鉴定其表达受疾病过程影响的蛋白质来实现的。 单个蛋白质被称为生物标志物,而一组表达水平改变的蛋白质称为蛋白质特征。 为了使生物标志物或蛋白质特征可用作癌症早期筛查和检测的候选物,必须将其分泌在汗液、血液或尿液等体液中,这样才能以非侵入性的方式进行大规模筛查。 目前使用生物标志物早期发现癌症的问题是假阴性结果的发生率很高。 假阴性结果是应为阳性的阴性测试结果。 换句话说,许多癌症病例未被发现,这使得生物标志物不可靠。 癌症检测中使用的蛋白质生物标志物的一些例子包括用于卵巢癌的 CA-125 和用于前列腺癌的 PSA。 在检测癌细胞方面,蛋白质特征可能比生物标志物更可靠。 蛋白质组学还被用于制定个性化治疗计划,其中包括预测一个人是否会对特定药物产生反应以及该个人可能产生的副作用。 蛋白质组学还被用来预测疾病复发的可能性。

国家癌症研究所制定了改善癌症检测和治疗的计划。 癌症临床蛋白质组学技术和早期检测研究网络旨在识别不同类型癌症特有的蛋白质特征。 生物医学蛋白质组学计划旨在识别蛋白质特征并为癌症患者设计有效的疗法。
摘要
基因组映射类似于用来自世界各地实验室的信息来解决一个庞大而复杂的难题。 遗传图谱概述了基因在基因组中的位置,它们根据减数分裂期间的重组频率估计基因和遗传标记之间的距离。 物理图谱提供有关基因之间物理距离的详细信息。 最详细的信息可通过序列映射获得。 将来自所有测绘和测序来源的信息结合起来,研究整个基因组。
全基因组测序是治疗遗传疾病的最新可用资源。 一些医生正在使用全基因组测序来挽救生命。 基因组学有许多工业应用,包括生物燃料开发、农业、制药和污染控制。
想象力是基因组学应用的唯一障碍。 基因组学被应用于大多数生物学领域;它可以用于个体化医学、预测个人层面的疾病风险、在进行临床试验之前研究药物相互作用,以及研究环境中而不是实验室中的微生物。 它还被应用于生产新的生物燃料、使用线粒体的系谱评估、法医学的进步以及农业的改善。
蛋白质组学是对特定类型细胞在特定环境条件下表达的整套蛋白质的研究。 在多细胞生物体中,不同的细胞类型会有不同的蛋白质组,这些蛋白质组会随着环境的变化而变化。 与基因组不同,蛋白质组是动态的,并且不断变化,这使得它比仅了解基因组更复杂,更有用。
词汇表
- 生物标志物
- 一种在患病状态下独一无二产生的单体蛋白质
- 遗传图谱
- 基于标记物之间的重组频率概述基因及其在染色体上的位置
- 基因组学
- 研究整个基因组,包括全套基因、其核苷酸序列和组织以及它们在一个物种内部和与其他物种的相互作用
- 宏基因组学
- 研究在环境利基中生长和相互作用的多个物种的集体基因组
- 模型生物
- 该物种经过研究并用作模型以了解模型生物所代表的其他物种的生物过程
- 药物基因组学
- 药物与基因组或蛋白质组相互作用的研究;也称为毒物基因组学
- 物理地图
- 代表基因或遗传标记之间的物理距离
- 蛋白质特征
- 一组以特定病变组织中细胞为特征的过度表达或表达不足的蛋白质
- 蛋白质组学
- 蛋白质组功能研究
- 全基因组测序
- 确定整个基因组核苷酸序列的过程


