4.1: 能量和新陈代谢
- Page ID
- 199428
科学家使用生物能量学一词来描述通过生命系统(如细胞\(\PageIndex{1}\))的能量流的概念(图)。 诸如复杂分子的生成和分解之类的细胞过程是通过逐步化学反应发生的。 其中一些化学反应是自发的并释放能量,而另一些则需要能量才能进行。 正如生物必须持续消耗食物来补充能量供应一样,细胞也必须不断产生更多的能量来补充不断发生的许多需要能量的化学反应所消耗的能量。 细胞内部发生的所有化学反应,包括消耗或产生能量的化学反应,共同被称为细胞的新陈代谢。
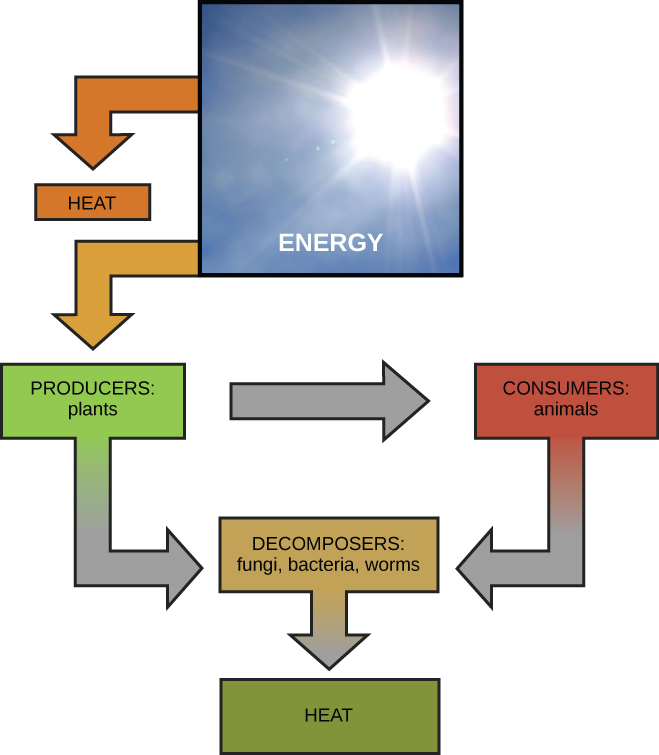
代谢途径
以糖的代谢为例。 这是使用和产生能量的众多细胞过程之一的典型例子。 生物消耗糖作为主要能量来源,因为糖分子的键中储存了大量的能量。 在大多数情况下,像植物这样的光合作用生物会产生这些糖。 在光合作用过程中,植物使用能量(最初来自阳光)将二氧化碳气体(CO 2)转化为糖分子(如葡萄糖:C 6 H 12 O 6)。 它们消耗二氧化碳并产生氧气作为废物。 这种反应总结为:
\[\ce{6CO2 + 6H2O -> C6H12O6 + 6O2}\nonumber\]
由于这个过程涉及合成能量储存分子,因此需要能量输入才能继续。 在光合作用的光反应中,能量由一种叫做三磷酸腺苷(ATP)的分子提供,它是所有细胞的主要能量货币。 就像美元被用作购买商品的货币一样,细胞使用ATP分子作为能量货币来立即发挥作用。 相比之下,葡萄糖等能量存储分子的消耗只是为了消耗能量而分解。 在需要氧气才能存活的细胞中收集糖分子能量的反应可以概括为与光合作用的逆向反应。 在这种反应中,氧气被消耗,二氧化碳作为废物被释放。 反应总结为:
\[\ce{C6H12O6 + 6O2 -> 6H2O + 6CO2}\nonumber\]
这两种反应都涉及许多步骤。
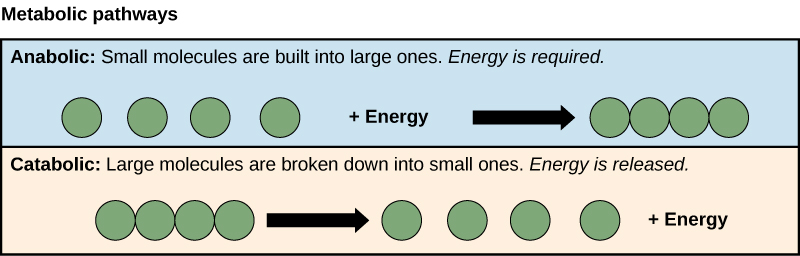
糖分子的制造和分解过程说明了代谢途径的两个例子。 代谢途径是一系列化学反应,它吸收起始分子,并通过一系列代谢中间体逐步对其进行修改,最终产生最终产物。 以糖代谢为例,第一种代谢途径从较小的分子中合成糖,而另一种途径将糖分解成较小的分子。 这两个相反的过程——第一个需要能量和第二个产生能量——分别被称为合成代谢途径(建筑聚合物)和分解代谢途径(将聚合物分解成单体)。 因此,新陈代谢由合成(合成代谢)和降解(分解代谢)组成(图\(\PageIndex{2}\))。
重要的是要知道,代谢途径的化学反应不是自行发生的。 每个反应步骤都由一种叫做酶的蛋白质促进或催化。 酶对于催化所有类型的生物反应都很重要,包括需要能量的生物反应和释放能量的反应。
能源
热力学是指研究涉及物理物质的能量和能量传递。 与特定能量传递案例相关的物质被称为系统,该物质之外的所有事物都称为周围环境。 例如,当在炉子上加热一壶水时,系统包括炉子、锅和水。 能量在系统内传输(在炉子、锅和水之间)。 有两种类型的系统:开放式和封闭式。 在开放系统中,能量可以与周围环境交换。 炉灶系统处于打开状态,因为热量可能会流失到空气中。 封闭的系统无法与周围环境交换能量。
生物是开放系统。 当它们使用来自太阳的能量进行光合作用或消耗能量储存分子并通过工作和释放热量向环境释放能量时,它们与周围环境之间会交换能量。 像物理世界中的所有事物一样,能量受物理定律的约束。 热力学定律控制着宇宙中所有系统内部和之间的能量传输。
一般而言,能量被定义为工作或创造某种变化的能力。 能量以不同的形式存在。 例如,电能、光能和热能都是不同类型的能量。 要了解能量流入和流出生物系统的方式,了解控制能量的两个物理定律非常重要。
热力学
热力学第一定律指出,宇宙中的总能量是恒定和守恒的。 换句话说,宇宙中一直存在并将永远存在完全相同的能量。 能量以许多不同的形式存在。 根据热力学第一定律,能量可以从一个地方转移到另一个地方,也可以转化为不同的形式,但不能被创造或摧毁。 能量的转移和转化无时无刻不在我们的周围。 灯泡将电能转化为光能和热能。 燃气灶将天然气中的化学能转化为热能。 植物进行地球上生物学上最有用的能量转化之一:将阳光的能量转化为储存在有机分子中的化学能(图\(\PageIndex{1}\))。 一些能量转换的例子如图所示\(\PageIndex{3}\)。
所有活生物体面临的挑战是从周围环境中获取能量,这些能量可以转移或转化为可用能量来工作。 活细胞已经进化以应对这一挑战。 储存在糖和脂肪等有机分子中的化学能通过一系列细胞化学反应转移并转化为ATP分子内的能量。 ATP 分子中的能量很容易就能起作用。 细胞需要做的工作类型的例子包括构建复杂的分子、运输材料、为纤毛或鞭毛的运动提供动力,以及收缩肌肉纤维以产生运动。

活细胞的主要任务是获取、转化和使用能量来工作,可能看起来很简单。 但是,热力学第二定律解释了为什么这些任务比看起来更难。 所有的能量转移和转换从来都不是完全有效的。 在每一次能量传递中,一定数量的能量都会以无法使用的形式流失。 在大多数情况下,这种形式是热能。 从热力学上讲,热能被定义为从一个系统转移到另一个系统的不起作用的能量。 例如,当灯泡开启时,从电能转化为光能的部分能量会作为热能流失。 同样,在细胞代谢反应过程中,一些能量会作为热能流失。
物理系统中的一个重要概念是秩序和混乱的概念。 系统向周围环境损失的能量越多,系统的秩序就越少,随机性就越强。 科学家将衡量系统内随机性或无序性的方法称为熵。 高熵意味着高混乱和低能量。 分子和化学反应也有不同的熵。 例如,当一个地方的高浓度分子扩散和扩散时,熵会增加。 热力学第二定律说,在能量转移或转换中,能量总是会像热量一样流失。
生物是高度有序的,需要在低熵状态下保持恒定的能量输入。
势能和动能
当一个物体在运动时,会有与该物体相关的能量。 想想一个破坏球。 即使是缓慢移动的破坏球也会对其他物体造成很大的伤害。 与运动中的物体相关的能量称为动能(图\(\PageIndex{4}\))。 超速子弹、行走的人和分子在空气中的快速移动(产生热量)都具有动能。
现在,如果用起重机将同样一动不动的破坏球抬到地上两层楼怎么办? 如果悬浮的破坏球不动,有与之相关的能量吗? 答案是肯定的。 举起破坏球所需的能量并没有消失,而是由于破坏球的位置和作用在破坏球上的重力而储存在破坏球中。 这种类型的能量称为势能(图\(\PageIndex{4}\))。 如果球掉下来,势能将转化为动能,直到球落在地面上时所有潜在能量都耗尽为止。 破坏球也像钟摆一样摆动;通过挥杆,势能(挥杆顶部最高)不断变化为动能(挥杆底部最高)。 潜在能量的其他例子包括大坝后面的水或即将从飞机上跳伞的人的能量。

势能不仅与物质的位置有关,还与物质的结构有关。 即使是地面上的弹簧被压缩,也会有潜在的能量;拉紧的橡皮筋也是如此。 在分子层面上,将分子原子固定在一起的键存在于具有势能的特定结构中。 请记住,合成代谢细胞途径需要能量才能从更简单的分子中合成复杂的分子,而分解代谢途径在复杂分子被分解时会释放能量。 某些化学键的分解可以释放能量,这意味着这些键具有潜在的能量。 实际上,在我们吃的所有食物分子的键中都储存着潜在的能量,这些能量最终被用来使用。 这是因为这些键在破裂时会释放能量。 存在于化学键中并在这些键断裂时释放出来的那种势能称为化学能。 化学能负责为活细胞提供食物中的能量。 当食物分子中的分子键被破坏时,就会释放能量。
概念在行动
访问该网站并从 “工作与能量” 菜单中选择 “摆锤”,查看运动中摆的动能和势能变化。
自由能和活化能
在得知化学反应在能量储存键被破坏时会释放能量之后,下一个重要的问题是:与这些化学反应相关的能量是如何量化和表达的? 如何将一种反应释放的能量与另一种反应释放的能量进行比较? 自由能的测量用于量化这些能量传递。 回想一下,根据热力学第二定律,所有能量转移都涉及以不可用形式(例如热量)损失一定数量的能量。 自由能专门指与化学反应相关的能量,这种能量在计入损失后可用。 换句话说,自由能是可用的能量,或可用于工作的能量。
如果在化学反应过程中释放了能量,则自由能的变化(以 ΔG(delta G)表示)将为负数。 自由能的负变化也意味着反应产物的自由能少于反应物,因为它们在反应过程中会释放一些自由能。 自由能发生负变化并因此释放自由能的反应被称为 exergonic 反应。 想想:ex energonic 意味着能量正在消耗系统。 这些反应也被称为自发反应,其产物储存的能量比反应物少。 必须在 “自发” 一词和立即发生化学反应的概念之间作出重要的区分。 与该术语的日常用法相反,自发反应不是突然或迅速发生的反应。 铁的生锈是自发反应的一个例子,随着时间的推移,这种反应逐渐缓慢发生。
如果化学反应吸收能量而不是平衡地释放能量,则该反应的 ΔG 将为正值。 在这种情况下,产物比反应物具有更多的自由能。 因此,这些反应的产物可以看作是能量储存分子。 这些化学反应被称为内源反应,它们是非自发的。 如果不添加自由能,内能反应就不会自行发生。
艺术连接

查看所示的每个过程,然后确定它是内源性还是外激性。
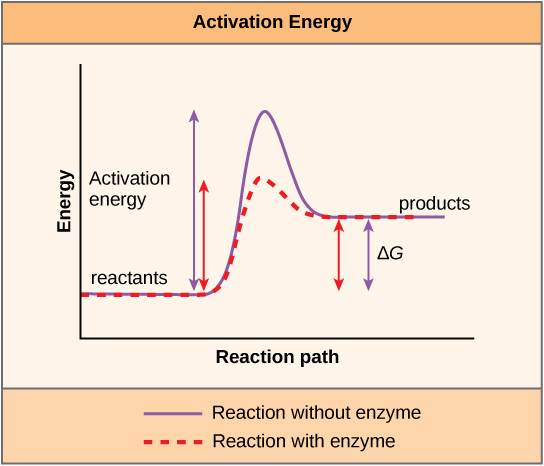
关于内能和外激反应,还有另一个重要的概念需要考虑。 Exergonic 反应需要少量能量输入才能开始,然后才能继续进行能量释放步骤。 这些反应可以净释放能量,但一开始仍然需要一些能量输入。 所有化学反应发生所需的少量能量输入称为活化能。
概念在行动
观看反应从自由能转变为过渡状态的动画。
酶
有助于发生化学反应的物质称为催化剂,催化生化反应的分子称为酶。 大多数酶都是蛋白质,其关键任务是降低细胞内化学反应的活化能。 大多数对活细胞至关重要的反应在正常温度下发生得太慢,对细胞没有任何用处。 没有酶来加速这些反应,生命就无法持续下去。 酶通过与反应物分子结合并保持它们的方式来做到这一点,从而使化学键破裂和形成过程更容易发生。 重要的是要记住,无论反应是外激素(自发)还是内激性,酶都不会改变。 这是因为它们不会改变反应物或产物的自由能。 它们只会减少反应进行所需的活化能(图\(\PageIndex{6}\))。 此外,酶本身不会因其催化反应而改变。 一旦一种反应被催化,该酶就能参与其他反应。
酶结合的化学反应物称为酶的底物。 可能存在一种或多种底物,具体取决于特定的化学反应。 在某些反应中,单个反应物底物会分解成多种产物。 在其他情况下,两个底物可能聚集在一起形成一个更大的分子。 两种反应物也可能进入反应并都经过改性,但它们将反应作为两种产物留下。 酶内底物结合的位置称为酶的活性位点。 活动站点是 “操作” 发生的地方。 由于酶是蛋白质,因此活性位点内存在氨基酸侧链的独特组合。 每条侧链都有不同的特性。 它们可以是大或小,弱酸性或碱性,亲水性或疏水性,带正电荷或负电荷的,或者是中性的。 侧链的独特组合在活性位点内创造了一个非常特殊的化学环境。 这种特定的环境适合与一种特定的化学底物(或底物)结合。
活跃地点会受到当地环境的影响。 提高环境温度通常会提高反应速率,无论是酶催化还是其他方式。 但是,超出最佳范围的温度会降低酶催化反应的速率。 高温最终会导致酶变性,这是三维形状不可逆转的变化,从而影响酶的功能。 酶也适合在一定的 pH 值和盐浓度范围内发挥最佳作用,而且,与温度一样,极端 pH 值和盐浓度会导致酶变性。
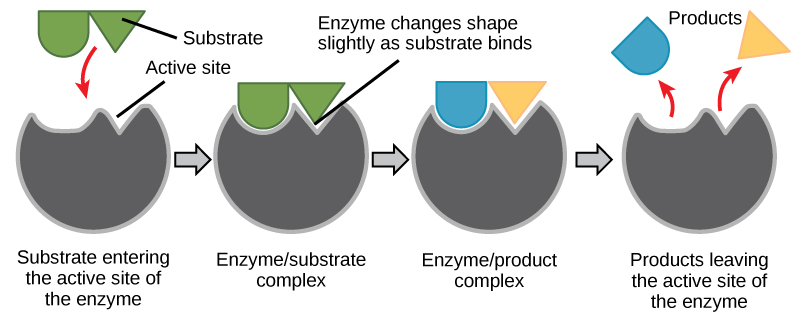
多年来,科学家们一直认为酶与底物的结合是以简单的 “锁和钥匙” 方式进行的。 该模型断言,酶和底物在一个瞬间的步骤中完美地结合在一起。 但是,目前的研究支持一种名为诱导拟合的模型(图\(\PageIndex{7}\))。 诱导拟合模型通过描述酶和底物之间更具动态性的结合,在锁和钥匙模型的基础上进行了扩展。 当酶和底物聚集在一起时,它们的相互作用会导致酶的结构发生轻微变化,从而在酶和底物之间形成理想的结合排列。
概念在行动
观看诱导拟合的动画。
当酶结合其底物时,就会形成酶底物复合物。 这种复合物降低了反应的活化能,并以多种可能的方式之一促进其快速发展。 在基本层面上,酶通过将底物聚集在一起以最佳的反应方向来促进涉及多种底物的化学反应。 酶促进其底物反应的另一种方法是在活性位点内为反应的发生创造最佳环境。 活性位点内氨基酸 R 基团的特定排列产生的化学特性为酶的特定底物反应创造了理想的环境。
酶底物复合物还可以通过破坏键结构来降低活化能,从而使其更容易破裂。 最后,酶还可以通过参与化学反应本身来降低活化能。 在这些情况下,重要的是要记住,反应完成后,酶将始终恢复到其原始状态。 酶的标志性特性之一是,它们所催化的反应最终保持不变。 在酶催化反应后,它会释放其产物并可以催化新的反应。
如果设想这样一种情景,即生物体的所有酶都供应充足,并且在所有细胞条件下、所有细胞中始终发挥最佳功能,这似乎是理想的选择。 但是,各种机制可以确保这种情况不会发生。 细胞的需求和条件因细胞而异,并且随着时间的推移,单个细胞内部会发生变化。 胃细胞所需的酶不同于脂肪储存细胞、皮肤细胞、血细胞和神经细胞的酶。 此外,与饭后的许多小时相比,消化器官细胞在饭后不久就更难处理和分解营养。 随着这些细胞需求和条件的变化,不同酶的数量和功能也必须变化。
由于生化反应的速率受活化能控制,而酶降低并决定化学反应的活化能,因此细胞内各种酶的相对含量和功能最终决定了哪些反应将以什么速率进行。 这种测定在细胞中受到严格控制。 在某些细胞环境中,酶活性部分受环境因素的控制,例如pH、温度、盐浓度,在某些情况下,还有辅助因子或辅酶。
也可以通过促进或降低酶活性的方式调节酶。 抑制或促进酶功能的分子种类很多,它们起作用的机制也多种多样。 在某些酶抑制情况下,抑制剂分子与底物足够相似,它可以与活性位点结合并简单地阻断底物的结合。 当这种情况发生时,该酶会通过竞争抑制而受到抑制,因为抑制剂分子与底物竞争与活性位点结合。
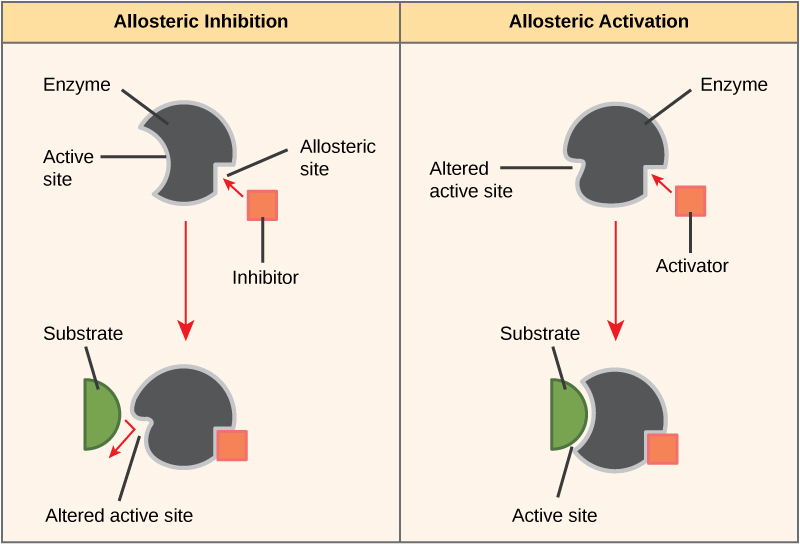
另一方面,在非竞争性抑制中,抑制剂分子在活性位点以外的位置与酶结合,称为变构位点,但仍然设法阻断底物与活性位点的结合。 一些抑制剂分子在结合诱导构象变化的位置与酶结合,从而降低酶对其底物的亲和力。 这种类型的抑制称为变构抑制(图\(\PageIndex{8}\))。 大多数变构调节的酶由多个多肽组成,这意味着它们具有多个蛋白质亚单位。 当变构抑制剂与酶上的某个区域结合时,蛋白质亚基上的所有活性位点都会略有变化,因此它们以较低的效率结合底物。 有变构激活剂和抑制剂。 变构激活剂与酶上远离活性位点的位置结合,诱发构象变化,从而增加该酶活性位点对其底物的亲和力(图\(\PageIndex{8}\))。
行动中的职业生涯:药物开发人员

酶是代谢途径的关键组成部分。 了解酶的工作原理以及如何对其进行监管是当今市场上许多药物开发背后的关键原则。 在该领域工作的生物学家与其他科学家合作设计药物(图\(\PageIndex{9}\))。
以他汀类药物为例,他汀类药物是一类可以降低胆固醇水平的药物的名称。 这些化合物是HMG-CoA还原酶的抑制剂,HMG-CoA还原酶是从体内脂质中合成胆固醇的酶。 通过抑制这种酶,可以降低体内合成的胆固醇水平。 同样,通常以泰诺品牌销售的对乙酰氨基酚是环氧合酶的抑制剂。 虽然它被用来缓解发烧和炎症(疼痛),但其作用机制仍未完全理解。
毒品是如何被发现的? 药物发现的最大挑战之一是确定药物靶标。 药物靶标是一种实际上是药物靶标的分子。 就他汀类药物而言,HMG-CoA 还原酶是药物靶标。 药物靶点是通过实验室的艰苦研究确定的。 仅识别靶标是不够的;科学家们还需要知道靶标在细胞内是如何作用的,以及发生疾病时哪些反应会出错。 一旦确定了靶点和途径,药物设计的实际过程就开始了。 在这个阶段,化学家和生物学家共同设计和合成可以阻断或激活特定反应的分子。 但是,这仅仅是开始:如果药物原型成功发挥其功能,那么在获得美国食品药品监督管理局的批准之前,它要经过从体外实验到临床试验的许多测试。
除非与其他特定的非蛋白质辅助分子结合,否则许多酶无法发挥最佳作用,甚至根本无法发挥作用。 它们可以通过离子键或氢键暂时结合,也可以通过更强的共价键永久结合。 与这些分子结合可促进其各自酶的最佳形状和功能。 这些类型的辅助分子的两个例子是辅因子和辅酶。 辅助因子是无机离子,例如铁离子和镁离子。 辅酶是有机辅助分子,具有由碳和氢组成的基本原子结构。 像酶一样,这些分子参与反应而不会自行改变,最终被回收和重复使用。 维生素是辅酶的来源。 有些维生素是辅酶的前体,而另一些则直接起到辅酶的作用。 维生素 C 是多种酶的直接辅酶,这些酶参与构建重要的结缔组织胶原蛋白。 因此,酶的功能在一定程度上受各种辅助因子和辅酶的丰富性的调节,这些辅助因子和辅酶可能由生物体的饮食提供,在某些情况下由生物体产生。
代谢途径中的反馈抑制
分子可以通过多种方式调节酶的功能。 但是,主要问题仍然存在:这些分子是什么,它们来自哪里? 如你所知,有些是辅助因子和辅酶。 细胞中还有哪些其他分子提供酶调节,例如变构调制以及竞争和非竞争抑制? 也许就酶促细胞代谢而言,最相关的调节分子来源是细胞代谢反应本身的产物。 以一种最有效和最优雅的方式,细胞已经进化为使用自身反应的产物来抑制酶活性的反馈。 反馈抑制涉及使用反应产物来调节其自身的进一步产生(图\(\PageIndex{10}\))。 细胞对大量产物的反应是减缓合成代谢或分解代谢反应期间的产生。 此类反应产物可以通过上述机制抑制催化其产生的酶。
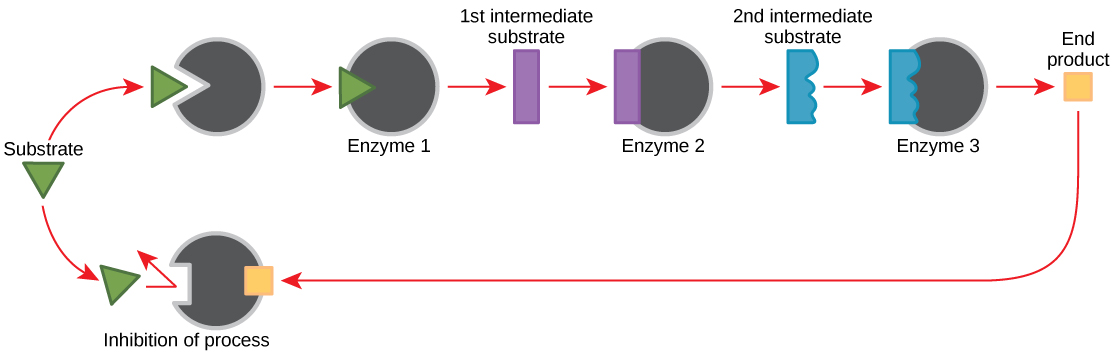
通过反馈抑制来控制氨基酸和核苷酸的产生。 此外,ATP 是糖分解代谢所涉及的一些酶的变构调节剂,糖分解是产生 ATP 的过程。 这样,当 ATP 供应充足时,细胞可以阻止 ATP 的产生。 另一方面,ADP 是一些被 ATP 抑制的相同酶的正变构调节剂(变构激活剂)。 因此,当与ATP相比,当ADP的相对水平较高时,细胞会被触发通过糖分解代谢产生更多的ATP。
章节摘要
细胞通过各种化学反应发挥生命的功能。 细胞的新陈代谢是指其内部发生的化学反应的组合。 分解代谢反应将复杂的化学物质分解成更简单的化学物质,并与能量释放有关。 合成代谢过程从较简单的分子中生成复杂的分子,需要能量。
在研究能量时,“系统” 一词是指能量转移所涉及的物质和环境。 熵是衡量系统无序的一种方法。 描述能量转移的物理定律是热力学定律。 第一定律指出,宇宙中的总能量是恒定的。 热力学第二定律指出,每一次能量传递都涉及一些不可用形式的能量损失,例如热能。 能量有不同的形式:动能、势能和自由能。 反应自由能的变化可以是负的(释放能量,exergonic),也可以是正的(消耗能量,endergonic)。 所有反应都需要初始能量输入才能进行,称为活化能。
酶是化学催化剂,通过降低活化能来加速化学反应。 酶的活性位点具有独特的化学环境,适合该酶的特定化学反应物,称为底物。 根据诱导拟合模型,酶和底物被认为是结合的。 对酶的作用进行调节,以节约资源并对环境做出最佳反应。
艺术联系
图\(\PageIndex{5}\):查看所示的每个过程,然后确定它是内源性还是外激性。
- 回答
-
堆肥堆的分解是一个运动过程。 从受精卵中发育出来的婴儿是一个内生过程。 茶溶解在水中是一种运动过程。 滚球下坡是一个运动过程。
词汇表
- 活化能
- 发生反应所需的初始能量
- 活跃站点
- 酶上底物结合的特定区域
- 变构抑制
- 抑制酶作用的机制,在这种机制中,调节分子与第二个位点(不是活性位点)结合并引发活性位点的构象变化,从而阻止与底物的结合
- 合成代谢的
- 描述了需要净能量输入才能从更简单的分子中合成复杂分子的途径
- 生物能量学
- 能量流经生命系统的概念
- 分解代谢的
- 描述了复杂分子被分解成更简单的分子,产生能量作为反应的额外产物的途径
- 竞争抑制
- 酶活性调节的一般机制,其中除酶底物之外的分子能够结合活性位点并防止底物本身结合,从而抑制酶的总体反应速率
- endergonic
- 描述了一种化学反应,该反应产生的产物比反应物储存更多的化学势能
- 酶
- 一种催化生化反应的分子
- exergonic
- 描述了一种化学反应,该反应产生的产物的化学势能比反应物少,再加上自由能的释放
- 反馈抑制
- 一种酶活性调节机制,其中反应的产物或一系列顺序反应的最终产物在反应系列的早期阶段抑制酶
- 热能
- 从一个系统转移到另一个系统的不起作用的能量
- 动能
- 与运动中的物体相关的能量类型
- 新陈代谢
- 细胞内部发生的所有化学反应,包括消耗能量的化学反应和释放能量的化学反应
- 非竞争性抑制
- 酶活性调节的一般机制,其中调节分子与活性位点以外的位点结合并阻止活性位点与底物结合;因此,抑制剂分子不会与底物竞争活性位点;变构抑制是一种形式非竞争性抑制
- 潜在能量
- 指工作潜力的能量类型
- 底层
- 酶作用的分子
- 热电学
- 热能、能量和工作之间关系的科学


