25.4: الالتهابات الطفيلية في الدورة الدموية والجهاز الليمفاوي
- Page ID
- 195200
أهداف التعلم
- تحديد الطفيليات الشائعة التي تسبب التهابات الدورة الدموية والجهاز الليمفاوي
- قارن الخصائص الرئيسية لأمراض طفيلية محددة تؤثر على الدورة الدموية والجهاز اللمفاوي
بعض البروتوزوا والذباب الطفيلية قادرة أيضًا على التسبب في التهابات في الدورة الدموية البشرية. على الرغم من أن هذه الإصابات نادرة في الولايات المتحدة، إلا أنها لا تزال تسبب معاناة واسعة النطاق في العالم النامي اليوم. الالتهابات الفطرية في الدورة الدموية نادرة جدًا. لذلك، لم تتم مناقشتها في هذا الفصل.
الملاريا
على الرغم من أكثر من قرن من الأبحاث المكثفة والتطورات السريرية، لا تزال الملاريا واحدة من أهم الأمراض المعدية في العالم اليوم. إن توزيعها على نطاق واسع يعرض أكثر من نصف سكان العالم للخطر. في عام 2015، قدرت منظمة الصحة العالمية وجود حوالي 214 مليون حالة إصابة بالملاريا في جميع أنحاء العالم، مما أدى إلى حوالي 438000 حالة وفاة؛ حوالي 88٪ من الحالات و 91٪ من الوفيات حدثت في أفريقيا. 1 على الرغم من أن الملاريا لا تشكل حاليًا تهديدًا كبيرًا في الولايات المتحدة، إلا أن إمكانية إعادة إدخالها مصدر قلق. تحدث الملاريا بسبب العديد من الطفيليات الأولية في جنس Plasmodium: P. falciparum و P. knowlesi و P. malariae و P. ovale و P. vivax. يصيب البلازموديوم خلايا الدم الحمراء بشكل أساسي وينتقل عن طريق لدغة بعوض الأنوفيل.
في الوقت الحالي، تعد P. falciparum السبب الأكثر شيوعًا والأكثر فتكًا للملاريا، وغالبًا ما تسمى الملاريا المنجلية. تنتشر الملاريا المنجلية في المناطق ذات الكثافة السكانية العالية في إفريقيا وآسيا، مما يعرض العديد من الأشخاص لخطر الإصابة بأشد أشكال المرض.
العلامات والأعراض الكلاسيكية للملاريا هي دورات من الحمى الشديدة والقشعريرة. تبدأ الأعراض المفاجئة والعنيفة للملاريا بالضيق والقشعريرة المفاجئة والحمى (39-41 درجة مئوية [102.2-105.8 درجة فهرنهايت]) والنبض السريع والخافت وبولي البول والصداع والألم العضلي والغثيان والقيء. بعد 2 إلى 6 ساعات من هذه الأعراض، تنخفض الحمى، ويحدث التعرق الغزير لمدة 2 إلى 3 ساعات، يليه التعب الشديد. هذه الأعراض ناتجة عن ظهور البلازموديوم من خلايا الدم الحمراء بشكل متزامن، مما يؤدي إلى تمزق متزامن لعدد كبير من خلايا الدم الحمراء، مما يؤدي إلى تلف الطحال والكبد والغدد الليمفاوية ونخاع العظام. يتسبب تلف الأعضاء الناتج عن انحلال الدم في إصابة المرضى بحمأة الدم (أي الدم الذي تتجمع فيه خلايا الدم الحمراء إلى كتل) مما قد يؤدي إلى نقص الأكسجين ونخر الأوعية الدموية وفشل الأعضاء والموت.
في حالات العدوى المؤكدة، تحدث دورات الملاريا من الحمى والقشعريرة عادةً كل يومين في المرض الموصوف بالملاريا الثلاثية، والذي يسببه P. vivax و P. ovale. تحدث الدورات كل 3 أيام في المرض الموصوف بالملاريا الكوارتانية، والذي تسببه بكتيريا الملاريا. قد تختلف هذه الفواصل بين الحالات.
يحتوي Plasmodium على دورة حياة معقدة تتضمن العديد من مراحل النمو التي يتم إنتاجها بالتناوب في البعوض والبشر (الشكل\(\PageIndex{1}\)). عندما تتناول البعوضة المصابة وجبة دم، يتم حقن الأبواغ الموجودة في الغدة اللعابية للبعوض في دم المضيف. وتنتقل هذه الطفيليات إلى الكبد، حيث تتطور إلى حالات انفصام. يخضع الفصاميون بعد ذلك لمرض الفصام، مما يؤدي إلى إطلاق العديد من الميروزويت في وقت واحد. تنتقل الميروزويت إلى مجرى الدم وتصيب خلايا الدم الحمراء. داخل خلايا الدم الحمراء، تتطور الميروزويت إلى تروفوزويت تنتج المزيد من الميروزويت. يؤدي الإطلاق المتزامن للميروزويت من خلايا الدم الحمراء في المساء إلى ظهور أعراض الملاريا.
بالإضافة إلى ذلك، تتطور بعض أنواع التروفوزويت بدلاً من ذلك إلى خلايا مشيمية ذكورية وأنثوية. يتم تناول الخلايا المشيمية عندما تأخذ البعوضة وجبة دم من شخص مصاب. تحدث الجراثيم الجنسية في أمعاء البعوض. تندمج الخلايا المشيمية لتشكل زيجوت في أمعاء الحشرات. تصبح الزيجوت متحركة وتتمدد إلى أوكينيت. يخترق هذا النموذج جدار الأمعاء الوسطى ويتطور إلى بويضة. أخيرًا، تطلق البويضة سبوروزويت جديدة تهاجر إلى الغدد اللعابية للبعوض لإكمال دورة الحياة.
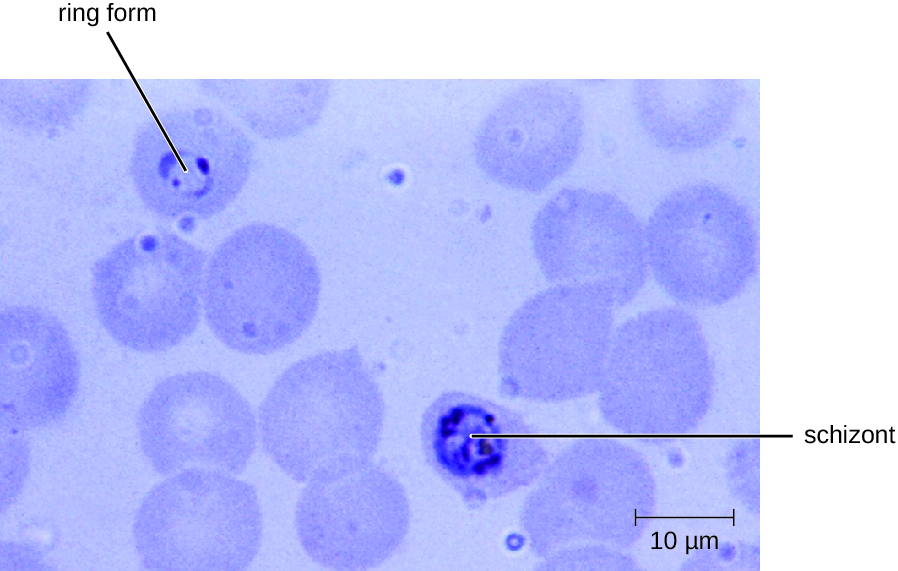
يتم تشخيص الملاريا عن طريق الملاحظة المجهرية للأشكال التنموية للبلازموديوم في مسحات الدم واختبارات تقييم الأثر البيئي السريعة التي تكشف عن مستضدات أو إنزيمات البلازموديوم (الشكل\(\PageIndex{2}\)). يمكن وصف أدوية مثل الكلوروكين والأتوفاكون والأرتيميثير واللوميفانترين لكل من العلاج الحاد والوقائي، على الرغم من أن بعض Plasmodium spp. أظهرت مقاومة للأدوية المضادة للملاريا. يمكن أن يؤدي استخدام المبيدات الحشرية والناموسيات المعالجة بمبيدات الحشرات إلى الحد من انتشار الملاريا. على الرغم من الجهود المبذولة لتطوير لقاح للملاريا، لا يتوفر أي لقاح حاليًا.
![دورة حياة بلاسموديوم. [مراحل الكبد البشري] 1 - يأخذ البعوض وجبة دم ويحقن البلازموديوم في الإنسان. 2 - يصيب البلازموديوم خلايا الكبد. 3 - يتكاثر البلازموديوم في خلية الكبد. [مراحل الدم البشري] 4 - يدخل البلازموديوم الدم. تبدو مرحلة الحلقة غير الناضجة مثل حلقة سيغنيت في خلية الدم الحمراء. تصبح هذه المرحلة مرحلة ناضجة وتخضع للانقسام الفتيلي لإنتاج الفصام الذي يتم إطلاقه عن طريق تمزق خلايا الدم الحمراء. 5 - الأمشاج (1n) التي ينتجها الانقسام الاختزالي. [مراحل البعوض] 6 - يأخذ البعوض وجبة دم ويبتلع الأمشاج. 7 - تقوم الميكروجاميت بتخصيب الماكروجاميت. 8 - أشكال الزيجوت (2n). 9 - يخضع الزيجوت للانقسام الفتيلي. 10 - يفرق الطفيل ويدخل لعاب البعوض.](https://bio.libretexts.org/@api/deki/files/9172/OSC_Microbio_25_04_Malaria.jpg)
دخلت حملة «لا شيء سوى الناموسيات»، وهي مبادرة من مؤسسة الأمم المتحدة، في شراكة مع مؤسسة بيل وميليندا غيتس لجعل الناموسيات متاحة في البلدان النامية في أفريقيا. قم بزيارة موقع الويب الخاص بهم لمعرفة المزيد عن جهودهم للوقاية من الملاريا.
التمارين الرياضية\(\PageIndex{1}\)
لماذا تعتبر الملاريا من أهم الأمراض المعدية؟
داء المقوسات
يحدث مرض التوكسوبلاسما بسبب التوكسوبلازما الغوندي الأولي. توجد T. gondii في مجموعة متنوعة من الطيور والثدييات، 2 والعدوى البشرية شائعة. تشير تقديرات مراكز مكافحة الأمراض والوقاية منها (CDC) إلى أن 22.5 في المائة من السكان الذين تبلغ أعمارهم 12 عامًا أو أكثر قد أصيبوا بعدوى T. gondii؛ لكن الأفراد ذوي الكفاءة المناعية عادة ما يكونون بدون أعراض. 3 القطط المنزلية هي المضيف النهائي الوحيد المعروف للمراحل الجنسية من T. gondii، وبالتالي فهي الخزانات الرئيسية للعدوى. تقوم القطط المصابة بإلقاء بويضات T. gondii في برازها، وعادة ما تنتشر هذه البويضات إلى البشر من خلال ملامسة المواد البرازية على أجسام القطط، أو في صناديق القمامة، أو في أسرّة الحدائق حيث تتبرز القطط في الهواء الطلق.
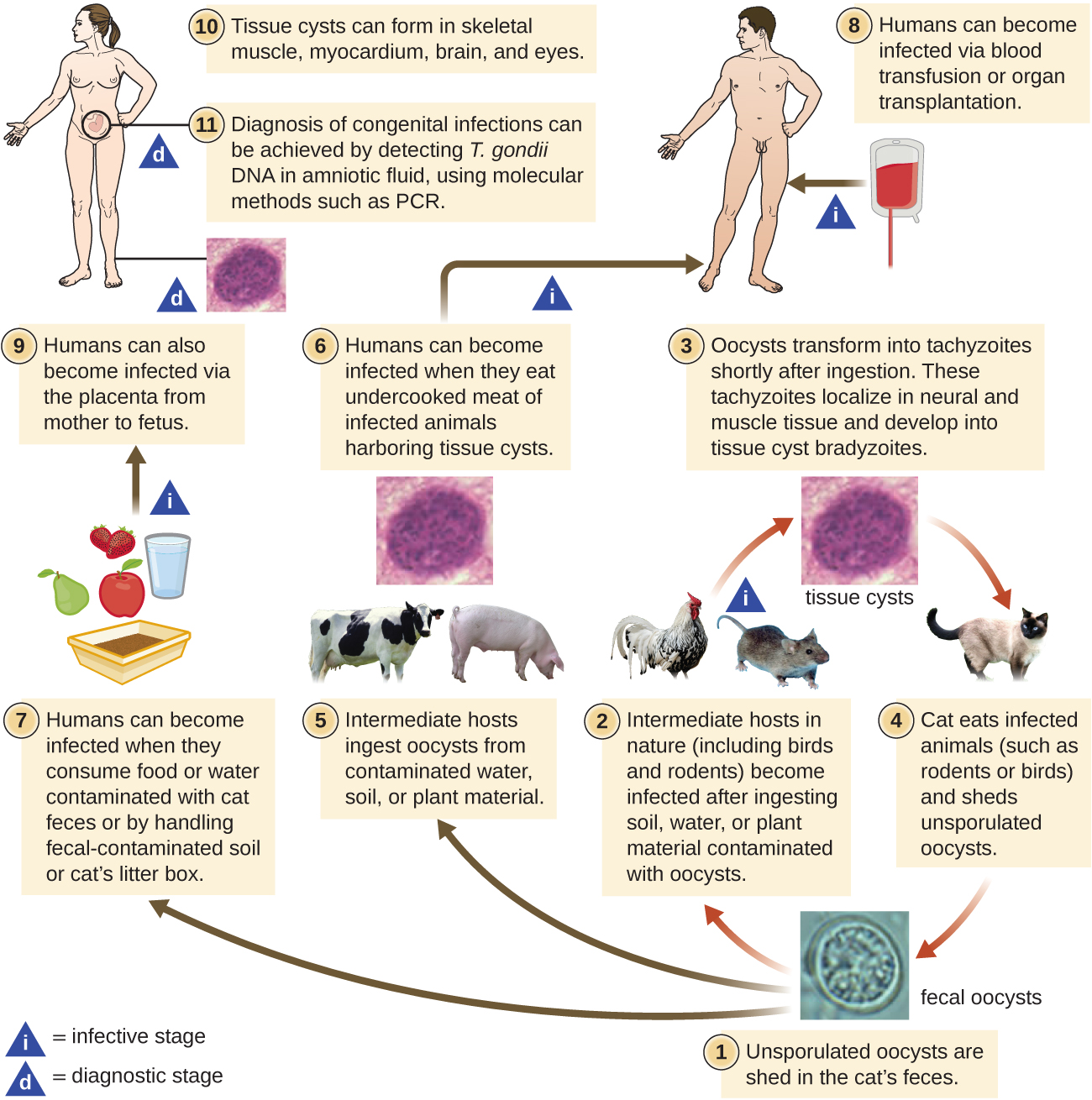
يحتوي T. gondii على دورة حياة معقدة تتضمن العديد من المضيفين. تبدأ دورة حياة T. gondii عندما يتم إلقاء البويضات غير المبثوثة في براز القطة. تستغرق هذه البويضات من 1 إلى 5 أيام لتتكاثر في البيئة وتصبح معدية. تشمل المضيفين المتوسطين في الطبيعة الطيور والقوارض، التي تصاب بالعدوى بعد تناول التربة أو الماء أو المواد النباتية الملوثة بالبويضات المعدية. بمجرد تناولها، تتحول البويضات إلى تاشيزويت تتمركز في الأنسجة العصبية والعضلية للطيور أو القوارض، حيث تتطور إلى كيسات نسيجية. قد تصاب القطط بعد تناول الطيور والقوارض التي تحتوي على أكياس الأنسجة. قد تصاب القطط والحيوانات الأخرى أيضًا مباشرة عن طريق ابتلاع البويضات المبثوثة في البيئة. ومن المثير للاهتمام أن عدوى التوكسوبلازما تبدو قادرة على تعديل سلوك المضيف. تفقد الفئران المصابة بالتوكسوبلازما خوفها من فيرومونات القطط. ونتيجة لذلك، تصبح فريسة أسهل للقطط، مما يسهل انتقال الطفيل إلى المضيف النهائي للقطط 4 (الشكل\(\PageIndex{3}\)).
تعد عدوى التوكسوبلازما عند البشر شائعة للغاية، ولكن معظم الأشخاص المصابين لا تظهر عليهم أعراض أو لديهم أعراض فرعية. تشير بعض الدراسات إلى أن الطفيل قد يكون قادرًا على التأثير على الشخصية والأداء النفسي الحركي للبشر المصابين، على غرار الطريقة التي يعدل بها السلوك في الثدييات الأخرى. 5 عندما تظهر الأعراض، فإنها تميل إلى أن تكون خفيفة وتشبه أعراض كريات الدم البيضاء. ومع ذلك، يمكن أن يصبح داء المقوسات بدون أعراض مشكلة في حالات معينة. يمكن أن تستقر الأكياس في مجموعة متنوعة من الأنسجة البشرية وتبقى نائمة لسنوات. يمكن أن تحدث إعادة تنشيط هذه العدوى الهادئة في المرضى الذين يعانون من نقص المناعة بعد الزرع أو علاج السرطان أو تطور اضطراب مناعي مثل الإيدز. في المرضى المصابين بالإيدز الذين يعانون من داء المقوسات، لا يستطيع الجهاز المناعي مكافحة نمو T. gondii في أنسجة الجسم؛ ونتيجة لذلك، يمكن أن تسبب هذه الأكياس التهاب الدماغ والتهاب الشبكية والالتهاب الرئوي والاضطرابات المعرفية والنوبات التي يمكن أن تكون قاتلة في نهاية المطاف.
يمكن أن يشكل داء المقوسات أيضًا خطرًا أثناء الحمل لأن تاكيزويت يمكن أن تعبر المشيمة وتسبب التهابات خطيرة في الجنين النامي. يعتمد مدى الضرر الجنيني الناتج عن داء المقوسات على شدة مرض الأم، والأضرار التي لحقت بالمشيمة، والعمر الحملي للجنين عند الإصابة، وضراوة الكائن الحي. غالبًا ما يؤدي داء المقوسات الخلقي إلى فقدان الجنين أو الولادة المبكرة ويمكن أن يؤدي إلى تلف الجهاز العصبي المركزي، ويتجلى ذلك في التخلف العقلي أو الصمم أو العمى. وبالتالي، ينصح مركز مكافحة الأمراض والوقاية منها النساء الحوامل بإيلاء عناية خاصة في إعداد اللحوم والبستنة ورعاية القطط الأليفة. 6 عادة ما يتم تشخيص عدوى داء المقوسات أثناء الحمل عن طريق علم الأمصال بما في ذلك اختبار TORCH (يشير الحرف «T» في TORCH إلى داء المقوسات). يمكن أيضًا تشخيص الالتهابات الخلقية عن طريق الكشف عن الحمض النووي لـ T. gondii في السائل الأمنيوسي، باستخدام طرق جزيئية مثل PCR.
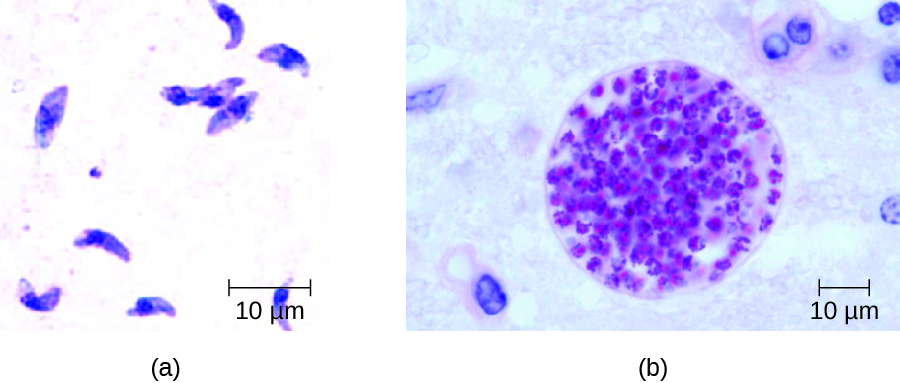
في البالغين، يمكن أن يشمل تشخيص داء المقوسات ملاحظة كيسات الأنسجة في عينات الأنسجة. يمكن ملاحظة تكيسات الأنسجة في عينات الخزعة الملطخة بغيمسا أو رايت، ويمكن أيضًا استخدام الأشعة المقطعية والتصوير بالرنين المغناطيسي والبزل القطني لتأكيد العدوى (الشكل\(\PageIndex{4}\)).
الوقاية من العدوى هي أفضل خط دفاع ضد داء المقوسات. تشمل التدابير الوقائية غسل اليدين جيدًا بعد التعامل مع اللحوم النيئة أو التربة أو فضلات القطط، وتجنب استهلاك الخضروات التي قد تكون ملوثة ببراز القطط. يجب طهي جميع اللحوم إلى درجة حرارة داخلية تتراوح بين 73.9-76.7 درجة مئوية (165-170 درجة فهرنهايت).
لا يحتاج معظم المرضى ذوي الكفاءة المناعية إلى تدخل سريري لعدوى التوكسوبلازما. ومع ذلك، يمكن علاج حديثي الولادة والنساء الحوامل والمرضى الذين يعانون من نقص المناعة باستخدام البيريميثامين والسلفاديازين - باستثناء خلال الأشهر الثلاثة الأولى من الحمل، لأن هذه الأدوية يمكن أن تسبب تشوهات خلقية. تم استخدام سبيراميسين بأمان لتقليل انتقال العدوى لدى النساء الحوامل المصابات بعدوى أولية خلال الأشهر الثلاثة الأولى من الحمل لأنه لا يعبر المشيمة.
التمارين الرياضية\(\PageIndex{2}\)
كيف تصيب T. gondii البشر؟
داء البابيزيا
داء البابيزيا هو مرض معدي حيواني نادر يسببه Babesia spp. تصيب هذه الطفيليات الطفيلية العديد من الحيوانات البرية والداجنة ويمكن أن تنتقل إلى البشر عن طريق قراد Ixodes ذات الأرجل السوداء. في البشر، تصيب البابيسيا خلايا الدم الحمراء وتتكاثر داخل الخلية حتى تتمزق. تستمر البابيزيا المنبعثة من خلايا الدم الحمراء الممزقة في دورة النمو عن طريق غزو خلايا الدم الحمراء الأخرى. قد يكون المرضى بدون أعراض، ولكن أولئك الذين يعانون من الأعراض غالبًا ما يعانون في البداية من الشعور بالضيق والتعب والقشعريرة والحمى والصداع وألم عضلي وألم مفصلي. في حالات نادرة، لا سيما في المرضى المصابين بمرض نقص الطحال (غياب الطحال) وكبار السن والمرضى المصابين بالإيدز، قد يشبه داء البابيزيا الملاريا المنجلية، مع ارتفاع درجة الحرارة وفقر الدم الانحلالي والهيموجلوبين (الهيموجلوبين أو الدم في البول) واليرقان والفشل الكلوي، ويمكن أن تكون العدوى قاتلة. قد تصبح عدوى بابيسيا بدون أعراض التي تم الحصول عليها سابقًا من أعراض إذا تم إجراء استئصال الطحال.
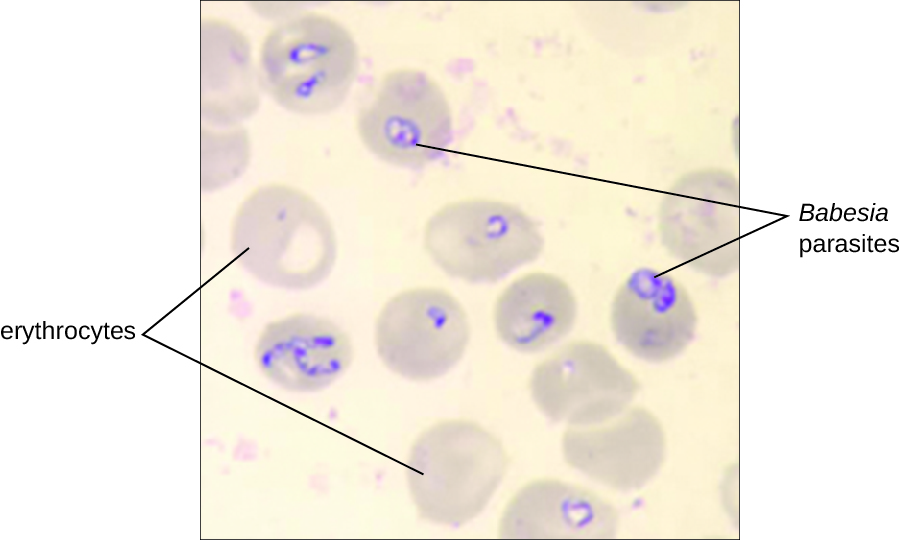
يعتمد التشخيص بشكل أساسي على الملاحظة المجهرية للطفيليات في مسحات الدم (الشكل\(\PageIndex{5}\)). يمكن أيضًا إجراء الكشف المصلي والأجسام المضادة بواسطة IFA وتتوفر الاختبارات القائمة على PCR. لا يحتاج العديد من الأشخاص إلى تدخل سريري لعدوى البابيسيا، ومع ذلك، يمكن إزالة العدوى الخطيرة بمزيج من أتوفاكون وأزيثروميسين أو مزيج من الكليندامايسين والكينين.
مرض شاغاس
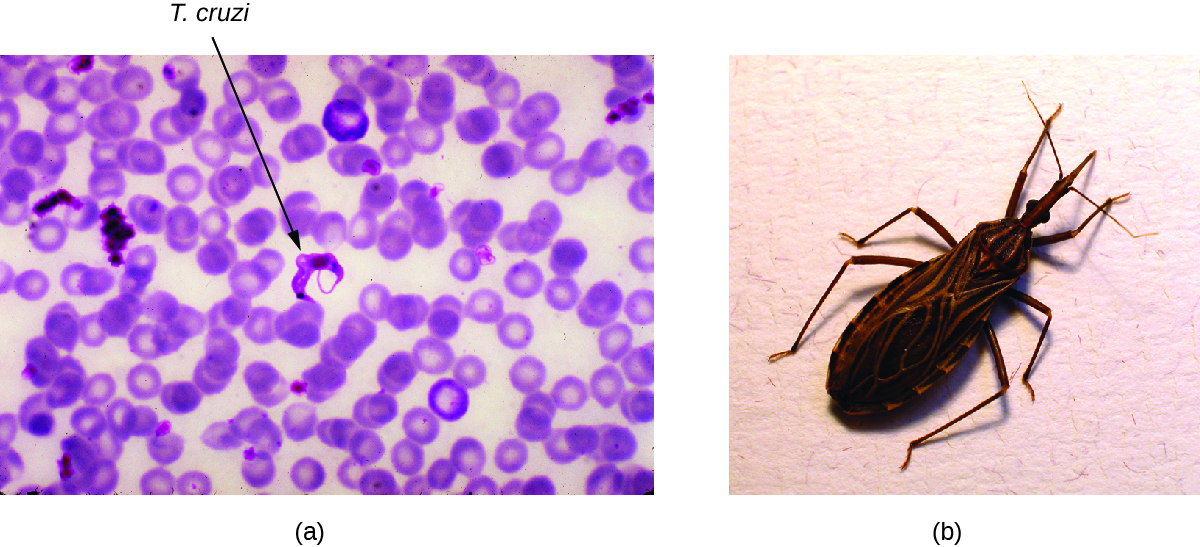
يُعرف مرض شاغاس أيضًا باسم داء المثقبيات الأمريكي، وهو مرض حيواني المنشأ يُصنف على أنه مرض استوائي مهمل (NTD). يحدث هذا المرض بسبب داء المثقبيات الكروزي البروتوزي ذي السوط وينتقل بشكل شائع إلى الحيوانات والبشر من خلال براز بق الترياتومين. يُطلق على حشرة الترياتومين اسم حشرة التقبيل لأنها كثيرًا ما تلدغ البشر على الوجه أو حول العينين؛ غالبًا ما تتبرز الحشرة بالقرب من اللدغة وقد يتم فرك المادة البرازية المصابة في جرح اللدغة من قبل الشخص الذي تعرض للعض (الشكل\(\PageIndex{6}\)). اللدغة نفسها غير مؤلمة، وفي البداية، لا يظهر الكثير من الناس أي علامات للمرض. تشمل طرق الانتقال البديلة عمليات نقل الدم الملوثة وزرع الأعضاء من المتبرعين المصابين والانتقال الخلقي من الأم إلى الجنين.
مرض شاغاس متوطن في معظم أنحاء المكسيك وأمريكا الوسطى وأمريكا الجنوبية، حيث تشير تقديرات منظمة الصحة العالمية إلى إصابة ما بين 6 و7 ملايين شخص. 7 حاليًا، لا يتوطن مرض شاغاس في الولايات المتحدة، على الرغم من وجود بق الترياتومين في النصف الجنوبي من البلاد.
عادةً ما تنشط حشرات الترياتومين في الليل، عندما تتناول وجبات الدم عن طريق عض وجوه وشفاه الأشخاص أو الحيوانات أثناء نومهم وغالبًا ما تتبرز بالقرب من مكان اللدغة. تحدث العدوى عندما يقوم المضيف بفرك البراز في عينيه أو فمه أو جرح اللدغة أو أي كسر آخر في الجلد. ثم يدخل البروتوزوان الدم ويغزو أنسجة القلب والجهاز العصبي المركزي، وكذلك البلاعم والخلايا الأحادية. تشمل المستودعات غير البشرية لطفيليات T. cruzi الحيوانات البرية والحيوانات الأليفة مثل الكلاب والقطط، والتي تعمل أيضًا كمستودعات للممرض. 8
هناك ثلاث مراحل لمرض شاغاس: الحادة والمتوسطة والمزمنة. يمكن أن تكون هذه المراحل إما بدون أعراض أو مهددة للحياة اعتمادًا على حالة الكفاءة المناعية للمريض.
في المرحلة الحادة من المرض، تشمل الأعراض الحمى والصداع والألم العضلي والطفح الجلدي والقيء والإسهال وتضخم الطحال والكبد والغدد الليمفاوية. بالإضافة إلى ذلك، قد تتشكل عقدة موضعية تسمى الشاغوما عند بوابة الدخول، وقد يحدث تورم في الجفون أو جانب الوجه، يسمى علامة Romaña، بالقرب من جرح اللدغة. قد تختفي أعراض المرحلة الحادة تلقائيًا، ولكن إذا لم يتم علاجها، يمكن أن تستمر العدوى في الأنسجة، مما يتسبب في تلف لا رجعة فيه للقلب أو الدماغ. في حالات نادرة، قد يموت الأطفال الصغار بسبب التهاب عضلة القلب أو التهاب السحايا والدماغ أثناء المرحلة الحادة من مرض شاغاس.
بعد المرحلة الحادة هي مرحلة متوسطة طويلة يتم خلالها العثور على عدد قليل من الطفيليات أو عدم وجودها في الدم ومعظم الناس لا تظهر عليهم أعراض. سيظل العديد من المرضى بدون أعراض مدى الحياة؛ ومع ذلك، بعد عقود من التعرض، سيصاب ما يقدر بنحو 20٪ - 30٪ من الأشخاص المصابين بأمراض مزمنة يمكن أن تكون منهكة وأحيانًا مهددة للحياة. في المرحلة المزمنة، قد يصاب المرضى بتورم مؤلم في القولون، مما يؤدي إلى التواء شديد وإمساك وانسداد الأمعاء؛ وتورم مؤلم في المريء، مما يؤدي إلى عسر البلع وسوء التغذية؛ وتضخم القلب الرخو (تضخم القلب)، مما قد يؤدي إلى فشل القلب والموت المفاجئ .
يمكن تأكيد التشخيص من خلال عدة اختبارات مختلفة، بما في ذلك المراقبة المجهرية المباشرة للمثقبيات في الدم، و IFA، و EIAs، و PCR، والاستنبات في الوسائط الاصطناعية. في المناطق الموبوءة، يمكن استخدام التشخيصات الخارجية؛ تتضمن هذه الطريقة السماح لحشرات التقبيل غير المصابة بالتغذية على المريض ثم فحص برازها بحثًا عن وجود T. cruzi.
تعتبر أدوية نيفورتيموx والبنزنيدازول علاجات فعالة خلال المرحلة الحادة من مرض شاغاس. تكون فعالية هذه الأدوية أقل بكثير عندما يكون المرض في المرحلة المزمنة. إن تجنب التعرض لمسببات الأمراض من خلال مكافحة النواقل هو الطريقة الأكثر فعالية للحد من هذا المرض.
التمارين الرياضية\(\PageIndex{3}\)
كيف تصيب حشرات التقبيل البشر بالتريبانوزوما كروزي؟
داء الليشمانيات
على الرغم من تصنيف داء الليشمانيات على أنه من الأمراض غير المعدية، إلا أنه منتشر نسبيًا في المناطق الاستوائية وشبه الاستوائية، ويؤثر على الناس في أكثر من 90 بلدًا. وينجم عن حوالي 20 نوعًا مختلفًا من الليشمانيا والطفيليات الأولية التي تنتقل عن طريق ناقلات ذبابة الرمل مثل Phlebotomus spp. و Lutzomia spp. يمكن أن تعمل الكلاب والقطط والأغنام والخيول وقوارض الماشية والبشر كخزانات.
يتم بلع الليشمانيا بروتوزوان بواسطة البلاعم ولكنه يستخدم عوامل الفوعة لتجنب التدمير داخل البلعمية. تعمل عوامل الضراوة على تثبيط إنزيمات البلعمية التي من شأنها تدمير الطفيل. يتكاثر الطفيل داخل البلاعم، ويحللها، وتصيب السلالة البلاعم الجديدة (انظر الاتصالات الدقيقة: عندما تفشل البلعمة).
الأشكال السريرية الرئيسية الثلاثة لداء الليشمانيات هي الجلد (القرحة الشرقية، وغلي دلهي، وغلي حلب)، والحشوية (الكالازار، وحمى الدمدوم)، والغشاء المخاطي (إسبونديا). أكثر أشكال المرض شيوعًا هو داء الليشمانيات الجلدي، والذي يتميز بتكوين تقرحات في موقع لدغة الحشرات التي قد تبدأ في شكل حطاطات أو عقيدات قبل أن تصبح تقرحات كبيرة (الشكل\(\PageIndex{7}\)).
قد يستغرق ظهور داء الليشمانيات الحشوي شهورًا وأحيانًا سنوات، مما يؤدي إلى تضخم الغدد الليمفاوية والكبد والطحال ونخاع العظام. يؤدي الضرر الذي يلحق بمواقع الجسم هذه إلى الحمى وفقدان الوزن وتورم الطحال والكبد. كما أنه يتسبب في انخفاض عدد خلايا الدم الحمراء (فقر الدم) وخلايا الدم البيضاء (نقص الكريات البيض) والصفائح الدموية (نقص الصفيحات)، مما يجعل المريض يعاني من نقص المناعة وأكثر عرضة للعدوى القاتلة في الرئتين والجهاز الهضمي.
الشكل المخاطي لداء الليشمانيات هو أحد الأشكال الأقل شيوعًا للمرض. يسبب آفة مشابهة للشكل الجلدي ولكن داء الليشمانيات المخاطي يرتبط بالأغشية المخاطية للفم أو القزحية أو البلعوم، ويمكن أن يكون مدمرًا ومشوهًا. يحدث داء الليشمانيات المخاطي بشكل أقل عندما تتم معالجة العدوى الجلدية الأصلية (الجلد) على الفور.
يتم إجراء التشخيص النهائي لداء الليشمانيات عن طريق تصوير الكائنات الحية في مسحات ملطخة بغيمسا، أو عن طريق عزل الكائنات الأولية في الليشمانيا في الثقافات، أو عن طريق اختبارات PCR على الشفاطات من الأنسجة المصابة. يمكن أن تساعد تحقيقات الحمض النووي المحددة أو تحليل الطفيليات المستزرعة في تمييز أنواع الليشمانيا التي تسبب داء الليشمانيات الجلدي البسيط عن الأنواع القادرة على التسبب في داء الليشمانيات المخاطي.
عادة لا يتم علاج داء الليشمانيات الجلدي. ستختفي الآفات بعد أسابيع (أو عدة أشهر)، ولكنها قد تؤدي إلى حدوث ندبات. معدلات التكرار منخفضة لهذا المرض. يمكن علاج الالتهابات الأكثر خطورة باستخدام ستيبوغلوكونات (غلوكونات الأنتيمون) والأمفوتيريسين B والميلتفوزين.

التمارين الرياضية\(\PageIndex{4}\)
قارن بين الأشكال المخاطية والجلدية لداء الليشمانيات.
داء البلهارسيات
داء البلهارسيا (البلهارسيا) هو مرض من الأمراض المنقولة بالاتصال الجنسي الناجم عن تدفقات الدم من جنس البلهارسيا التي تنتمي إلى منطقة البحر الكاريبي وأمريكا الجنوبية والشرق الأوسط وآسيا وأفريقيا. تحدث معظم حالات داء البلهارسيات البشري بسبب البلهارسيا مانسوني أو إس هيماتوبيوم أو S. japonicum. البلهارسيا هي الديدان الخيطية الوحيدة التي تغزو الجلد، بينما تصيب جميع الديدان الخيطية الأخرى عن طريق الابتلاع. تشير تقديرات منظمة الصحة العالمية إلى أن 258 مليون شخص على الأقل احتاجوا إلى العلاج الوقائي لداء البلهارسيات في عام 2014. 9
تقوم الكائنات البشرية المضيفة المصابة بإلقاء بيض البلهارسيا في البول والبراز، الأمر الذي يمكن أن يلوث موائل المياه العذبة للقواقع التي تعمل كمضيف وسيط. يفقس البيض في الماء ويطلق ميراسيديا، وهي مرحلة نمو وسيطة للبلهارسيا التي تصيب القواقع. تنضج الميراسيديا وتتكاثر داخل القواقع، وتتحول إلى سيركاريا تترك الحلزون وتدخل الماء، حيث يمكنها اختراق جلد السباحين والسباحين. تهاجر السيكاريا عبر الأنسجة البشرية وتدخل مجرى الدم، حيث تنضج لتصبح ديدان ذكور وإناث بالغة تتزاوج وتطلق بيضًا مخصبًا. تنتقل البويضات عبر مجرى الدم وتخترق مواقع الجسم المختلفة، بما في ذلك المثانة أو الأمعاء، حيث يتم إفرازها في البول أو البراز لبدء دورة الحياة مرة أخرى (الشكل 5.2.4).
بعد بضعة أيام من الإصابة، قد يصاب المرضى بطفح جلدي أو حكة في الجلد مرتبطة بموقع تغلغل السركاريا. في غضون شهر إلى شهرين من الإصابة، قد تظهر الأعراض، بما في ذلك الحمى والقشعريرة والسعال والألم العضلي، حيث أن البويضات التي لا تفرز تنتشر عبر الجسم. بعد سنوات من العدوى، تستقر البويضات في الأنسجة وتسبب الالتهاب والندبات التي يمكن أن تلحق الضرر بالكبد والجهاز العصبي المركزي والأمعاء والطحال والرئتين والمثانة. قد يسبب هذا ألمًا في البطن وتضخم الكبد ودم في البول أو البراز ومشاكل في التبول. ترتبط زيادة خطر الإصابة بسرطان المثانة أيضًا بعدوى البلهارسيا المزمنة. بالإضافة إلى ذلك، يمكن للأطفال المصابين بشكل متكرر أن يصابوا بسوء التغذية وفقر الدم وصعوبات التعلم.
يتم تشخيص داء البلهارسيات من خلال الملاحظة المجهرية للبيض في البراز أو البول أو عينات أنسجة الأمعاء أو المثانة أو الاختبارات المصلية. عقار برازيكوانتيل فعال لعلاج جميع التهابات البلهارسيا. يمكن أن يساعد تحسين إدارة مياه الصرف الصحي وتثقيف السكان المعرضين للخطر للحد من التعرض للمياه الملوثة في السيطرة على انتشار المرض.
التهاب الجلد العنقي
يمكن أن تتحول سيركاريا بعض أنواع البلهارسيا فقط إلى ديدان بالغة وتكمل دورة حياتها في الحيوانات المضيفة مثل الطيور المهاجرة والثدييات. لا تزال سيركاريا هذه الديدان قادرة على اختراق جلد الإنسان، لكنها غير قادرة على إثبات عدوى منتجة في الأنسجة البشرية. ومع ذلك، فإن وجود سيركاريا في الأوعية الدموية الصغيرة يحفز الاستجابة المناعية، مما يؤدي إلى ظهور نتوءات بارزة مثيرة للحكة تسمى التهاب الجلد العنقي (المعروف أيضًا باسم حكة السباح أو حكة حفار المحار). على الرغم من أنه غير مريح، فإن التهاب الجلد العنقي عادةً ما يكون مقيدًا ذاتيًا ونادرًا ما يكون خطيرًا. يمكن استخدام مضادات الهيستامين ومضادات الحكة للحد من الالتهاب والحكة، على التوالي.
التمارين الرياضية\(\PageIndex{5}\)
كيف تحدث عدوى البلهارسيا في البشر؟
مسببات الأمراض الشائعة حقيقية النواة في الدورة الدموية البشرية
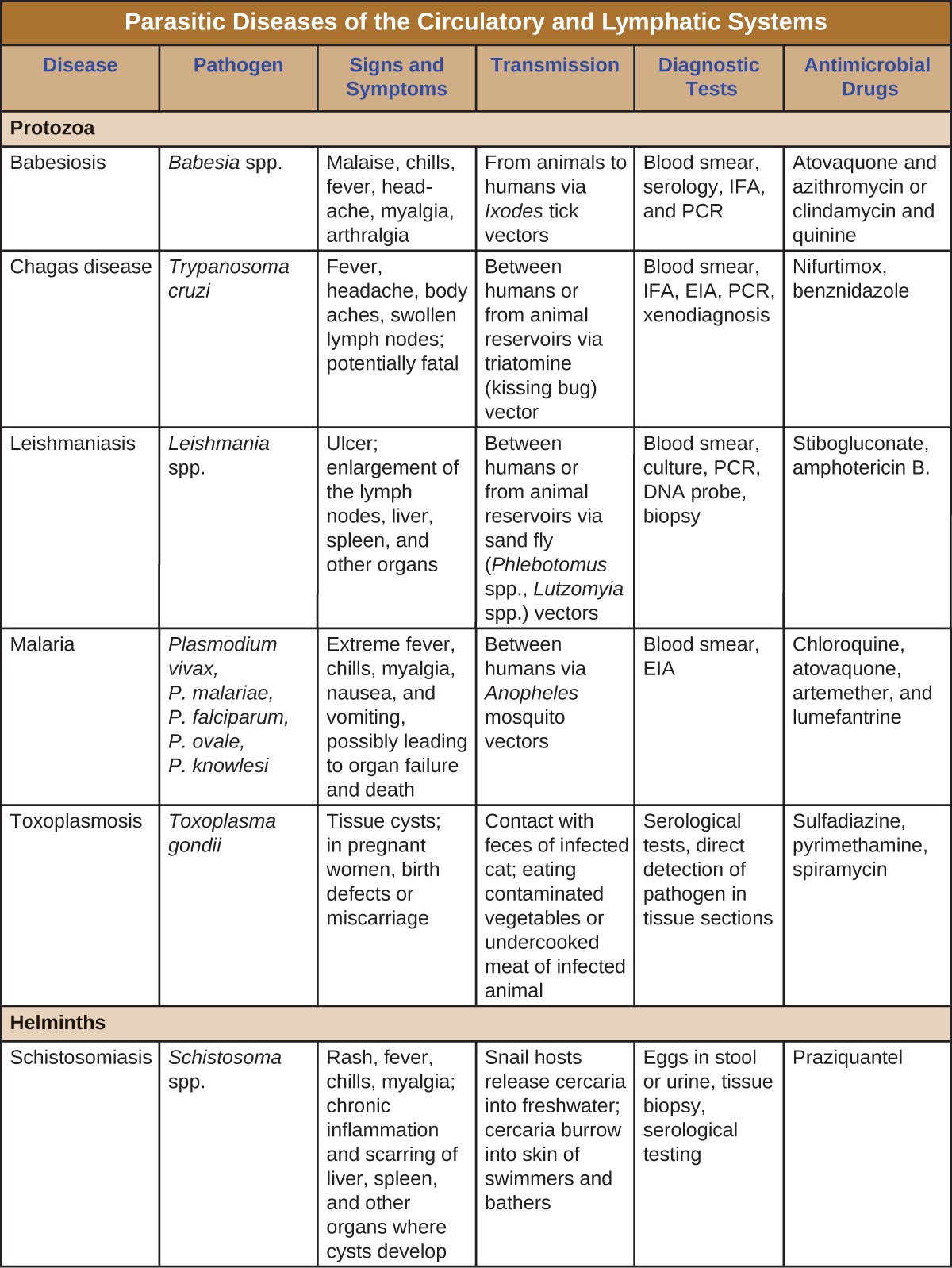
تنتشر عدوى البروتوزوان والديدان الطفيلية في العالم النامي. تم تلخيص عدد قليل من الإصابات الطفيلية الأكثر أهمية في الشكل\(\PageIndex{8}\).
على الرغم من استمرار العلاج بالمضادات الحيوية وإزالة القسطرة الوريدية، انخفضت حالة باربرا بشكل أكبر. بدأت تظهر عليها علامات الصدمة وانخفض ضغط دمها إلى 77/50 ملم زئبق. تم إعطاء الأدوية المضادة للالتهابات والدروتريكوجين ألفا لمكافحة الإنتان. ومع ذلك، بحلول اليوم السابع من دخول المستشفى، تعرضت باربرا لفشل كبدي وكلوي وتوفيت.
على الأرجح شكلت المكورات العنقودية الذهبية فيلمًا حيويًا على سطح قسطرة باربرا. من هناك، تم إلقاء البكتيريا بشكل مزمن في الدورة الدموية وإنتاج الأعراض السريرية الأولية. فشلت علاجات العلاج الكيميائي في جزء كبير منها بسبب عزل MRSA المقاوم للأدوية. كما تدخلت عوامل ضراوة مثل الليوكوسيدين والهيموليزين في استجابتها المناعية. قد يكون الانخفاض النهائي لباربرا نتيجة لإنتاج السموم المعوية وتوكسين متلازمة الصدمة السامة (TSST)، والتي يمكن أن تسبب صدمة سامة.
تعتبر القسطرة الوريدية من التدخلات الشائعة المنقذة للحياة للعديد من المرضى الذين يحتاجون إلى تناول الأدوية أو السوائل على المدى الطويل. ومع ذلك، فهي أيضًا مواقع شائعة لعدوى مجرى الدم. تقدر منظمة الصحة العالمية أن هناك ما يصل إلى 80,000 حالة عدوى في مجرى الدم مرتبطة بالقسطرة كل عام في الولايات المتحدة، مما يؤدي إلى حوالي 20,000 حالة وفاة. 10
المفاهيم الأساسية والملخص
- الملاريا هي طفيل أولي يظل سببًا مهمًا للوفاة في المقام الأول في المناطق الاستوائية. هناك عدة أنواع في جنس Plasmodium مسؤولة عن الملاريا وتنتقل جميعها عن طريق بعوض Anopheles. يصيب البلازموديوم خلايا الدم الحمراء البشرية ويدمرها، مما يؤدي إلى تلف الأعضاء وفقر الدم ونخر الأوعية الدموية والموت. يمكن علاج الملاريا بالعديد من الأدوية المضادة للملاريا والوقاية منها من خلال مكافحة ناقلات الأمراض.
- داء المقوسات هو عدوى أولية منتشرة يمكن أن تسبب التهابات خطيرة في الأشخاص الذين يعانون من نقص المناعة وفي الأجنة النامية. القطط المنزلية هي المضيف النهائي.
- داء البابيزيا هو عدوى لا تظهر عليها أعراض بشكل عام تصيب خلايا الدم الحمراء ويمكن أن تسبب أعراضًا تشبه الملاريا لدى كبار السن أو الذين يعانون من نقص المناعة أو مرضى نقص المناعة.
- مرض شاغاس هو مرض استوائي ينتقل عن طريق بق الترياتومين. يصيب المثقبيات القلب والأنسجة العصبية والخلايا الأحادية والخلايا البلعمية، وغالبًا ما يظل كامنًا لسنوات عديدة قبل أن يتسبب في أضرار خطيرة ومميتة أحيانًا للجهاز الهضمي والقلب.
- يحدث داء الليشمانيات بسبب الليشمانيا الأولية وينتقل عن طريق ذباب الرمل. تكون الأعراض خفيفة بشكل عام، ولكن الحالات الخطيرة قد تسبب تلف الأعضاء وفقر الدم وفقدان الكفاءة المناعية.
- يحدث داء البلهارسيات بسبب صدفة تنتقل عن طريق القواقع. ينتقل الحظ في جميع أنحاء الجسم في مجرى الدم ويصيب الأنسجة المختلفة بشكل مزمن، مما يؤدي إلى تلف الأعضاء.
الحواشي
- 1 منظمة الصحة العالمية. «تقرير الملاريا العالمي 2015: ملخص». 2015. http://www.who.int/malaria/publicati...015/report/en/. تم الوصول إليه في 28 يوليو 2016.
- 2 صباحًا تينتر وآخرون. «التوكسوبلازما جوندي: من الحيوانات إلى البشر». المجلة الدولية لعلم الطفيليات 30 رقم 12-13 (2000): 1217-1258.
- 3 مراكز للسيطرة على الأمراض والوقاية منها. «الطفيليات - داء المقوسات (عدوى التوكسوبلازما). علم الأوبئة وعوامل الخطر.» 2015 http://www.cdc.gov/parasites/toxoplasmosis/epi.html. تم الوصول إليه في 28 يوليو 2016.
- 4 جيه فليجر. «آثار التوكسوبلازما على السلوك البشري». نشرة الفصام 33، رقم 3 (2007): 757-760.
- 5 المرجع نفسه
- 6 مراكز للسيطرة على الأمراض والوقاية منها. «الطفيليات - داء المقوسات (عدوى التوكسوبلازما). الأسئلة الشائعة حول داء المقوسات». 2013. http://www.cdc.gov/parasites/toxopla...info/faqs.html. تم الوصول إليه في 28 يوليو 2016.
- 7 منظمة الصحة العالمية. «مرض شاغاس (داء المثقبيات الأمريكي). ورقة حقائق.» 2016. http://www.who.int/mediacentre/factsheets/fs340/en/. تم الوصول إليه في 29 يوليو 2016.
- 8 سي إي ريزنمان وآخرون. «عدوى حشرات التقبيل بمرض التريبانوسوما كروزي، توكسون، أريزونا، الولايات المتحدة الأمريكية.» الأمراض المعدية الناشئة 16 رقم 3 (2010): 400-405.
- 9 منظمة الصحة العالمية. «داء البلهارسيات». ورقة حقائق.» 2016. http://www.who.int/mediacentre/factsheets/fs115/en/. تم الوصول إليه في 29 يوليو 2016.
- 10 منظمة الصحة العالمية. «سلامة المرضى والوقاية من التهابات مجرى الدم من القسطرة الوريدية للخط المركزي». 2016. www.who.int/patientsafety/imp... tation/bsi/en/. تم الوصول إليه في 29 يوليو 2016.


