17.1: الفيروسات
- Page ID
- 191296
لا أحد يعرف بالضبط متى ظهرت الفيروسات أو من أين أتت، لأن الفيروسات لا تترك آثارًا تاريخية مثل الحفريات. يُعتقد أن الفيروسات الحديثة عبارة عن فسيفساء من أجزاء وقطع من الأحماض النووية تم التقاطها من مصادر مختلفة على طول مسارات التطور الخاصة بكل منها. الفيروسات هي كيانات طفيلية غير خلوية لا يتم تصنيفها ضمن أي مجال لأنها لا تعتبر حية. لا تحتوي على غشاء بلازما أو عضيات داخلية أو عمليات أيضية، ولا تنقسم. بدلاً من ذلك، فإنها تصيب الخلية المضيفة وتستخدم عمليات النسخ المتماثل للمضيف لإنتاج جزيئات فيروس النسل. تصيب الفيروسات جميع أشكال الكائنات الحية بما في ذلك البكتيريا والعرايا والفطريات والنباتات والحيوانات. تنمو الكائنات الحية وتستقلب وتتكاثر. تتكاثر الفيروسات، ولكن للقيام بذلك، فإنها تعتمد كليًا على الخلايا المضيفة لها. لا يتم استقلابها أو نموها، ولكن يتم تجميعها في شكلها الناضج.

الفيروسات متنوعة. وهي تختلف في بنيتها وطرق النسخ المتماثل الخاصة بها وفي المضيفين المستهدفين أو حتى الخلايا المضيفة. في حين يمكن فهم معظم التنوع البيولوجي من خلال التاريخ التطوري، مثل كيفية تكيف الأنواع مع الظروف والبيئات، لا يزال الكثير عن أصول الفيروسات وتطورها غير معروف.
كيف تتكاثر الفيروسات
تم اكتشاف الفيروسات لأول مرة بعد تطوير مرشح خزفي، يسمى مرشح Chamberland-Pasteur، والذي يمكنه إزالة جميع البكتيريا المرئية تحت المجهر من أي عينة سائلة. في عام 1886، أثبت أدولف ماير أن مرض نباتات التبغ، وهو مرض فسيفساء التبغ، يمكن أن ينتقل من نبات مريض إلى نبات صحي من خلال المستخلصات النباتية السائلة. في عام 1892، أظهر دميتري إيفانوفسكي أن هذا المرض يمكن أن ينتقل بهذه الطريقة حتى بعد أن أزال مرشح Chamberland-Pasteur جميع البكتيريا القابلة للحياة من المستخلص. ومع ذلك، فقد مرت سنوات عديدة قبل إثبات أن هذه العوامل المعدية «القابلة للفلترة» لم تكن مجرد بكتيريا صغيرة جدًا ولكنها كانت نوعًا جديدًا من الجسيمات الصغيرة المسببة للأمراض.
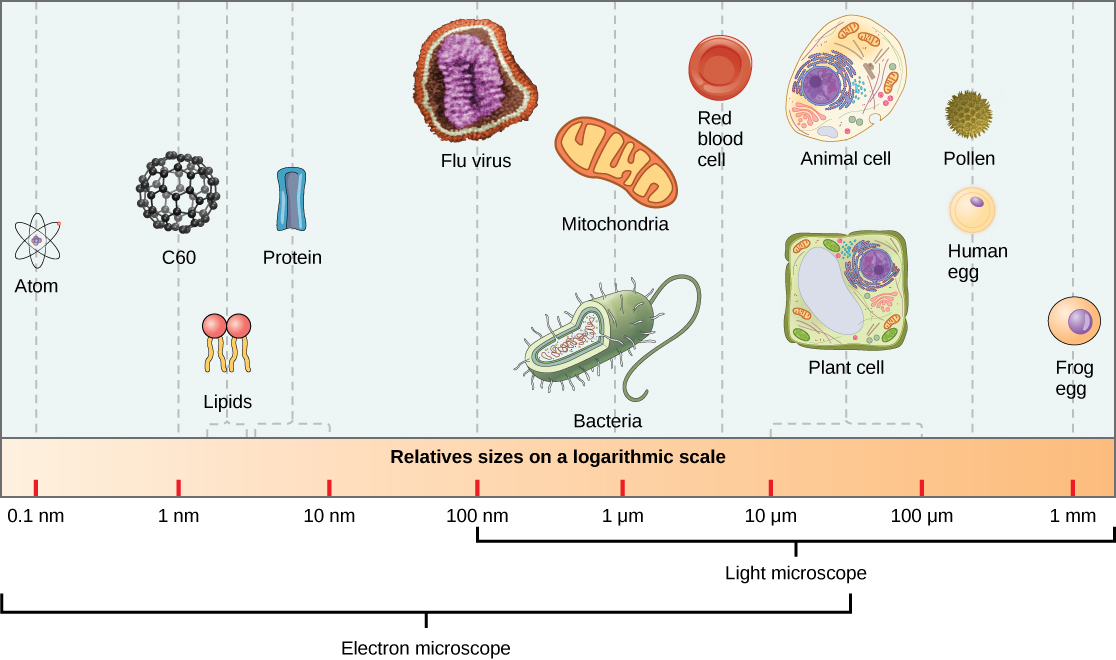
الفيروسات، وهي جزيئات أحادية الفيروس، صغيرة جدًا، حوالي 20-250 نانومتر (1 نانومتر = 1/1،000،000 مم). جزيئات الفيروس الفردية هذه هي الشكل المعدي للفيروس خارج الخلية المضيفة. على عكس البكتيريا (التي يبلغ حجمها حوالي 100 مرة)، لا يمكننا رؤية الفيروسات باستخدام المجهر الضوئي، باستثناء بعض الفيروسات الكبيرة من عائلة فيروس الجدري (الشكل\(\PageIndex{2}\)).
لم يحصل العلماء على أول رؤية جيدة لبنية فيروس فسيفساء التبغ (الشكل\(\PageIndex{1}\)) وغيرها حتى تطور المجهر الإلكتروني في الأربعينيات. يمكن ملاحظة البنية السطحية للفيريونات من خلال المسح والفحص المجهري الإلكتروني للإرسال، في حين لا يمكن ملاحظة الهياكل الداخلية للفيروس إلا في الصور من المجهر الإلكتروني المرسل (الشكل\(\PageIndex{3}\)).
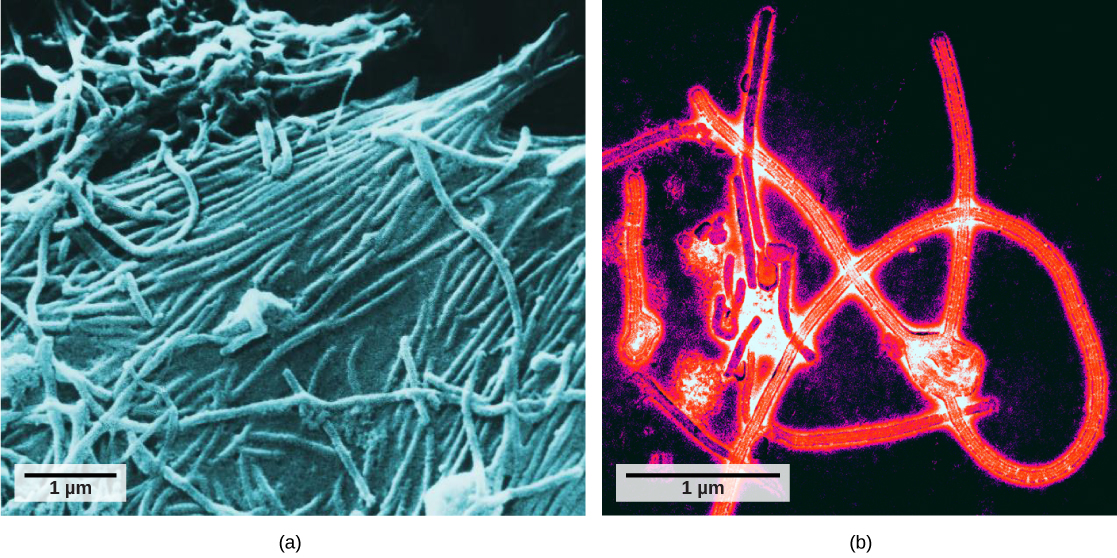
وقد سمح استخدام هذه التكنولوجيا باكتشاف العديد من الفيروسات من جميع أنواع الكائنات الحية. تم تجميعها في البداية حسب الشكل المورفولوجي المشترك، مما يعني حجمها وشكلها وهياكلها المميزة. في وقت لاحق، تم تصنيف مجموعات الفيروسات حسب نوع الحمض النووي الذي تحتويه، الحمض النووي أو الحمض النووي الريبي، وما إذا كان حمضها النووي أحادي أو مزدوج. وفي الآونة الأخيرة، أدى التحليل الجزيئي لدورات التكاثر الفيروسي إلى زيادة تحسين تصنيفها.
يتكون الفيريون من نواة الحمض النووي، وطبقة خارجية من البروتين، وأحيانًا غلاف خارجي مصنوع من البروتين وأغشية الفوسفوليبيد المشتقة من الخلية المضيفة. الفرق الأكثر وضوحًا بين أفراد العائلات الفيروسية هو مورفولوجيتهم، وهي متنوعة تمامًا. ميزة مثيرة للاهتمام للتعقيد الفيروسي هي أن تعقيد المضيف لا يرتبط بتعقيد الفيروس. يتم ملاحظة بعض هياكل الفيريون الأكثر تعقيدًا في البكتيريا والفيروسات التي تصيب أبسط الكائنات الحية والبكتيريا.
تأتي الفيروسات بأشكال وأحجام عديدة، ولكنها متسقة ومتميزة لكل عائلة فيروسية (الشكل\(\PageIndex{4}\)). تحتوي جميع الفيروسات على جينوم الحمض النووي المغطى بطبقة واقية من البروتين تسمى القفيصة. يتكون الكابسيد من وحدات بروتينية فرعية تسمى الكابسوميرات. بعض القبضات الفيروسية عبارة عن «كرات» بسيطة متعددة السطوح، في حين أن البعض الآخر معقد جدًا في التركيب. يُطلق على البنية الخارجية المحيطة بقفصة بعض الفيروسات اسم الغلاف الفيروسي. تستخدم جميع الفيروسات نوعًا من البروتين السكري للارتباط بالخلايا المضيفة في جزيئات على الخلية تسمى المستقبلات الفيروسية. يستغل الفيروس جزيئات سطح الخلية هذه، التي تستخدمها الخلية لغرض آخر، كطريقة للتعرف على أنواع معينة من الخلايا وإصابتها. على سبيل المثال، يستخدم فيروس الحصبة بروتينًا سكري على سطح الخلية في البشر يعمل عادةً في التفاعلات المناعية وربما في تفاعل الحيوانات المنوية مع البويضة عند الإخصاب. يعد التعلق أحد متطلبات الفيروسات لاختراق غشاء الخلية لاحقًا وحقن الجينوم الفيروسي وإكمال تكراره داخل الخلية.
تعد بكتيريا T4، التي تصيب بكتيريا E. coli، من بين الفيروسات الأكثر تعقيدًا المعروفة؛ يحتوي T4 على بنية ذيل بروتينية يستخدمها الفيروس للارتباط بالخلية المضيفة وهيكل الرأس الذي يحتوي على الحمض النووي الخاص به.
يستخدم الفيروس الغدي، وهو فيروس حيواني غير مغلف يسبب أمراض الجهاز التنفسي لدى البشر، طفرات بروتينية بارزة من غلافاته للالتصاق بالخلية المضيفة. تشمل الفيروسات غير المغلفة أيضًا تلك التي تسبب شلل الأطفال (فيروس شلل الأطفال) والثآليل الأخمصية (فيروس الورم الحليمي) والتهاب الكبد A (فيروس التهاب الكبد A). تميل الفيروسات غير المغلفة إلى أن تكون أكثر قوة وأكثر عرضة للبقاء على قيد الحياة في ظل ظروف قاسية، مثل القناة الهضمية.
تتكون الفيروسات المغلفة مثل فيروس نقص المناعة البشرية (HIV)، العامل المسبب لمرض الإيدز (متلازمة نقص المناعة المكتسب)، من الحمض النووي (RNA في حالة فيروس نقص المناعة البشرية) وبروتينات القفيصة المحاطة بغلاف ثنائي الطبقة الفوسفورية والبروتينات المرتبطة به (الشكل\(\PageIndex{4}\)). يعد الجدري والأنفلونزا والنكاف أمثلة على الأمراض التي تسببها الفيروسات ذات المغلفات. بسبب هشاشة الغلاف، تكون الفيروسات غير المغلفة أكثر مقاومة للتغيرات في درجة الحرارة ودرجة الحموضة وبعض المطهرات من الفيروسات المغلفة.
بشكل عام، لا يخبرنا شكل الفيريون ووجود أو عدم وجود غلاف إلا القليل عن الأمراض التي قد تسببها الفيروسات أو الأنواع التي قد تصيبها، ولكنها لا تزال وسيلة مفيدة لبدء التصنيف الفيروسي.
آرت كونيكشن
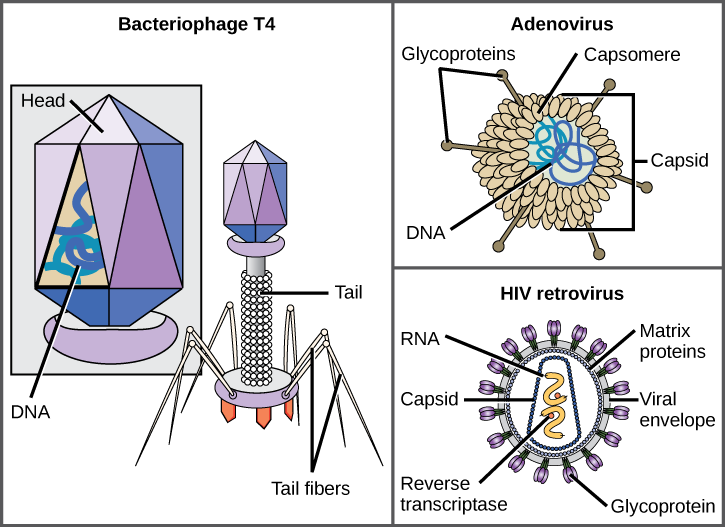
أي من العبارات التالية حول بنية الفيروسات صحيحة؟
- جميع الفيروسات مغلفة بغشاء فيروسي.
- يتكون الكابسومير من وحدات بروتينية صغيرة تسمى الكابسيدات.
- الحمض النووي هو المادة الوراثية في جميع الفيروسات.
- تساعد البروتينات السكرية الفيروس على الالتصاق بالخلية المضيفة.
على عكس جميع الكائنات الحية التي تستخدم الحمض النووي كمادة وراثية، قد تستخدم الفيروسات إما الحمض النووي أو الحمض النووي الريبي كمادة لها. يحتوي جوهر الفيروس على الجينوم أو المحتوى الجيني الكلي للفيروس. تميل الجينومات الفيروسية إلى أن تكون صغيرة مقارنة بالبكتيريا أو حقيقيات النوى، وتحتوي فقط على تلك الجينات التي ترمز للبروتينات التي لا يستطيع الفيروس الحصول عليها من الخلية المضيفة. قد تكون هذه المادة الجينية أحادية الجديلة أو مزدوجة الجديلة. قد تكون أيضًا خطية أو دائرية. في حين أن معظم الفيروسات تحتوي على شريحة واحدة من الحمض النووي، فإن البعض الآخر يحتوي على جينومات تتكون من عدة أجزاء.
تحتوي فيروسات الحمض النووي على جوهر الحمض النووي. يقوم الحمض النووي الفيروسي بتوجيه بروتينات النسخ المتماثل للخلية المضيفة لتجميع نسخ جديدة من الجينوم الفيروسي ونسخ وترجمة هذا الجينوم إلى بروتينات فيروسية. تسبب فيروسات الحمض النووي أمراضًا بشرية مثل الجدري والتهاب الكبد B وبعض الأمراض التناسلية مثل الهربس والثآليل التناسلية.
تحتوي فيروسات RNA على RNA فقط في نواتها. لتكرار جينوماتها في الخلية المضيفة، تقوم جينومات فيروسات الحمض النووي الريبي بترميز الإنزيمات غير الموجودة في الخلايا المضيفة. إنزيمات بوليميراز الحمض النووي الريبي ليست مستقرة مثل بوليميرات الحمض النووي وغالبًا ما ترتكب أخطاء أثناء النسخ. لهذا السبب، تحدث الطفرات والتغيرات في تسلسل النيوكليوتيد في فيروسات الحمض النووي الريبي بشكل متكرر أكثر من فيروسات الحمض النووي. هذا يؤدي إلى مزيد من التطور السريع والتغيير في فيروسات RNA. على سبيل المثال، حقيقة أن الأنفلونزا هي فيروس RNA هي أحد أسباب الحاجة إلى لقاح إنفلونزا جديد كل عام. تشمل الأمراض البشرية التي تسببها فيروسات الحمض النووي الريبي التهاب الكبد C والحصبة وداء الكلب.
يمكن اعتبار الفيروسات طفيليات إلزامية داخل الخلايا. يجب أن يلتصق الفيروس بخلية حية، وأن يتم أخذه إلى الداخل، وتصنيع البروتينات ونسخ الجينوم الخاص به، وإيجاد طريقة للهروب من الخلية حتى يتمكن الفيروس من إصابة خلايا أخرى وفي النهاية أفراد آخرين. يمكن للفيروسات أن تصيب أنواعًا معينة فقط من المضيفين وخلايا معينة فقط داخل هذا المضيف. الأساس الجزيئي لهذه الخصوصية هو أنه يجب العثور على جزيء سطحي معين، يعرف باسم المستقبل الفيروسي، على سطح الخلية المضيفة حتى يلتصق الفيروس. كما أن الاختلافات الأيضية التي تظهر في أنواع الخلايا المختلفة بناءً على التعبير الجيني التفاضلي هي عامل محتمل للخلايا التي قد يستخدمها الفيروس لتكرارها. يجب أن تصنع الخلية المواد التي يحتاجها الفيروس، مثل الإنزيمات التي لا يحتوي جينوم الفيروس نفسه على جينات لها، أو لن يتمكن الفيروس من التكاثر باستخدام تلك الخلية.
خطوات الإصابة بالفيروسات
يجب أن «يستولي» الفيروس على خلية لتكرارها. يمكن أن تنتج دورة التكاثر الفيروسي تغييرات بيوكيميائية وهيكلية جذرية في الخلية المضيفة، مما قد يتسبب في تلف الخلايا. يمكن لهذه التغييرات، التي تسمى تأثيرات الاعتلال الخلوي، تغيير وظائف الخلية أو حتى تدمير الخلية. تموت بعض الخلايا المصابة، مثل تلك المصابة بفيروس البرد الشائع (فيروس الأنف)، من خلال التحلل (الانفجار) أو موت الخلايا المبرمج (موت الخلايا المبرمج أو «انتحار الخلية»)، مما يؤدي إلى إطلاق جميع فيروسات النسل في وقت واحد. تنجم أعراض الأمراض الفيروسية عن الاستجابة المناعية للفيروس، الذي يحاول السيطرة على الفيروس والقضاء عليه من الجسم، ومن تلف الخلايا الناجم عن الفيروس. تغادر العديد من الفيروسات الحيوانية، مثل فيروس نقص المناعة البشرية (HIV)، الخلايا المصابة في الجهاز المناعي من خلال عملية تعرف باسم التبرعم، حيث تغادر الفيروسات الخلية بشكل فردي. أثناء عملية التبرعم، لا تخضع الخلية للتحلل ولا تُقتل على الفور. ومع ذلك، فإن الضرر الذي يلحق بالخلايا التي يصيبها فيروس نقص المناعة البشرية قد يجعل من المستحيل على الخلايا أن تعمل كوسيط للمناعة، على الرغم من أن الخلايا تظل حية لفترة من الوقت. تتبع معظم حالات العدوى الفيروسية المنتجة خطوات مماثلة في دورة تكرار الفيروس: التعلق والاختراق وفك الطلاء والتكرار والتجميع والإطلاق.
يرتبط الفيروس بموقع مستقبل معين على غشاء الخلية المضيفة من خلال بروتينات التعلق في الغلاف أو البروتينات المضمنة في غلافه. المرفق محدد، وعادة ما يرتبط الفيروس فقط بخلايا نوع واحد أو عدد قليل من الأنواع وأنواع خلايا معينة فقط داخل تلك الأنواع مع المستقبلات المناسبة.
مفهوم في العمل
شاهد هذا الفيديو للحصول على شرح مرئي لكيفية هجوم الأنفلونزا على الجسم.
على عكس الفيروسات الحيوانية، يتم حقن الحمض النووي للبكتيريا في الخلية المضيفة عارية، تاركًا القفيصة خارج الخلية. يمكن للفيروسات النباتية والحيوانية أن تدخل خلاياها من خلال إندوسيتوسيس، حيث يحيط غشاء الخلية بالفيروس بأكمله ويبتلعه. تدخل بعض الفيروسات المغلفة الخلية عندما يندمج الغلاف الفيروسي مباشرة مع غشاء الخلية. بمجرد دخول الخلية، يتحلل الغطاء الفيروسي ويتم إطلاق الحمض النووي الفيروسي، والذي يصبح بعد ذلك متاحًا للتكرار والنسخ.
تعتمد آلية النسخ المتماثل على الجينوم الفيروسي. عادةً ما تستخدم فيروسات الحمض النووي بروتينات الخلايا المضيفة والإنزيمات لإنتاج حمض نووي إضافي يُستخدم لنسخ الجينوم أو يتم نسخه إلى الحمض النووي الريبي المرسل (mRNA)، والذي يستخدم بعد ذلك في تخليق البروتين. عادةً ما تستخدم فيروسات RNA، مثل فيروس الأنفلونزا، نواة RNA كنموذج لتوليف الحمض النووي الريبي الجيني الفيروسي و mRNA. تتم ترجمة mRNA الفيروسي إلى إنزيمات فيروسية وبروتينات قفيصة لتجميع فيروسات جديدة (الشكل\(\PageIndex{5}\)). بالطبع، هناك استثناءات لهذا النمط. إذا لم توفر الخلية المضيفة الإنزيمات اللازمة للتكاثر الفيروسي، فإن الجينات الفيروسية توفر المعلومات للتوليف المباشر للبروتينات المفقودة. تحتوي الفيروسات القهقرية، مثل فيروس نقص المناعة البشرية، على جينوم الحمض النووي الريبي الذي يجب نسخه عكسيًا لصنع الحمض النووي، والذي يتم إدخاله بعد ذلك في الحمض النووي للمضيف. لتحويل الحمض النووي الريبي إلى الحمض النووي، تحتوي الفيروسات القهقرية على جينات تقوم بتشفير النسخ العكسي للإنزيم الخاص بالفيروس الذي ينسخ قالب الحمض النووي الريبي إلى الحمض النووي. إن حقيقة أن فيروس نقص المناعة البشرية ينتج بعض الإنزيمات الخاصة به، والتي لا توجد في المضيف، سمحت للباحثين بتطوير أدوية تثبط هذه الإنزيمات. تمنع هذه الأدوية، بما في ذلك مثبط النسخ العكسي AZT، تكاثر فيروس نقص المناعة البشرية عن طريق تقليل نشاط الإنزيم دون التأثير على عملية التمثيل الغذائي للمضيف.
المرحلة الأخيرة من التكاثر الفيروسي هي إطلاق الفيروسات الجديدة في الكائن الحي المضيف، حيث تكون قادرة على إصابة الخلايا المجاورة وتكرار دورة النسخ المتماثل. يتم إطلاق بعض الفيروسات عندما تموت الخلية المضيفة ويمكن للفيروسات الأخرى أن تترك الخلايا المصابة عن طريق التبرعم عبر الغشاء دون قتل الخلية مباشرة.
آرت كونيكشن
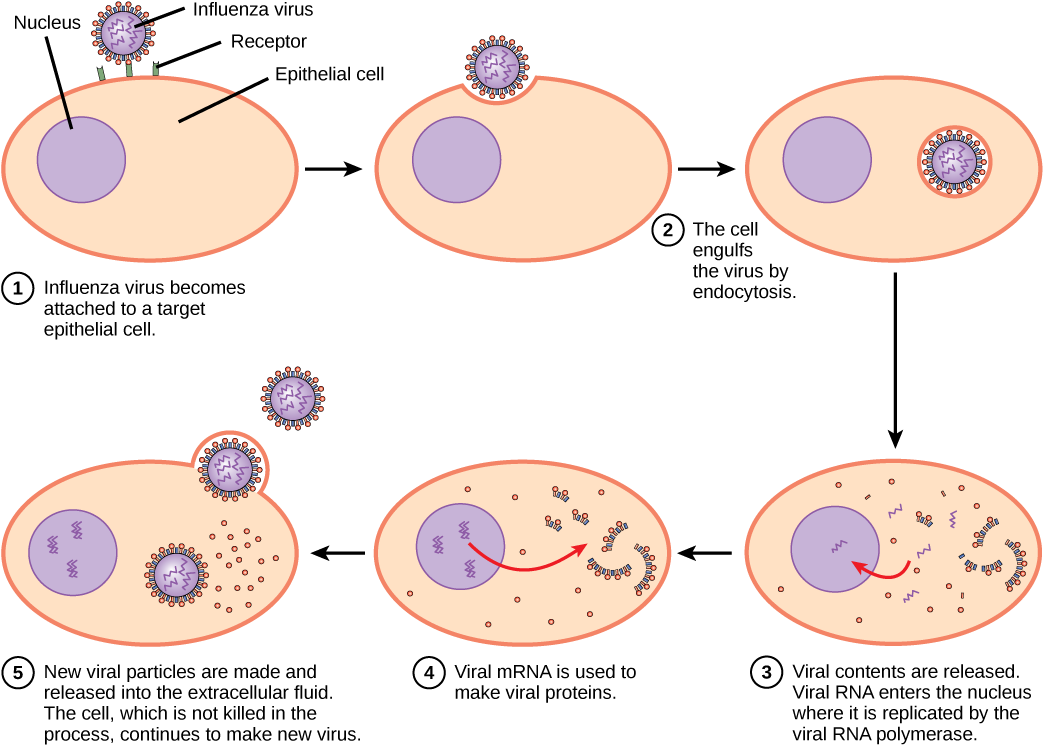
يتم تعبئة فيروس الإنفلونزا في غلاف فيروسي يندمج مع غشاء البلازما. بهذه الطريقة، يمكن للفيروس الخروج من الخلية المضيفة دون قتلها. ما الميزة التي يكتسبها الفيروس من خلال الحفاظ على الخلية المضيفة حية؟
مفهوم في العمل
انقر فوق هذا البرنامج التعليمي حول الفيروسات لتحديد الهياكل وأنماط الإرسال والنسخ المتماثل والمزيد.
الفيروسات والأمراض
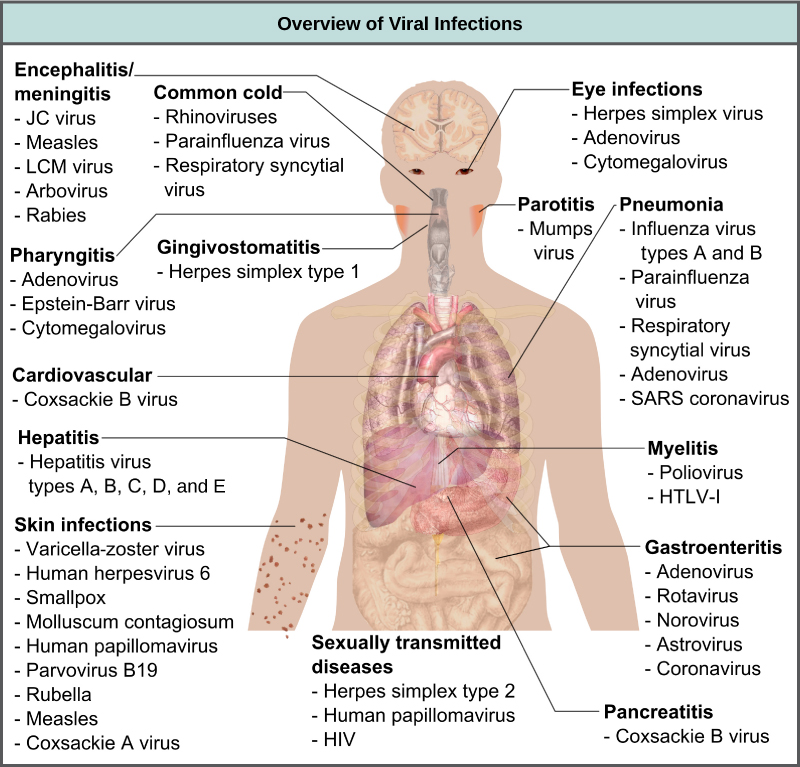
تسبب الفيروسات مجموعة متنوعة من الأمراض في الحيوانات، بما في ذلك البشر، تتراوح من نزلات البرد إلى الأمراض القاتلة المحتملة مثل التهاب السحايا (الشكل\(\PageIndex{6}\)). يمكن علاج هذه الأمراض عن طريق الأدوية المضادة للفيروسات أو اللقاحات، ولكن بعض الفيروسات، مثل فيروس نقص المناعة البشرية، قادرة على تجنب الاستجابة المناعية والتحور حتى تصبح مقاومة للأدوية المضادة للفيروسات.
لقاحات للوقاية
في حين أن لدينا عددًا محدودًا من الأدوية الفعالة المضادة للفيروسات، مثل تلك المستخدمة لعلاج فيروس نقص المناعة البشرية والإنفلونزا، فإن الطريقة الأساسية للسيطرة على المرض الفيروسي هي التطعيم، الذي يهدف إلى منع تفشي المرض من خلال بناء المناعة ضد فيروس أو عائلة فيروسات. يمكن تحضير اللقاح باستخدام فيروسات حية ضعيفة أو فيروسات قاتلة أو وحدات فرعية جزيئية من الفيروس. بشكل عام، تؤدي الفيروسات الحية إلى مناعة أفضل، ولكن لديها إمكانية التسبب في المرض بتردد منخفض. اللقاح الفيروسي القاتل وفيروسات الوحدة الفرعية كلاهما غير قادرين على التسبب في المرض، ولكن بشكل عام يؤديان إلى مناعة أقل فعالية أو طويلة الأمد.
تم تصميم اللقاحات الفيروسية الحية الضعيفة في المختبر لإحداث أعراض قليلة لدى المتلقين مع منحهم مناعة ضد العدوى المستقبلية. كان شلل الأطفال أحد الأمراض التي تمثل علامة فارقة في استخدام اللقاحات. أدت حملات التحصين الجماعية في الولايات المتحدة في الخمسينيات (اللقاح المقتول) والستينيات (اللقاح الحي) إلى القضاء بشكل أساسي على المرض، مما تسبب في شلل العضلات لدى الأطفال وأثار الخوف لدى عامة السكان عند حدوث الأوبئة الإقليمية. مهد نجاح لقاح شلل الأطفال الطريق للتوزيع الروتيني للقاحات للأطفال ضد الحصبة والنكاف والحصبة الألمانية وجدري الماء وأمراض أخرى.
عادة ما يتم تصنيع اللقاحات الحية عن طريق تخفيف (إضعاف) الفيروس «البري» (المسبب للمرض) عن طريق زراعته في المختبر في الأنسجة أو في درجات حرارة مختلفة عما اعتاد عليه الفيروس في المضيف. على سبيل المثال، قد ينمو الفيروس في خلايا في أنبوب اختبار، في أجنة الطيور، أو في الحيوانات الحية. يؤدي التكيف مع هذه الخلايا الجديدة أو درجة الحرارة إلى حدوث طفرات في جينومات الفيروس، مما يسمح لها بالنمو بشكل أفضل في المختبر مع تثبيط قدرتها على التسبب في المرض عند إعادة إدخالها في الحالات الموجودة في المضيف. وبالتالي لا تزال هذه الفيروسات الموهنة تسبب العدوى، لكنها لا تنمو بشكل جيد، مما يسمح للاستجابة المناعية بالتطور في الوقت المناسب للوقاية من الأمراض الرئيسية. إن خطر استخدام اللقاحات الحية، التي عادة ما تكون أكثر فعالية من اللقاحات القاتلة، هو الخطر المنخفض ولكن الكبير المتمثل في عودة هذه الفيروسات إلى شكلها المسبب للمرض عن طريق الطفرات الخلفية. تحدث الطفرات الخلفية عندما يخضع اللقاح لطفرات في المضيف بحيث يتكيف مع المضيف ويمكن أن يسبب المرض مرة أخرى، والذي يمكن أن ينتشر بعد ذلك إلى البشر الآخرين في حالة الوباء. حدث هذا مؤخرًا في عام 2007 في نيجيريا حيث أدت الطفرات في لقاح شلل الأطفال إلى وباء شلل الأطفال في ذلك البلد.
بعض اللقاحات قيد التطوير المستمر لأن بعض الفيروسات، مثل الأنفلونزا وفيروس نقص المناعة البشرية، لديها معدل طفرة مرتفع مقارنة بالفيروسات الأخرى أو الخلايا المضيفة. في حالة الإنفلونزا، تساعد الطفرة في جينات الجزيئات السطحية الفيروس على تجنب المناعة الوقائية التي ربما تم الحصول عليها في موسم الإنفلونزا السابق، مما يجعل من الضروري للأفراد الحصول على التطعيم كل عام. أما الفيروسات الأخرى، مثل تلك التي تسبب أمراض الطفولة مثل الحصبة والنكاف والحصبة الألمانية، فإنها تتحور قليلاً بحيث يتم استخدام نفس اللقاح عامًا بعد عام.
اللقاحات والأدوية المضادة للفيروسات للعلاج
في بعض الحالات، يمكن استخدام اللقاحات لعلاج عدوى فيروسية نشطة. في حالة داء الكلب، وهو مرض عصبي قاتل ينتقل عن طريق لعاب الحيوانات المصابة بفيروس داء الكلب، قد يكون تطور المرض من وقت لدغة الحيوان إلى وقت دخوله الجهاز العصبي المركزي أسبوعين أو أكثر. هذا هو الوقت الكافي لتلقيح شخص يشتبه في تعرضه للعض من قبل حيوان مصاب بداء الكلب، والاستجابة المناعية المعززة من التطعيم كافية لمنع الفيروس من دخول الأنسجة العصبية. وبالتالي، يتم تجنب العواقب العصبية القاتلة للمرض ويجب على الفرد فقط التعافي من اللدغة المصابة. يتم استخدام هذا النهج أيضًا لعلاج الإيبولا، وهو أحد أسرع الفيروسات وأكثرها فتكًا التي تصيب البشر، على الرغم من أنه عادة ما يصيب مجموعات سكانية محدودة. الإيبولا هو أيضًا سبب رئيسي للوفاة في الغوريلا. يمكن أن يتسبب هذا الفيروس، الذي ينتقل عن طريق الخفافيش والقردة العليا، في وفاة 70-90 بالمائة من المصابين في غضون أسبوعين. باستخدام اللقاحات المطورة حديثًا التي تعزز الاستجابة المناعية، هناك أمل في أن تكون أجهزة المناعة للأفراد المصابين قادرة بشكل أفضل على السيطرة على الفيروس، مما قد يقلل من معدلات الوفيات.
طريقة أخرى لعلاج الالتهابات الفيروسية هي استخدام الأدوية المضادة للفيروسات. غالبًا ما تكون لهذه الأدوية قدرة محدودة على علاج الأمراض الفيروسية ولكنها تُستخدم للسيطرة على أعراض مجموعة متنوعة من الأمراض الفيروسية وتقليلها. بالنسبة لمعظم الفيروسات، تمنع هذه الأدوية الفيروس عن طريق منع عمل واحد أو أكثر من بروتيناته. من المهم أن يتم ترميز البروتينات المستهدفة بواسطة الجينات الفيروسية وأن لا تكون هذه الجزيئات موجودة في خلية مضيفة صحية. بهذه الطريقة، يتم منع نمو الفيروس دون الإضرار بالمضيف. هناك أعداد كبيرة من الأدوية المضادة للفيروسات المتاحة لعلاج العدوى، بعضها خاص بفيروس معين والبعض الآخر يمكن أن يؤثر على فيروسات متعددة.
تم تطوير مضادات الفيروسات لعلاج الهربس التناسلي (الهربس البسيط الثاني) والإنفلونزا. بالنسبة للهربس التناسلي، يمكن لأدوية مثل الأسيكلوفير أن تقلل من عدد ومدة نوبات المرض الفيروسي النشط التي يصاب خلالها المرضى بآفات فيروسية في خلايا جلدهم. نظرًا لأن الفيروس يظل كامنًا في الأنسجة العصبية للجسم مدى الحياة، فإن هذا الدواء ليس علاجًا ولكنه يمكن أن يجعل أعراض المرض أكثر قابلية للإدارة. بالنسبة للأنفلونزا، يمكن لأدوية مثل تاميفلو أن تقلل من مدة أعراض «الأنفلونزا» لمدة يوم أو يومين، لكن الدواء لا يمنع الأعراض تمامًا. تم استخدام أدوية أخرى مضادة للفيروسات، مثل ريبافيرين، لعلاج مجموعة متنوعة من الالتهابات الفيروسية.
إلى حد بعيد، كان الاستخدام الأكثر نجاحًا لمضادات الفيروسات هو علاج فيروس نقص المناعة البشرية القهقرية، الذي يسبب مرضًا، إذا لم يتم علاجه، يكون عادةً مميتًا في غضون 10-12 عامًا بعد الإصابة. تمكنت الأدوية المضادة لفيروس نقص المناعة البشرية من التحكم في تكاثر الفيروس لدرجة أن الأفراد الذين يتلقون هذه الأدوية يعيشون لفترة أطول بكثير من غير المعالجين.
تمنع الأدوية المضادة لفيروس نقص المناعة البشرية تكاثر الفيروس في العديد من المراحل المختلفة من الدورة التكرارية لفيروس نقص المناعة البشرية. تم تطوير الأدوية التي تمنع اندماج الغلاف الفيروسي لفيروس نقص المناعة البشرية مع الغشاء البلازمي للخلية المضيفة (مثبطات الاندماج)، وتحويل جينوم الحمض النووي الريبي إلى الحمض النووي المزدوج (مثبطات النسخ العكسي)، ودمج الحمض النووي الفيروسي في جينوم المضيف (مثبطات الإنتيغراز)، و معالجة البروتينات الفيروسية (مثبطات البروتياز).
عند استخدام أي من هذه الأدوية بشكل فردي، فإن معدل الطفرة المرتفع للفيروس يسمح للفيروس بتطوير مقاومة الدواء بسرعة. كان الاختراق في علاج فيروس نقص المناعة البشرية هو تطوير علاج مضاد للفيروسات القهقرية عالي النشاط (HAART)، والذي يتضمن مزيجًا من الأدوية المختلفة، يُطلق عليه أحيانًا اسم «الكوكتيل». من خلال مهاجمة الفيروس في مراحل مختلفة من دورة النسخ المتماثل، يصعب على الفيروس تطوير مقاومة للعديد من الأدوية في نفس الوقت. ومع ذلك، حتى مع استخدام العلاج المركب HAART، هناك قلق من أن الفيروس سيطور مقاومة لهذا العلاج بمرور الوقت. وبالتالي، يتم تطوير أدوية جديدة مضادة لفيروس نقص المناعة البشرية باستمرار على أمل مواصلة المعركة ضد هذا الفيروس القاتل للغاية.
ملخص
الفيروسات هي كيانات غير خلوية لا يمكن رؤيتها عادةً إلا باستخدام المجهر الإلكتروني. تحتوي جينوماتها إما على DNA أو RNA، وتتكاثر باستخدام بروتينات النسخ المتماثل للخلية المضيفة. تتنوع الفيروسات وتصيب الأركيا والبكتيريا والفطريات والنباتات والحيوانات. تتكون الفيروسات من نواة حمض نووي محاطة بغلاف بروتيني مع أو بدون غلاف شحمي خارجي.
يؤدي التكاثر الفيروسي داخل الخلية الحية دائمًا إلى حدوث تغييرات في الخلية، مما يؤدي أحيانًا إلى موت الخلية وأحيانًا قتل الخلايا المصابة ببطء. هناك ست مراحل أساسية في دورة تكرار الفيروسات: المرفق والاختراق وفك الطلاء والتكرار والتجميع والإصدار. قد تكون العدوى الفيروسية منتجة، مما يؤدي إلى ظهور فيروسات جديدة، أو غير منتجة، مما يعني أن الفيروس يبقى داخل الخلية دون إنتاج فيروسات جديدة.
تسبب الفيروسات مجموعة متنوعة من الأمراض لدى البشر. يمكن الوقاية من العديد من هذه الأمراض باستخدام اللقاحات الفيروسية التي تحفز المناعة الوقائية ضد الفيروس دون التسبب في مرض كبير. يمكن أيضًا استخدام اللقاحات الفيروسية في حالات العدوى الفيروسية النشطة، مما يعزز قدرة الجهاز المناعي على التحكم في الفيروس أو تدميره. تم تطوير الأدوية المضادة للفيروسات التي تستهدف الإنزيمات والمنتجات البروتينية الأخرى للجينات الفيروسية واستخدامها بنجاح متفاوت. تم استخدام مجموعات من الأدوية المضادة لفيروس نقص المناعة البشرية للسيطرة الفعالة على الفيروس، وإطالة عمر الأفراد المصابين.
اتصالات فنية
الشكل\(\PageIndex{4}\): أي من العبارات التالية حول بنية الفيروسات صحيحة؟
ج: جميع الفيروسات مغلفة بغشاء فيروسي.
B. يتكون الكابسومير من وحدات بروتينية صغيرة تسمى الكابسيدات.
C. DNA هو المادة الوراثية في جميع الفيروسات.
تساعد البروتينات السكرية D الفيروس على الالتصاق بالخلية المضيفة.
- إجابة
-
د
الشكل\(\PageIndex{5}\): يتم تعبئة فيروس الأنفلونزا في غلاف فيروسي يندمج مع غشاء البلازما. بهذه الطريقة، يمكن للفيروس الخروج من الخلية المضيفة دون قتلها. ما الميزة التي يكتسبها الفيروس من خلال الحفاظ على الخلية المضيفة حية؟
- إجابة
-
يمكن أن تستمر الخلية المضيفة في صنع جزيئات فيروس جديدة.
مسرد المصطلحات
- خلوي
- تفتقر إلى الخلايا
- موت الخلايا المبرمج
- موت الخلايا الناجم عن تحريض الآليات الداخلية للخلية إما كخطوة طبيعية في تطور كائن متعدد الخلايا أو بسبب عوامل بيئية أخرى مثل الإشارات من خلايا الجهاز المناعي
- تخفيف
- ضعف الفيروس أثناء تطوير اللقاح
- غطاء الرأس
- طلاء البروتين للنواة الفيروسية
- اعتلال الخلايا
- تسبب تلف الخلايا
- بروتين سكري
- جزيء بروتين مع جزيئات كربوهيدرات مرفقة
- لقاح
- حل ضعيف لمكونات الفيروسات أو الفيروسات أو العوامل الأخرى التي تنتج استجابة مناعية
- فيريون
- جسيم فيروس فردي خارج الخلية المضيفة
- مغلف فيروسي
- طبقة ثنائية دهنية تغلف بعض الفيروسات


