37.3: تنظيم عمليات الجسم
- Page ID
- 196174
المهارات اللازمة للتطوير
- اشرح كيف تنظم الهرمونات نظام الإخراج
- ناقش دور الهرمونات في الجهاز التناسلي
- وصف كيفية تنظيم الهرمونات لعملية التمثيل الغذائي
- شرح دور الهرمونات في الأمراض المختلفة
للهرمونات مجموعة واسعة من التأثيرات وتعدل العديد من عمليات الجسم المختلفة. العمليات التنظيمية الرئيسية التي سيتم فحصها هنا هي تلك التي تؤثر على جهاز الإخراج، والجهاز التناسلي، والتمثيل الغذائي، وتركيزات الكالسيوم في الدم، والنمو، والاستجابة للإجهاد.
التنظيم الهرموني لنظام الإخراج
يعد الحفاظ على توازن الماء المناسب في الجسم أمرًا مهمًا لتجنب الجفاف أو الإفراط في الترطيب (نقص صوديوم الدم). تتم مراقبة تركيز الماء في الجسم بواسطة المستقبلات التناضحية في منطقة ما تحت المهاد، والتي تكتشف تركيز الإلكتروليتات في السائل خارج الخلية. يرتفع تركيز الإلكتروليتات في الدم عندما يكون هناك فقدان للمياه بسبب التعرق المفرط أو عدم كفاية تناول الماء أو انخفاض حجم الدم بسبب فقدان الدم. تؤدي الزيادة في مستويات الإلكتروليت في الدم إلى إرسال إشارة عصبية من المستقبلات الأسموزية في نوى المهاد. تتكون الغدة النخامية من عنصرين: الأمامي والخلفي. تتكون الغدة النخامية الأمامية من خلايا غدية تفرز هرمونات البروتين. الغدة النخامية الخلفية هي امتداد لمنطقة ما تحت المهاد. وتتكون إلى حد كبير من الخلايا العصبية المستمرة مع منطقة ما تحت المهاد.
ينتج المهاد هرمونًا متعدد الببتيد يُعرف باسم الهرمون المضاد لإدرار البول (ADH)، والذي يتم نقله إلى الغدة النخامية الخلفية وإطلاقها منها. يتمثل الإجراء الرئيسي لـ ADH في تنظيم كمية المياه التي تفرزها الكلى. نظرًا لأن ADH (المعروف أيضًا باسم vasopressin) يسبب إعادة امتصاص الماء مباشرة من أنابيب الكلى، تتركز الأملاح والفضلات في ما سيتم إفرازه في النهاية على شكل بول. يتحكم المهاد في آليات إفراز ADH، إما عن طريق تنظيم حجم الدم أو تركيز الماء في الدم. يمكن أن يتسبب الجفاف أو الإجهاد الفسيولوجي في زيادة الأسمولية فوق 300 مللي أمبير/لتر، مما يؤدي بدوره إلى زيادة إفراز هرمون ADH وسيتم الاحتفاظ بالماء، مما يؤدي إلى زيادة ضغط الدم. ينتقل ADH في مجرى الدم إلى الكلى. بمجرد الوصول إلى الكلى، يغير ADH الكلى لتصبح أكثر نفاذية للماء عن طريق إدخال قنوات المياه مؤقتًا، وهي الأكوابورينات، في أنابيب الكلى. ينتقل الماء من أنابيب الكلى عبر الأكوابورينات، مما يقلل من حجم البول. يتم إعادة امتصاص الماء في الشعيرات الدموية مما يؤدي إلى خفض الأسمولية في الدم إلى وضعها الطبيعي. مع انخفاض الأسمولية في الدم، تقلل آلية التغذية الراجعة السلبية من نشاط مستقبلات التناضح في منطقة ما تحت المهاد، ويقل إفراز ADH. يمكن تقليل إطلاق ADH بمواد معينة، بما في ذلك الكحول، والتي يمكن أن تسبب زيادة إنتاج البول والجفاف.
يؤدي نقص الإنتاج المزمن لـ ADH أو طفرة في مستقبلات ADH إلى مرض السكري الكاذب. إذا لم تفرز الغدة النخامية الخلفية كمية كافية من هرمون ADH، فلا يمكن للكلى الاحتفاظ بالماء وفقده كبول. يؤدي هذا إلى زيادة العطش، ولكن الماء الذي يتم تناوله يتم فقده مرة أخرى ويجب استهلاكه باستمرار. إذا لم تكن الحالة شديدة، فقد لا يحدث الجفاف، ولكن الحالات الشديدة يمكن أن تؤدي إلى اختلال توازن الإلكتروليت بسبب الجفاف.
هرمون آخر مسؤول عن الحفاظ على تركيزات الإلكتروليت في السوائل خارج الخلية هو الألدوستيرون، وهو هرمون الستيرويد الذي تنتجه قشرة الغدة الكظرية. على عكس ADH، الذي يعزز إعادة امتصاص الماء للحفاظ على توازن الماء المناسب، يحافظ الألدوستيرون على توازن الماء المناسب من خلال تعزيز إعادة امتصاص Na + وإفراز K + من السائل خارج الخلية للخلايا في أنابيب الكلى. نظرًا لأنه يتم إنتاجه في قشرة الغدة الكظرية ويؤثر على تركيزات المعادن Na + و K +، يشار إلى الألدوستيرون باسم مينيرالوكورتيكويد، وهو كورتيكوستيرويد يؤثر على توازن الأيونات والماء. يتم تحفيز إطلاق الألدوستيرون من خلال انخفاض مستويات الصوديوم في الدم أو حجم الدم أو ضغط الدم أو زيادة مستويات البوتاسيوم في الدم. كما أنه يمنع فقدان Na + من العرق واللعاب وعصير المعدة. تؤدي إعادة امتصاص Na + أيضًا إلى إعادة الامتصاص التناضحي للماء، مما يغير حجم الدم وضغط الدم.
يمكن تحفيز إنتاج الألدوستيرون عن طريق انخفاض ضغط الدم، مما يؤدي إلى سلسلة من الإطلاق الكيميائي، كما هو موضح في الشكل\(\PageIndex{1}\). عندما ينخفض ضغط الدم، يتم تنشيط نظام الرينين-أنجيوتنسين-الألدوستيرون (RAAS). تقوم الخلايا الموجودة في الجهاز الجداري، الذي ينظم وظائف النيفرون في الكلى، باكتشاف ذلك وإطلاق الرينين. الرينين، وهو إنزيم، يدور في الدم ويتفاعل مع بروتين البلازما الذي ينتجه الكبد والذي يسمى أنجيوتنسينوجين. عندما يتم شق الأنجيوتنسينوجين بواسطة الرينين، فإنه ينتج الأنجيوتنسين 1، والذي يتم تحويله بعد ذلك إلى أنجيوتنسين 2 في الرئتين. يعمل الأنجيوتنسين II كهرمون ثم يتسبب في إطلاق هرمون الألدوستيرون بواسطة قشرة الغدة الكظرية، مما يؤدي إلى زيادة امتصاص Na + واحتباس الماء وزيادة ضغط الدم. بالإضافة إلى كونه مضيقًا قويًا للأوعية، يتسبب أيضًا في زيادة هرمون ADH وزيادة العطش، وكلاهما يساعد على رفع ضغط الدم.
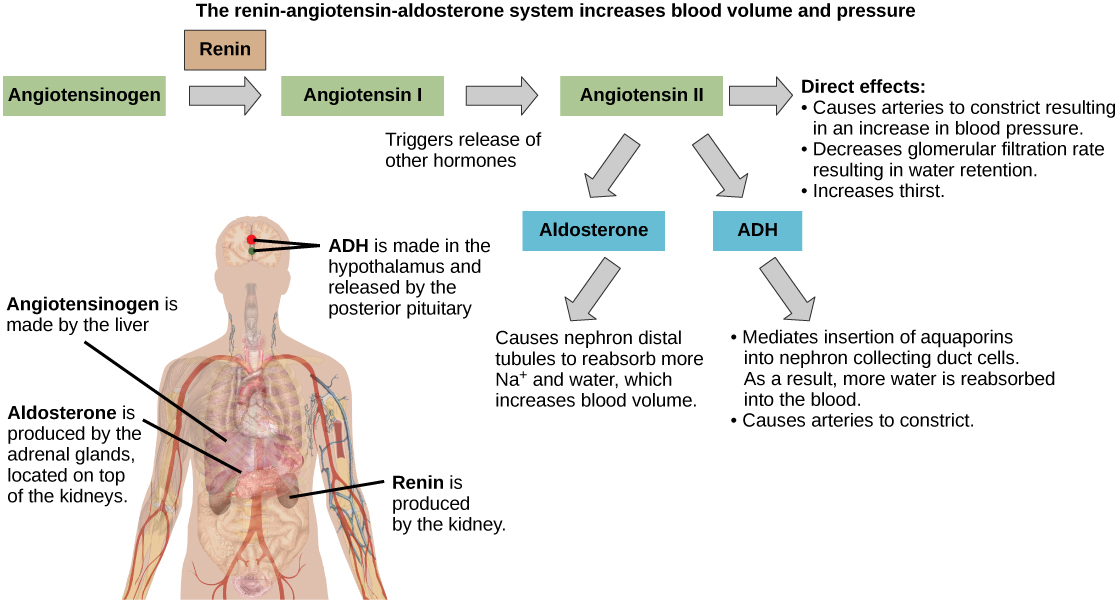
التنظيم الهرموني للجهاز التناسلي
تنظيم الجهاز التناسلي هو عملية تتطلب عمل الهرمونات من الغدة النخامية وقشرة الغدة الكظرية والغدد التناسلية. خلال فترة البلوغ في كل من الذكور والإناث، ينتج الوطاء هرمون إفراز الغدد التناسلية (GnRH)، الذي يحفز إنتاج وإطلاق الهرمون المنبه للجريب (FSH) والهرمون اللوتيني (LH) من الغدة النخامية الأمامية. تنظم هذه الهرمونات الغدد التناسلية (الخصيتين في الذكور والمبيض عند الإناث) وبالتالي تسمى الجونادوتروبين. في كل من الذكور والإناث، يحفز FSH إنتاج الأمشاج ويحفز LH إنتاج الهرمونات عن طريق الغدد التناسلية. تؤدي الزيادة في مستويات هرمون الغدد التناسلية إلى تثبيط إنتاج GnRH من خلال حلقة ردود فعل سلبية.
تنظيم الجهاز التناسلي الذكري
في الذكور، يحفز FSH نضوج خلايا الحيوانات المنوية. يتم تثبيط إنتاج FSH بواسطة هرمون المثبط الذي تفرزه الخصيتان. يحفز LH إنتاج الهرمونات الجنسية (الأندروجينات) بواسطة الخلايا الخلالية للخصيتين، وبالتالي يطلق عليه أيضًا هرمون تحفيز الخلايا الخلالية. الاندروجين الأكثر شهرة في الذكور هو هرمون التستوستيرون. يعزز التستوستيرون إنتاج الحيوانات المنوية والخصائص الذكورية. تنتج قشرة الغدة الكظرية أيضًا كميات صغيرة من سلائف التستوستيرون، على الرغم من أن دور إنتاج هذا الهرمون الإضافي غير مفهوم تمامًا.
الاتصال اليومي: مخاطر الهرمونات الاصطناعية
يحاول بعض الرياضيين تعزيز أدائهم باستخدام الهرمونات الاصطناعية التي تعزز أداء العضلات. الستيرويدات الابتنائية، وهي شكل من أشكال هرمون التستوستيرون الذكري، هي واحدة من أكثر أدوية تحسين الأداء المعروفة على نطاق واسع. تستخدم المنشطات للمساعدة في بناء كتلة العضلات. تشمل الهرمونات الأخرى التي تستخدم لتعزيز الأداء الرياضي الإريثروبويتين، الذي يحفز إنتاج خلايا الدم الحمراء، وهرمون النمو البشري، الذي يمكن أن يساعد في بناء كتلة العضلات. معظم أدوية تحسين الأداء غير قانونية للأغراض غير الطبية. كما تم حظرها من قبل الهيئات الإدارية الوطنية والدولية بما في ذلك اللجنة الأولمبية الدولية واللجنة الأولمبية الأمريكية والرابطة الوطنية لألعاب القوى الجماعية ودوري البيسبول الرئيسي والدوري الوطني لكرة القدم.

غالبًا ما تكون الآثار الجانبية للهرمونات الاصطناعية كبيرة ولا يمكن عكسها، وفي بعض الحالات تكون قاتلة. تنتج الأندروجينات العديد من المضاعفات مثل اختلال وظائف الكبد وأورام الكبد، وتضخم غدة البروستاتا، وصعوبة التبول، والإغلاق المبكر للغضاريف المشاشية، وضمور الخصية، والعقم، واكتئاب الجهاز المناعي. غالبًا ما يكون الإجهاد الفسيولوجي الذي تسببه هذه المواد أكبر مما يمكن للجسم تحمله، مما يؤدي إلى آثار غير متوقعة وخطيرة ويربط استخدامها بالنوبات القلبية والسكتات الدماغية وضعف وظائف القلب.
تنظيم الجهاز التناسلي الأنثوي
في الإناث، يحفز هرمون FSH نمو خلايا البويضات، التي تسمى البويضات، والتي تتطور في هياكل تسمى البصيلات. تنتج خلايا الجريب هرمون المثبط، الذي يمنع إنتاج FSH. يلعب LH أيضًا دورًا في تطور البويضات وتحريض الإباضة وتحفيز إنتاج الاستراديول والبروجسترون بواسطة المبيضين، كما هو موضح في الشكل\(\PageIndex{3}\). استراديول والبروجستيرون هي هرمونات الستيرويد التي تعد الجسم للحمل. ينتج استراديول خصائص جنسية ثانوية عند الإناث، بينما ينظم كل من الاستراديول والبروجستيرون الدورة الشهرية.
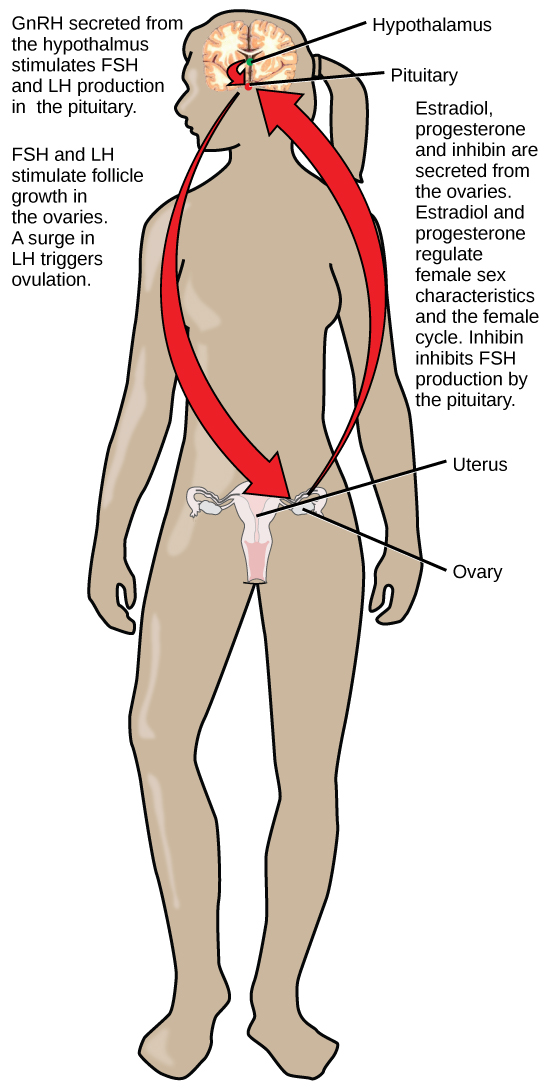
بالإضافة إلى إنتاج FSH و LH، ينتج الجزء الأمامي من الغدة النخامية أيضًا هرمون البرولاكتين (PRL) في الإناث. يحفز البرولاكتين إنتاج الحليب عن طريق الغدد الثديية بعد الولادة. يتم تنظيم مستويات البرولاكتين بواسطة هرمونات المهاد هرمون إفراز البرولاكتين (PRH) وهرمون تثبيط البرولاكتين (PIH)، والذي يُعرف الآن باسم الدوبامين. يحفز PRH إطلاق البرولاكتين ويثبط PIH ذلك.
تطلق الغدة النخامية الخلفية هرمون الأوكسيتوسين، الذي يحفز تقلصات الرحم أثناء الولادة. لا تكون عضلات الرحم الملساء حساسة جدًا للأوكسيتوسين حتى وقت متأخر من الحمل عندما يصل عدد مستقبلات الأوكسيتوسين في الرحم إلى ذروته. يؤدي تمدد الأنسجة في الرحم وعنق الرحم إلى تحفيز إفراز الأوكسيتوسين أثناء الولادة. تزداد شدة الانقباضات مع ارتفاع مستويات الأوكسيتوسين في الدم عبر آلية التغذية الراجعة الإيجابية حتى اكتمال الولادة. يحفز الأوكسيتوسين أيضًا تقلص الخلايا العضلية الظهارية حول الغدد الثديية المنتجة للحليب. عندما تنقبض هذه الخلايا، يتم دفع الحليب من الحويصلات الهوائية الإفرازية إلى قنوات الحليب ويتم إخراجه من الثدي في منعكس طرد الحليب («التراجع»). يتم تحفيز إطلاق الأوكسيتوسين عن طريق إرضاع الرضيع، مما يؤدي إلى تخليق الأوكسيتوسين في منطقة ما تحت المهاد وإطلاقه في الدورة الدموية في الغدة النخامية الخلفية.
التنظيم الهرموني لعملية التمثيل الغذائي
تختلف مستويات الجلوكوز في الدم بشكل كبير على مدار اليوم حيث تتناوب فترات استهلاك الطعام مع فترات الصيام. الأنسولين والجلوكاجون هما الهورمونان المسؤولان بشكل أساسي عن الحفاظ على توازن مستويات الجلوكوز في الدم. يتم تنظيم إضافي بواسطة هرمونات الغدة الدرقية.
تنظيم مستويات الجلوكوز في الدم بواسطة الأنسولين والجلوكاجون
تحتاج خلايا الجسم إلى العناصر الغذائية لكي تعمل، ويتم الحصول على هذه العناصر الغذائية من خلال التغذية. من أجل إدارة تناول المغذيات وتخزين الكمية الزائدة واستخدام الاحتياطيات عند الضرورة، يستخدم الجسم الهرمونات لتخفيف مخازن الطاقة. يتم إنتاج الأنسولين بواسطة خلايا بيتا في البنكرياس، والتي يتم تحفيزها لإطلاق الأنسولين مع ارتفاع مستويات الجلوكوز في الدم (على سبيل المثال، بعد تناول الوجبة). يخفض الأنسولين مستويات الجلوكوز في الدم من خلال تعزيز معدل امتصاص الجلوكوز واستخدامه من قبل الخلايا المستهدفة، والتي تستخدم الجلوكوز لإنتاج ATP. كما أنه يحفز الكبد لتحويل الجلوكوز إلى جليكوجين، والذي يتم تخزينه بعد ذلك بواسطة الخلايا لاستخدامه لاحقًا. يزيد الأنسولين أيضًا من نقل الجلوكوز إلى خلايا معينة، مثل خلايا العضلات والكبد. ينتج هذا عن زيادة بوساطة الأنسولين في عدد بروتينات نقل الجلوكوز في أغشية الخلايا، والتي تزيل الجلوكوز من الدورة الدموية عن طريق الانتشار الميسر. نظرًا لأن الأنسولين يرتبط بالخلية المستهدفة عبر مستقبلات الأنسولين ونقل الإشارة، فإنه يحفز الخلية على دمج بروتينات نقل الجلوكوز في غشاءها. هذا يسمح للجلوكوز بدخول الخلية، حيث يمكن استخدامه كمصدر للطاقة. ومع ذلك، لا يحدث هذا في جميع الخلايا: يمكن لبعض الخلايا، بما في ذلك تلك الموجودة في الكلى والدماغ، الوصول إلى الجلوكوز دون استخدام الأنسولين. يحفز الأنسولين أيضًا تحويل الجلوكوز إلى الدهون في الخلايا الشحمية وتخليق البروتينات. تؤدي هذه الإجراءات التي يتوسطها الأنسولين إلى انخفاض تركيزات الجلوكوز في الدم، والتي تسمى بتأثير نقص السكر في الدم «انخفاض السكر»، والذي يمنع المزيد من إطلاق الأنسولين من خلايا بيتا من خلال حلقة التغذية الراجعة السلبية.
رابط إلى التعلم
تصف هذه الرسوم المتحركة دور الأنسولين والبنكرياس في مرض السكري.
يمكن أن يؤدي ضعف وظيفة الأنسولين إلى حالة تسمى داء السكري، وتظهر الأعراض الرئيسية لها في الشكل\(\PageIndex{4}\). يمكن أن يحدث هذا بسبب انخفاض مستويات إنتاج الأنسولين من قبل خلايا بيتا في البنكرياس، أو بسبب انخفاض حساسية خلايا الأنسجة للأنسولين. يمنع هذا الجلوكوز من امتصاص الخلايا، مما يسبب مستويات عالية من الجلوكوز في الدم، أو ارتفاع السكر في الدم (ارتفاع السكر). ارتفاع مستويات الجلوكوز في الدم يجعل من الصعب على الكلى استعادة كل الجلوكوز من البول الناشئ، مما يؤدي إلى فقدان الجلوكوز في البول. يؤدي ارتفاع مستويات الجلوكوز أيضًا إلى إعادة امتصاص كميات أقل من الماء عن طريق الكلى، مما يؤدي إلى إنتاج كميات كبيرة من البول؛ وقد يؤدي ذلك إلى الجفاف. مع مرور الوقت، يمكن أن يتسبب ارتفاع مستويات الجلوكوز في الدم في تلف الأعصاب للعينين وأنسجة الجسم الطرفية، بالإضافة إلى تلف الكلى ونظام القلب والأوعية الدموية. يمكن أن يسبب الإفراط في إفراز الأنسولين نقص السكر في الدم وانخفاض مستويات الجلوكوز في الدم. يؤدي هذا إلى عدم توفر الجلوكوز الكافي للخلايا، وغالبًا ما يؤدي إلى ضعف العضلات، ويمكن أن يتسبب أحيانًا في فقدان الوعي أو الوفاة إذا تُرك دون علاج.
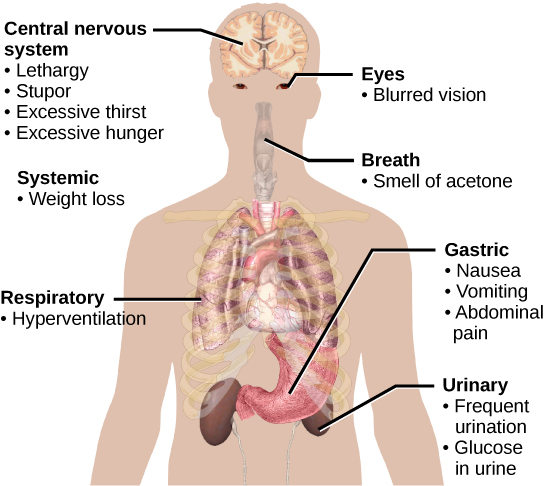
عندما تنخفض مستويات الجلوكوز في الدم إلى ما دون المستويات الطبيعية، على سبيل المثال بين الوجبات أو عند استخدام الجلوكوز بسرعة أثناء التمرين، يتم إطلاق هرمون الجلوكاجون من خلايا ألفا في البنكرياس. يرفع الجلوكاجون مستويات الجلوكوز في الدم، مما يؤدي إلى ما يسمى بتأثير ارتفاع السكر في الدم، عن طريق تحفيز تحلل الجليكوجين إلى جلوكوز في خلايا العضلات الهيكلية وخلايا الكبد في عملية تسمى تحلل الجليكوجين. يمكن بعد ذلك استخدام الجلوكوز كطاقة بواسطة خلايا العضلات وإطلاقه في الدورة الدموية بواسطة خلايا الكبد. يحفز الجلوكاجون أيضًا امتصاص الأحماض الأمينية من الدم عن طريق الكبد، مما يحولها بعد ذلك إلى جلوكوز. تسمى عملية تخليق الجلوكوز هذه بتكوين السكر. يحفز الجلوكاجون أيضًا الخلايا الدهنية لإطلاق الأحماض الدهنية في الدم. تؤدي هذه الإجراءات التي يتوسطها الجلوكاجون إلى زيادة مستويات الجلوكوز في الدم إلى مستويات التوازن الطبيعية. يؤدي ارتفاع مستويات الجلوكوز في الدم إلى منع المزيد من إطلاق الجلوكاجون من البنكرياس عبر آلية التغذية الراجعة السلبية. بهذه الطريقة، يعمل الأنسولين والجلوكاجون معًا للحفاظ على مستويات الجلوكوز المتجانسة، كما هو موضح في الشكل\(\PageIndex{5}\).
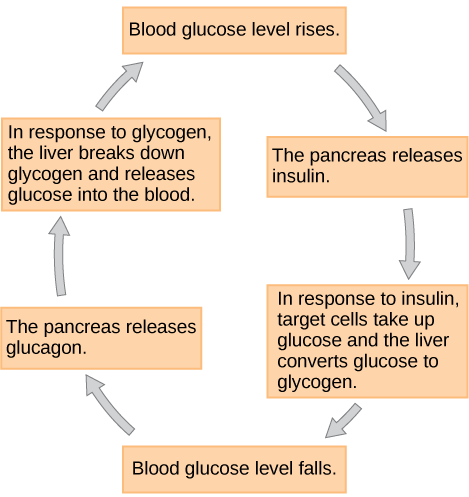
التمارين
قد تسبب أورام البنكرياس إفرازًا زائدًا من الجلوكاجون. ينتج داء السكري من النوع الأول عن فشل البنكرياس في إنتاج الأنسولين. أي من العبارات التالية عن هذين الشرطين صحيحة؟
- سيكون لورم البنكرياس ومرض السكري من النوع الأول تأثيرات عكسية على مستويات السكر في الدم.
- يتسبب كل من ورم البنكرياس وداء السكري من النوع الأول في ارتفاع السكر في الدم.
- يتسبب كل من ورم البنكرياس وداء السكري من النوع الأول في نقص السكر في الدم.
- يؤدي كل من أورام البنكرياس ومرض السكري من النوع الأول إلى عدم قدرة الخلايا على امتصاص الجلوكوز.
- إجابة
-
ب
تنظيم مستويات الجلوكوز في الدم بواسطة هرمونات الغدة الدرقية
يتم تحديد معدل الأيض القاعدي، وهو كمية السعرات الحرارية التي يحتاجها الجسم أثناء الراحة، من خلال هرمونين تنتجهما الغدة الدرقية: هرمون الغدة الدرقية، المعروف أيضًا باسم تيترايودوثيرونين أو T 4، وثلاثي يودوثيرونين، المعروف أيضًا باسم T 3. تؤثر هذه الهرمونات على كل خلية في الجسم تقريبًا باستثناء الدماغ البالغ والرحم والخصيتين وخلايا الدم والطحال. يتم نقلها عبر الغشاء البلازمي للخلايا المستهدفة وترتبط بمستقبلات الميتوكوندريا مما يؤدي إلى زيادة إنتاج ATP. في النواة، يقوم T 3 و T 4 بتنشيط الجينات المشاركة في إنتاج الطاقة وأكسدة الجلوكوز. يؤدي هذا إلى زيادة معدلات التمثيل الغذائي وإنتاج حرارة الجسم، والذي يُعرف بالتأثير الحراري للهرمون.
يتم تحفيز إطلاق T 3 و T 4 من الغدة الدرقية بواسطة هرمون تحفيز الغدة الدرقية (TSH)، الذي تنتجه الغدة النخامية الأمامية. يؤدي ارتباط TSH في مستقبلات بصيلات الغدة الدرقية إلى إنتاج T 3 و T 4 من بروتين سكري يسمى ثيروجلوبولين. يوجد الثيروجلوبولين في بصيلات الغدة الدرقية، ويتم تحويله إلى هرمونات الغدة الدرقية مع إضافة اليود. يتكون اليود من أيونات اليوديد التي تنتقل بنشاط إلى بصيلات الغدة الدرقية من مجرى الدم. ثم يربط إنزيم البيروكسيديز اليود بالحمض الأميني التيروزين الموجود في الثيروجلوبولين. يحتوي T 3 على ثلاثة أيونات اليود المرفقة، بينما يحتوي T 4 على أربعة أيونات اليود المرفقة. ثم يتم إطلاق T 3 و T 4 في مجرى الدم، مع إطلاق T 4 بكميات أكبر بكثير من T 3. نظرًا لأن T 3 أكثر نشاطًا من T 4 وهو مسؤول عن معظم تأثيرات هرمونات الغدة الدرقية، فإن أنسجة الجسم تحول T 4 إلى T 3 عن طريق إزالة أيون اليود. يتم ربط معظم T 3 و T 4 المُطلقين لنقل البروتينات في مجرى الدم وغير قادر على عبور الغشاء البلازمي للخلايا. يتم إطلاق هذه الجزيئات المرتبطة بالبروتين فقط عندما تبدأ مستويات الدم من الهرمون غير المرتبط في الانخفاض. بهذه الطريقة، يتم الحفاظ على هرمون احتياطي لمدة أسبوع في الدم. تؤدي زيادة مستويات T 3 و T 4 في الدم إلى تثبيط إطلاق TSH، مما يؤدي إلى انخفاض إطلاق T 3 و T 4 من الغدة الدرقية.
تتطلب الخلايا الجريبية للغدة الدرقية يوديدات (أنيونات اليود) من أجل تخليق T 3 و T 4. يتم نقل اليوديدات التي يتم الحصول عليها من النظام الغذائي بنشاط إلى الخلايا البصيلية مما يؤدي إلى تركيز أعلى بحوالي 30 مرة من الدم. يوفر النظام الغذائي النموذجي في أمريكا الشمالية كمية أكبر من اليود مما هو مطلوب بسبب إضافة اليوديد إلى ملح الطعام. يؤدي تناول اليود غير الكافي، الذي يحدث في العديد من البلدان النامية، إلى عدم القدرة على تخليق هرمونات T 3 و T 4. تتضخم الغدة الدرقية في حالة تسمى تضخم الغدة الدرقية، والتي تحدث بسبب الإفراط في إنتاج هرمون TSH دون تكوين هرمون الغدة الدرقية. يوجد ثايروجلوبولين في سائل يسمى الغرواني، ويؤدي تحفيز TSH إلى مستويات أعلى من تراكم الغروانية في الغدة الدرقية. في حالة عدم وجود اليود، لا يتم تحويل هذا إلى هرمون الغدة الدرقية، وتبدأ الغروانية في التراكم أكثر فأكثر في الغدة الدرقية، مما يؤدي إلى تضخم الغدة الدرقية.
يمكن أن تنشأ الاضطرابات من نقص الإنتاج والإفراط في إنتاج هرمونات الغدة الدرقية. يمكن أن يتسبب قصور الغدة الدرقية، ونقص إنتاج هرمونات الغدة الدرقية، في انخفاض معدل الأيض مما يؤدي إلى زيادة الوزن والحساسية للبرد وانخفاض النشاط العقلي، من بين أعراض أخرى. في الأطفال، يمكن أن يسبب قصور الغدة الدرقية كريتينيسم، مما قد يؤدي إلى التخلف العقلي وعيوب النمو. يمكن أن يؤدي فرط نشاط الغدة الدرقية، وهو الإفراط في إنتاج هرمونات الغدة الدرقية، إلى زيادة معدل الأيض وآثاره: فقدان الوزن، وإنتاج الحرارة الزائدة، والتعرق، وزيادة معدل ضربات القلب. يعد مرض جريفز أحد الأمثلة على حالة فرط نشاط الغدة الدرقية.
التحكم الهرموني في مستويات الكالسيوم في الدم
يعد تنظيم تركيزات الكالسيوم في الدم أمرًا مهمًا لتوليد تقلصات العضلات والنبضات العصبية التي يتم تحفيزها كهربائيًا. إذا ارتفعت مستويات الكالسيوم أكثر من اللازم، تنخفض نفاذية الغشاء للصوديوم وتصبح الأغشية أقل استجابة. إذا كانت مستويات الكالسيوم منخفضة جدًا، تزداد نفاذية الغشاء للصوديوم ويمكن أن يؤدي ذلك إلى حدوث تشنجات أو تشنجات عضلية.
يتم تنظيم مستويات الكالسيوم في الدم بواسطة هرمون الغدة الدرقية (PTH)، الذي تنتجه الغدد فوق الدرقية، كما هو موضح في الشكل\(\PageIndex{6}\). يتم إطلاق PTH استجابة لانخفاض مستويات Ca 2+ في الدم. يزيد PTH من مستويات Ca 2+ من خلال استهداف الهيكل العظمي والكلى والأمعاء. في الهيكل العظمي، يحفز PTH الخلايا الآكلة للعظام، مما يؤدي إلى إعادة امتصاص العظام، مما يؤدي إلى إطلاق Ca 2+ من العظام إلى الدم. يثبط PTH أيضًا بانيات العظم، مما يقلل من ترسب الكالسيوم 2+ في العظام. في الأمعاء، يزيد PTH من امتصاص الكالسيوم 2+ الغذائي، وفي الكلى، يحفز PTH إعادة امتصاص CA 2+. بينما يعمل PTH مباشرة على الكلى لزيادة امتصاص Ca 2+، فإن آثاره على الأمعاء غير مباشرة. يؤدي PTH إلى تكوين الكالسيتريول، وهو شكل نشط من فيتامين د، والذي يعمل على الأمعاء لزيادة امتصاص الكالسيوم الغذائي. يتم منع إطلاق PTH عن طريق ارتفاع مستويات الكالسيوم في الدم.
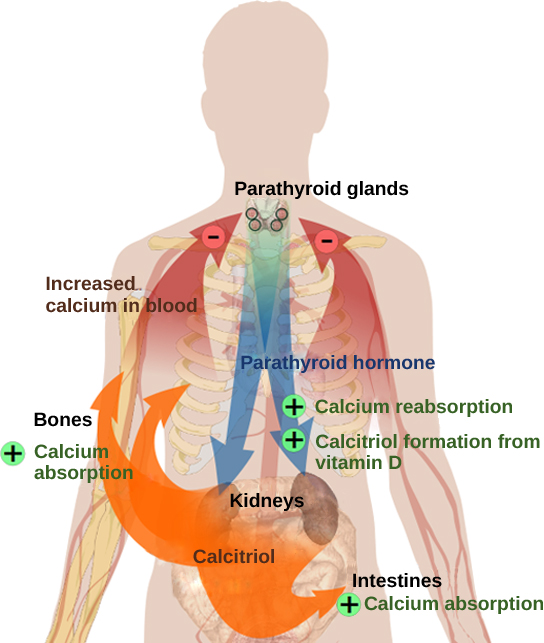
ينتج فرط نشاط جارات الدرق عن الإفراط في إنتاج هرمون الغدة الدرقية. يؤدي هذا إلى إزالة الكالسيوم الزائد من العظام وإدخاله في الدورة الدموية، مما يؤدي إلى ضعف هيكلي للعظام، مما قد يؤدي إلى التشوه والكسور، بالإضافة إلى ضعف الجهاز العصبي بسبب ارتفاع مستويات الكالسيوم في الدم. يؤدي نقص نشاط جارات الدرق، وهو نقص إنتاج PTH، إلى مستويات منخفضة للغاية من الكالسيوم في الدم، مما يؤدي إلى ضعف وظائف العضلات وقد يؤدي إلى تكزز (تقلص العضلات الشديد المستمر).
هرمون الكالسيتونين، الذي تنتجه الخلايا شبه الجزيئية أو C في الغدة الدرقية، له تأثير معاكوس على مستويات الكالسيوم في الدم كما يفعل PTH. يقلل الكالسيتونين من مستويات الكالسيوم في الدم عن طريق تثبيط الخلايا الآكلة للعظام وتحفيز بانيات العظم وتحفيز إفراز الكالسيوم عن طريق الكلى. يؤدي هذا إلى إضافة الكالسيوم إلى العظام لتعزيز السلامة الهيكلية. يعتبر الكالسيتونين أكثر أهمية عند الأطفال (عندما يحفز نمو العظام)، وأثناء الحمل (عندما يقلل من فقدان عظام الأم)، وأثناء الجوع لفترات طويلة (لأنه يقلل من فقدان كتلة العظام). في البالغين الأصحاء غير الحوامل وغير المتعطشين، يكون دور الكالسيتونين غير واضح.
التنظيم الهرموني للنمو
التنظيم الهرموني مطلوب لنمو وتكرار معظم الخلايا في الجسم. يعمل هرمون النمو (GH)، الذي ينتجه الجزء الأمامي من الغدة النخامية، على تسريع معدل تخليق البروتين، خاصة في العضلات والعظام الهيكلية. هرمون النمو له آليات عمل مباشرة وغير مباشرة. أول عمل مباشر لـ GH هو تحفيز تكسير الدهون الثلاثية (تحلل الدهون) وإطلاقها في الدم بواسطة الخلايا الشحمية. ينتج عن ذلك تحول معظم الأنسجة من استخدام الجلوكوز كمصدر للطاقة إلى استخدام الأحماض الدهنية. هذه العملية تسمى تأثير الحفاظ على الجلوكوز. في آلية مباشرة أخرى، يحفز هرمون النمو انهيار الجليكوجين في الكبد؛ ثم يتم إطلاق الجليكوجين في الدم على شكل جلوكوز. تزداد مستويات الجلوكوز في الدم حيث تستخدم معظم الأنسجة الأحماض الدهنية بدلاً من الجلوكوز لاحتياجاتها من الطاقة. يُطلق على الزيادة التي يتوسطها هرمون النمو في مستويات الجلوكوز في الدم تأثير السكري لأنها تشبه مستويات الجلوكوز المرتفعة في الدم التي تظهر في داء السكري.
يتم التوسط في الآلية غير المباشرة لعمل هرمون النمو من خلال عوامل النمو الشبيهة بالأنسولين (IGFs) أو السوماتوميدين، وهي عائلة من البروتينات المعززة للنمو التي ينتجها الكبد، والتي تحفز نمو الأنسجة. تحفز IGFs امتصاص الأحماض الأمينية من الدم، مما يسمح بتكوين بروتينات جديدة، خاصة في خلايا العضلات الهيكلية وخلايا الغضاريف والخلايا المستهدفة الأخرى، كما هو موضح في الشكل\(\PageIndex{7}\). هذا مهم بشكل خاص بعد الوجبة، عندما تكون مستويات تركيز الجلوكوز والأحماض الأمينية عالية في الدم. يتم تنظيم مستويات هرمون النمو بواسطة هرمونين ينتجهما منطقة ما تحت المهاد. يتم تحفيز إطلاق هرمون النمو عن طريق هرمون إفراز هرمون النمو (GHRH) ويتم تثبيطه بواسطة هرمون تثبيط هرمون النمو (GHIH)، والذي يسمى أيضًا السوماتوستاتين.
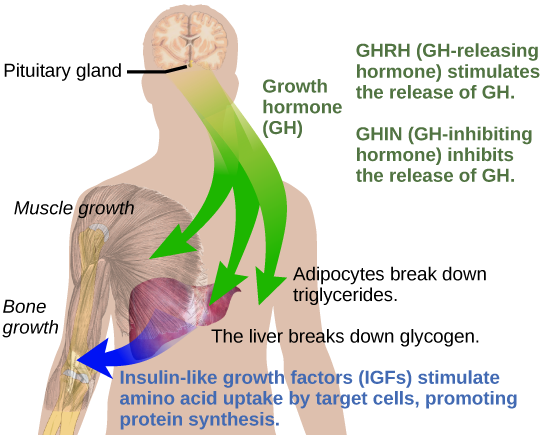
إن الإنتاج المتوازن لهرمون النمو أمر بالغ الأهمية للتطور السليم. لا يبدو أن نقص إنتاج هرمون النمو لدى البالغين يسبب أي تشوهات، ولكن عند الأطفال يمكن أن يؤدي إلى تقزم الغدة النخامية، حيث ينخفض النمو. يتميز تقزم الغدة النخامية بتكوين الجسم المتماثل. في بعض الحالات، يقل ارتفاع الأفراد عن 30 بوصة. يمكن أن يؤدي الإفراط في إفراز هرمون النمو إلى الإصابة بالعملاقة لدى الأطفال، مما يتسبب في نمو مفرط. في بعض الحالات الموثقة، يمكن للأفراد الوصول إلى ارتفاعات تزيد عن ثمانية أقدام. عند البالغين، يمكن أن يؤدي هرمون النمو المفرط إلى تضخم الأطراف، وهي حالة يحدث فيها تضخم في عظام الوجه واليدين والقدمين التي لا تزال قادرة على النمو.
التنظيم الهرموني للإجهاد
عندما يتم إدراك التهديد أو الخطر، يستجيب الجسم بإفراز الهرمونات التي ستجهزه لاستجابة «القتال أو الهروب». آثار هذه الاستجابة مألوفة لأي شخص كان في موقف مرهق: زيادة معدل ضربات القلب وجفاف الفم ووقوف الشعر.
اتصال التطور: استجابة القتال أو الطيران
تطورت تفاعلات هرمونات الغدد الصماء لضمان استقرار البيئة الداخلية للجسم. الضغوطات هي محفزات تعطل التوازن. أدى الانقسام الودي للجهاز العصبي اللاإرادي للفقاريات إلى تطوير استجابة القتال أو الطيران لمواجهة الاضطرابات الناجمة عن الإجهاد في التوازن. في مرحلة الإنذار الأولي، يحفز الجهاز العصبي الودي زيادة مستويات الطاقة من خلال زيادة مستويات الجلوكوز في الدم. هذا يهيئ الجسم للنشاط البدني الذي قد يكون مطلوبًا للاستجابة للتوتر: إما للقتال من أجل البقاء أو الفرار من الخطر.
ومع ذلك، يمكن أن تستمر بعض الضغوط، مثل المرض أو الإصابة، لفترة طويلة. يتم استنفاد احتياطيات الجليكوجين، التي توفر الطاقة في الاستجابة قصيرة المدى للتوتر، بعد عدة ساعات ولا يمكنها تلبية احتياجات الطاقة على المدى الطويل. إذا كانت احتياطيات الجليكوجين هي مصدر الطاقة الوحيد المتاح، فلا يمكن الحفاظ على الأداء العصبي بمجرد استنفاد الاحتياطيات بسبب ارتفاع متطلبات الجهاز العصبي للجلوكوز. في هذه الحالة، طور الجسم استجابة لمواجهة الإجهاد طويل الأمد من خلال إجراءات الجلوكوكورتيكويدات، التي تضمن إمكانية تلبية متطلبات الطاقة على المدى الطويل. تعمل الجلوكوكورتيكويدات على تعبئة احتياطيات الدهون والبروتين، وتحفيز تكوين الجلوكوز، والحفاظ على الجلوكوز لاستخدامه من قبل الأنسجة العصبية، وتحفيز الحفاظ على الأملاح والمياه. آليات الحفاظ على التوازن الموصوفة هنا هي تلك التي لوحظت في جسم الإنسان. ومع ذلك، فإن استجابة القتال أو الطيران موجودة بشكل ما في جميع الفقاريات.
ينظم الجهاز العصبي الودي الاستجابة للتوتر عبر منطقة ما تحت المهاد. تتسبب المنبهات المسببة للتوتر في قيام منطقة ما تحت المهاد بإرسال إشارة إلى النخاع الكظري (الذي يتوسط استجابات الإجهاد قصيرة المدى) عبر النبضات العصبية، وقشرة الغدة الكظرية، التي تتوسط استجابات الإجهاد على المدى الطويل، عن طريق هرمون الكظر القشري (ACTH)، الذي تنتجه الغدة النخامية الأمامية.
استجابة الإجهاد على المدى القصير
عند التعرض لموقف مرهق، يستجيب الجسم بالدعوة إلى إطلاق الهرمونات التي توفر دفعة من الطاقة. يتم إطلاق هرمونات الإيبينيفرين (المعروف أيضًا باسم الأدرينالين) والنورادرينالين (المعروف أيضًا باسم النورادرينالين) بواسطة النخاع الكظري. كيف توفر هذه الهرمونات دفعة من الطاقة؟ يعمل الإيبينيفرين والنورادرينالين على زيادة مستويات الجلوكوز في الدم عن طريق تحفيز الكبد والعضلات الهيكلية لتحطيم الجليكوجين وتحفيز إطلاق الجلوكوز بواسطة خلايا الكبد. بالإضافة إلى ذلك، تزيد هذه الهرمونات من توافر الأكسجين للخلايا عن طريق زيادة معدل ضربات القلب وتوسيع القصبات الهوائية. كما تعطي الهرمونات الأولوية لوظائف الجسم عن طريق زيادة إمدادات الدم إلى الأعضاء الأساسية مثل القلب والدماغ والعضلات الهيكلية، مع تقييد تدفق الدم إلى الأعضاء التي ليست في حاجة ماسة إليها، مثل الجلد والجهاز الهضمي والكلى. يُطلق على الإيبينيفرين والنورادرينالين بشكل جماعي اسم الكاتيكولامينات.
رابط إلى التعلم
شاهد هذه الرسوم المتحركة لقناة Discovery التي تصف الاستجابة للرحلة أو الرحلة.
استجابة الإجهاد على المدى الطويل
تختلف الاستجابة للتوتر على المدى الطويل عن الاستجابة للضغط على المدى القصير. لا يستطيع الجسم تحمل دفعات الطاقة بوساطة الإيبينيفرين والنورادرينالين لفترات طويلة. بدلاً من ذلك، تلعب الهرمونات الأخرى دورًا. في الاستجابة للإجهاد على المدى الطويل، يؤدي المهاد إلى إطلاق ACTH من الغدة النخامية الأمامية. يتم تحفيز قشرة الغدة الكظرية بواسطة ACTH لإطلاق هرمونات الستيرويد التي تسمى الكورتيكوستيرويدات. تعمل الكورتيكوستيرويدات على نسخ جينات معينة في نواة الخلايا المستهدفة. إنها تغير تركيزات الإنزيم في السيتوبلازم وتؤثر على التمثيل الغذائي الخلوي. هناك نوعان من الكورتيكوستيرويدات الرئيسية: الجلوكوكورتيكويدات مثل الكورتيزول، والكورتيكويدات المعدنية مثل الألدوستيرون. تستهدف هذه الهرمونات تكسير الدهون إلى أحماض دهنية في الأنسجة الدهنية. يتم إطلاق الأحماض الدهنية في مجرى الدم للأنسجة الأخرى لاستخدامها في إنتاج ATP. تؤثر الجلوكوكورتيكويدات بشكل أساسي على استقلاب الجلوكوز عن طريق تحفيز تخليق الجلوكوز. تحتوي الجلوكوكورتيكويدات أيضًا على خصائص مضادة للالتهابات من خلال تثبيط جهاز المناعة. على سبيل المثال، يستخدم الكورتيزون كدواء مضاد للالتهابات؛ ومع ذلك، لا يمكن استخدامه على المدى الطويل لأنه يزيد من القابلية للإصابة بالأمراض بسبب آثاره المثبطة للمناعة.
تعمل مينيرالوكورتيكويدات على تنظيم توازن الأيونات والماء في الجسم. يحفز هرمون الألدوستيرون إعادة امتصاص الماء وأيونات الصوديوم في الكلى، مما يؤدي إلى زيادة ضغط الدم وحجمه.
يمكن أن يسبب فرط إفراز الجلوكوكورتيكويدات حالة تعرف باسم مرض كوشينغ، والتي تتميز بتغيير مناطق تخزين الدهون في الجسم. هذا يمكن أن يسبب تراكم الأنسجة الدهنية في الوجه والرقبة، والجلوكوز المفرط في الدم. يمكن أن يسبب نقص إفراز الكورتيكوستيرويدات مرض أديسون، مما قد يؤدي إلى تسمير الجلد ونقص السكر في الدم وانخفاض مستويات الإلكتروليت في الدم.
ملخص
يتم التحكم في مستويات الماء في الجسم عن طريق الهرمون المضاد لإدرار البول (ADH)، الذي يتم إنتاجه في منطقة ما تحت المهاد ويؤدي إلى إعادة امتصاص الماء عن طريق الكلى. يمكن أن يسبب نقص إنتاج ADH مرض السكري الكاذب. يعزز الألدوستيرون، وهو هرمون تنتجه قشرة الغدة الكظرية في الكلى، إعادة امتصاص Na + من السوائل خارج الخلية وإعادة امتصاص الماء لاحقًا عن طريق الانتشار. نظام الرينين-أنجيوتنسين-الألدوستيرون هو إحدى الطرق التي يتم بها التحكم في إطلاق الألدوستيرون.
يتم التحكم في الجهاز التناسلي عن طريق هرمون تحفيز بصيلات الجونادوتروبين (FSH) والهرمون اللوتيني (LH)، اللذان تنتجهما الغدة النخامية. يتم التحكم في إطلاق الجونادوتروبين بواسطة هرمون ما تحت المهاد هرمون إفراز الجونادوتروبين (GnRH). يحفز FSH نضوج خلايا الحيوانات المنوية عند الذكور ويتم تثبيطه بواسطة الهرمون المثبط، بينما يحفز LH إنتاج هرمون التستوستيرون الأندروجين. يحفز FSH نضوج البيض عند الإناث، بينما يحفز LH إنتاج هرمون الاستروجين والبروجسترون. الإستروجين عبارة عن مجموعة من هرمونات الستيرويد التي تنتجها المبايض والتي تحفز تطور الخصائص الجنسية الثانوية لدى الإناث وكذلك تتحكم في نضوج البويضة. في الإناث، تنتج الغدة النخامية أيضًا البرولاكتين، الذي يحفز إنتاج الحليب بعد الولادة، والأوكسيتوسين، الذي يحفز تقلص الرحم أثناء الولادة وتراجع الحليب أثناء الرضاعة.
ينتج البنكرياس الأنسولين استجابة لارتفاع مستويات الجلوكوز في الدم ويسمح للخلايا باستخدام جلوكوز الدم وتخزين الجلوكوز الزائد لاستخدامه لاحقًا. يحدث داء السكري بسبب انخفاض نشاط الأنسولين ويسبب ارتفاع مستويات الجلوكوز في الدم أو ارتفاع السكر في الدم. يتم إطلاق الجلوكاجون بواسطة البنكرياس استجابة لانخفاض مستويات الجلوكوز في الدم ويحفز تكسير الجليكوجين إلى جلوكوز، والذي يمكن أن يستخدمه الجسم. يتم التحكم في معدل الأيض القاعدي في الجسم عن طريق هرمونات الغدة الدرقية الثيروكسين (T 4) وثلاثي يودوثيرونين (T 3). تنتج الغدة النخامية الأمامية هرمون تحفيز الغدة الدرقية (TSH)، الذي يتحكم في إطلاق T 3 و T 4 من الغدة الدرقية. اليود ضروري في إنتاج هرمون الغدة الدرقية، ويمكن أن يؤدي نقص اليود إلى حالة تسمى تضخم الغدة الدرقية.
يتم إنتاج هرمون الغدة الدرقية (PTH) بواسطة الغدد فوق الدرقية استجابة لانخفاض مستويات Ca 2+ في الدم. تنتج الخلايا شبه الجزيئية للغدة الدرقية الكالسيتونين، مما يقلل من مستويات Ca 2+ في الدم. يتم إنتاج هرمون النمو (GH) بواسطة الغدة النخامية الأمامية ويتحكم في معدل نمو العضلات والعظام. يتم التوسط في عمل GH بشكل غير مباشر من خلال عوامل النمو الشبيهة بالأنسولين (IGFs). يؤدي الإجهاد قصير المدى إلى تحفيز منطقة ما تحت المهاد لنخاع الغدة الكظرية لإطلاق الإيبينيفرين والنورادرينالين، مما يؤدي إلى الاستجابة للقتال أو الهروب. يؤدي الإجهاد طويل الأمد إلى قيام منطقة ما تحت المهاد بحفز الغدة النخامية الأمامية على إطلاق هرمون الكظر القشري (ACTH)، الذي يتسبب في إطلاق الكورتيكوستيرويدات والجلوكوكورتيكويدات والقشرية المعدنية من قشرة الغدة الكظرية.
مسرد المصطلحات
- تضخم الأطراف
- الحالة الناجمة عن الإفراط في إنتاج هرمون النمو لدى البالغين
- مرض أديسون
- اضطراب ناتج عن نقص إفراز الكورتيكوستيرويدات
- هرمون الكظر القشري (ACTH)
- الهرمون الذي تطلقه الغدة النخامية الأمامية، والذي يحفز قشرة الغدة الكظرية على إطلاق الكورتيكوستيرويدات أثناء الاستجابة للإجهاد على المدى الطويل
- الألدوستيرون
- هرمون الستيرويد الذي تنتجه قشرة الغدة الكظرية الذي يحفز إعادة امتصاص Na + من السوائل خارج الخلية وإفراز K +.
- الأندروجين
- هرمون الذكورة مثل هرمون التستوستيرون
- هرمون مضاد لإدرار البول (ADH)
- هرمون ينتجه المهاد ويطلقه الغدة النخامية الخلفية مما يزيد من إعادة امتصاص الماء عن طريق الكلى
- كالسيتونين
- الهرمون الذي تنتجه الخلايا شبه الجزيئية للغدة الدرقية والذي يعمل على خفض مستويات Ca 2+ في الدم وتعزيز نمو العظام
- كورتيكوستيرويد
- هرمون تطلقه قشرة الغدة الكظرية استجابة للإجهاد طويل الأمد
- الكورتيزول
- يتم إنتاج الجلوكوكورتيكويد استجابة للإجهاد
- مرض كوشينج
- اضطراب ناتج عن فرط إفراز الجلوكوكورتيكويدات
- مرض السكري الكاذب
- اضطراب ناتج عن نقص إنتاج ADH
- داء السكري
- اضطراب ناتج عن انخفاض مستويات نشاط الأنسولين
- تأثير السكري
- تأثير هرمون النمو الذي يؤدي إلى ارتفاع مستويات الجلوكوز في الدم على غرار داء السكري
- ادرينالين
- هرمون يفرزه النخاع الكظري استجابة لضغط قصير المدى
- هرمون الاستروجين
- - مجموعة من هرمونات الستيرويد، بما في ذلك الاستراديول والعديد من الهرمونات الأخرى، التي ينتجها المبيضان وتستخرج الخصائص الجنسية الثانوية لدى الإناث وكذلك تتحكم في نضوج البويضة
- هرمون تحفيز الجريبات (FSH)
- هرمون تنتجه الغدة النخامية الأمامية التي تحفز إنتاج الأمشاج
- العملقة
- الحالة الناجمة عن الإفراط في إنتاج هرمون النمو لدى الأطفال
- الجلوكاجون
- هرمون تنتجه خلايا ألفا في البنكرياس استجابة لانخفاض نسبة السكر في الدم؛ يعمل على رفع مستويات السكر في الدم
- جلايكورتيكود
- كورتيكوستيرويد الذي يؤثر على استقلاب الجلوكوز
- تكوين السكر
- تخليق الجلوكوز من الأحماض الأمينية
- تأثير حفظ الجلوكوز
- تأثير هرمون النمو الذي يجعل الأنسجة تستخدم الأحماض الدهنية بدلاً من الجلوكوز كمصدر للطاقة
- تحلل الغليكوجين
- انهيار الجليكوجين إلى جلوكوز
- تضخم الغدة الدرقية
- تضخم الغدة الدرقية بسبب عدم كفاية مستويات اليود الغذائية
- الجونادوتروبين
- الهرمون الذي ينظم الغدد التناسلية، بما في ذلك FSH و LH
- هرمون النمو (GH)
- هرمون تنتجه الغدة النخامية الأمامية التي تعزز تخليق البروتين ونمو الجسم
- هرمون تثبيط هرمون النمو (GHIH)
- هرمون ينتجه المهاد الذي يمنع إنتاج هرمون النمو، ويسمى أيضًا السوماتوستاتين
- هرمون إفراز هرمون النمو (GHRH)
- الهرمون الصادر عن منطقة ما تحت المهاد الذي يؤدي إلى إطلاق هرمون النمو
- فرط سكر الدم
- ارتفاع مستوى السكر في الدم
- فرط الدرقية
- فرط نشاط الغدة الدرقية
- نقص السكر
- انخفاض مستوى السكر في الدم
- قصور الغدة الدرقية
- نقص نشاط الغدة الدرقية
- إنسولين
- هرمون تنتجه خلايا بيتا في البنكرياس استجابة لارتفاع مستويات الجلوكوز في الدم؛ يعمل على خفض مستويات الجلوكوز في الدم
- عامل النمو الشبيه بالأنسولين (IGF)
- البروتين المعزز للنمو الذي ينتجه الكبد
- مينيرالوكورتيكويد
- كورتيكوستيرويد يؤثر على توازن الأيونات والماء
- بافراز
- هرمون يفرزه النخاع الكظري استجابة لإنتاج هرمون الإجهاد قصير المدى بواسطة الغدد التناسلية
- مستقبل التناضح
- مستقبلات في منطقة ما تحت المهاد تراقب تركيز الإلكتروليتات في الدم
- الأوكسيتوسين
- الهرمون الذي تطلقه الغدة النخامية الخلفية لتحفيز تقلصات الرحم أثناء الولادة وتراجع الحليب في الغدد الثديية
- هرمون الغدة الدرقية (PTH)
- هرمون تنتجه الغدد فوق الدرقية استجابة لانخفاض مستويات Ca 2+ في الدم؛ يعمل على رفع مستويات Ca 2+ في الدم
- قزامة الغدة النخامية
- الحالة الناجمة عن نقص إنتاج هرمون النمو لدى الأطفال
- برولاكتين (PRL)
- هرمون تنتجه الغدة النخامية الأمامية التي تحفز إنتاج الحليب
- هرمون تثبيط البرولاكتين
- هرمون ينتجه المهاد الذي يمنع إفراز البرولاكتين
- هرمون إفراز البرولاكتين
- هرمون ينتجه المهاد الذي يحفز إفراز البرولاكتين
- رينين
- إنزيم ينتجه الجهاز الجاكستالوميري للكلى الذي يتفاعل مع الأنجيوتنسينوجين للتسبب في إطلاق الألدوستيرون
- ثايروجلوبولين
- بروتين سكري موجود في الغدة الدرقية يتم تحويله إلى هرمون الغدة الدرقية
- هرمون تحفيز الغدة الدرقية (TSH)
- هرمون تنتجه الغدة النخامية الأمامية التي تتحكم في إطلاق T 3 و T 4 من الغدة الدرقية
- هرمون الغدة الدرقية (تيترايودوثيرونين، T 4)
- هرمون الغدة الدرقية الذي يتحكم في معدل الأيض القاعدي
- ثلاثي يودوثيرونين (T 3)
- هرمون الغدة الدرقية الذي يتحكم في معدل الأيض القاعدي


