17.2: الهرمونات
- Page ID
- 203074
أهداف التعلم
- حدد الفئات الرئيسية الثلاث للهرمونات على أساس التركيب الكيميائي
- قارن وقارن بين مستقبلات الهرمونات داخل الخلايا والغشاء الخلوي
- وصف مسارات إرسال الإشارات التي تتضمن CamP وIP3
- حدد العديد من العوامل التي تؤثر على استجابة الخلية المستهدفة
- ناقش دور حلقات التغذية الراجعة والمحفزات الخلطية والهرمونية والعصبية في التحكم بالهرمونات
على الرغم من أن هرمونًا معينًا قد ينتقل في جميع أنحاء الجسم في مجرى الدم، إلا أنه سيؤثر على نشاط الخلايا المستهدفة فقط؛ أي الخلايا ذات المستقبلات لهذا الهرمون المحدد. بمجرد ارتباط الهرمون بالمستقبل، تبدأ سلسلة من الأحداث التي تؤدي إلى استجابة الخلية المستهدفة. تلعب الهرمونات دورًا مهمًا في تنظيم العمليات الفسيولوجية بسبب استجابات الخلايا المستهدفة التي تنظمها. تساهم هذه الاستجابات في التكاثر البشري ونمو وتطور أنسجة الجسم والتمثيل الغذائي وتوازن السوائل والكهارل والنوم والعديد من وظائف الجسم الأخرى. يتم تحديد الهرمونات الرئيسية لجسم الإنسان وتأثيراتها في الجدول\(\PageIndex{1}\).
| غدة صماء | الهرمونات المصاحبة | فئة كيميائية | تأثير |
|---|---|---|---|
| الغدة النخامية (الأمامية) | هرمون النمو (GH) | بروتين | يعزز نمو أنسجة الجسم |
| الغدة النخامية (الأمامية) | برولاكتين (PRL) | الببتيد | يعزز إنتاج الحليب |
| الغدة النخامية (الأمامية) | هرمون تحفيز الغدة الدرقية (TSH) | بروتين سكري | يحفز إطلاق هرمون الغدة الدرقية |
| الغدة النخامية (الأمامية) | هرمون الكظر القشري (ACTH) | الببتيد | يحفز إفراز الهرمونات عن طريق قشرة الغدة الكظرية |
| الغدة النخامية (الأمامية) | هرمون تحفيز الجريبات (FSH) | بروتين سكري | يحفز إنتاج الأمشاج |
| الغدة النخامية (الأمامية) | الهرمون اللوتيني (LH) | بروتين سكري | يحفز إنتاج الأندروجين عن طريق الغدد التناسلية |
| الغدة النخامية (الخلفية) | الهرمون المضاد لإدرار البول (ADH) | الببتيد | يحفز إعادة امتصاص الماء عن طريق الكلى |
| الغدة النخامية (الخلفية) | أوكسي | الببتيد | يحفز تقلصات الرحم أثناء الولادة |
| الغدة الدرقية | هرمون الغدة الدرقية (T 4)، ثلاثي يودوثيرونين (T 3) | آمين | تحفيز معدل الأيض القاعدي |
| الغدة الدرقية | كالسيتونين | الببتيد | يقلل من مستويات Ca 2+ في الدم |
| جار درقية | هرمون الغدة الدرقية (PTH) | الببتيد | يزيد من مستويات Ca 2+ في الدم |
| قشرة الغدة الكظرية | الألدوستيرون | ستيرويد | يزيد من مستويات Na + في الدم |
| قشرة الغدة الكظرية | الكورتيزول، الكورتيكوستيرون، الكورتيزون | ستيرويد | زيادة مستويات الجلوكوز في الدم |
| الغدة الكظرية (النخاع) | الإيبينيفرين والنورادرينالين | آمين | تحفيز الاستجابة للقتال أو الطيران |
| الصنوبرية | ميلاتونين | آمين | ينظم دورات النوم |
| البنكرياس | الأنسولين | بروتين | يقلل من مستويات الجلوكوز في الدم |
| البنكرياس | الجلوكاجون | بروتين | يزيد من مستويات الجلوكوز في الدم |
| الخصيتين | هرمون التستوستيرون | ستيرويد | يحفز تطوير الخصائص الجنسية الثانوية للذكور وإنتاج الحيوانات المنوية |
| المبايض | هرمون الاستروجين والبروجستيرون | ستيرويد | تحفيز تطوير الخصائص الجنسية الثانوية للإناث وإعداد الجسم للولادة |
أنواع الهرمونات
يمكن تقسيم هرمونات الجسم البشري إلى مجموعتين رئيسيتين على أساس تركيبها الكيميائي. تشمل الهرمونات المشتقة من الأحماض الأمينية الأمينات والببتيدات والبروتينات. تلك المشتقة من الدهون تشمل المنشطات (الشكل\(\PageIndex{1}\)). تؤثر هذه المجموعات الكيميائية على توزيع الهرمون ونوع المستقبلات التي يرتبط بها والجوانب الأخرى لوظيفته.

الهرمونات الأمينية
يشار إلى الهرمونات المشتقة من تعديل الأحماض الأمينية باسم الهرمونات الأمينية. عادةً ما يتم تعديل البنية الأصلية للحمض الأميني بحيث تتم إزالة مجموعة —COOH أو الكربوكسيل، بينما تبقى مجموعة NH 3+، أو الأمين.
يتم تصنيع الهرمونات الأمينية من الأحماض الأمينية التربتوفان أو التيروزين. مثال على هرمون مشتق من التربتوفان هو الميلاتونين، الذي تفرزه الغدة الصنوبرية ويساعد على تنظيم إيقاع الساعة البيولوجية. تشمل مشتقات التيروزين هرمونات الغدة الدرقية المنظمة لعملية التمثيل الغذائي، وكذلك الكاتيكولامينات، مثل الإيبينيفرين والنورادرينالين والدوبامين. يُفرز النخاع الكظري الإيبينيفرين والنورادرينالين ويلعبان دورًا في الاستجابة للقتال أو الطيران، بينما يفرز الدوبامين في منطقة ما تحت المهاد ويمنع إفراز بعض هرمونات الغدة النخامية الأمامية.
هرمونات الببتيد والبروتين
في حين أن الهرمونات الأمينية مشتقة من حمض أميني واحد، فإن هرمونات الببتيد والبروتين تتكون من أحماض أمينية متعددة ترتبط لتشكيل سلسلة من الأحماض الأمينية. تتكون هرمونات الببتيد من سلاسل قصيرة من الأحماض الأمينية، في حين أن هرمونات البروتين هي بولي ببتيدات أطول. يتم تصنيع كلا النوعين مثل بروتينات الجسم الأخرى: يتم نسخ الحمض النووي إلى mRNA، والذي يتم ترجمته إلى سلسلة الأحماض الأمينية.
تشمل أمثلة هرمونات الببتيد الهرمون المضاد لإدرار البول (ADH)، وهو هرمون الغدة النخامية المهم في توازن السوائل، والببتيد الأذيني الناتريوتريك، الذي ينتجه القلب ويساعد على خفض ضغط الدم. بعض الأمثلة على هرمونات البروتين تشمل هرمون النمو، الذي تنتجه الغدة النخامية، وهرمون تحفيز الجريبات (FSH)، الذي يحتوي على مجموعة كربوهيدرات مرتبطة وبالتالي يتم تصنيفه على أنه بروتين سكري. يساعد FSH على تحفيز نضوج البويضات في المبايض والحيوانات المنوية في الخصيتين.
هرمونات ستيرويد
الهرمونات الأولية المشتقة من الدهون هي الستيرويدات. يتم اشتقاق هرمونات الستيرويد من الكوليسترول الدهني. على سبيل المثال، الهرمونات التناسلية التستوستيرون والإستروجين - التي تنتجها الغدد التناسلية (الخصيتين والمبايض) - هي هرمونات الستيرويد. تنتج الغدد الكظرية هرمون الستيرويد الألدوستيرون، الذي يشارك في تنظيم التناضح، والكورتيزول، الذي يلعب دورًا في عملية التمثيل الغذائي.
مثل الكوليسترول، هرمونات الستيرويد غير قابلة للذوبان في الماء (فهي كارهة للماء). نظرًا لأن الدم يعتمد على الماء، يجب أن تنتقل الهرمونات المشتقة من الدهون إلى الخلية المستهدفة المرتبطة ببروتين النقل. تعمل هذه البنية الأكثر تعقيدًا على إطالة عمر هرمونات الستيرويد لفترة أطول بكثير من الهرمونات المشتقة من الأحماض الأمينية. نصف عمر الهرمون هو الوقت اللازم لتدهور نصف تركيز الهرمون. على سبيل المثال، يبلغ عمر النصف لهرمون الكورتيزول المشتق من الدهون حوالي 60 إلى 90 دقيقة. في المقابل، يبلغ عمر النصف لهرمون الإيبينيفرين المشتق من الأحماض الأمينية دقيقة واحدة تقريبًا.
مسارات عمل الهرمونات
يتم استقبال الرسالة التي يرسلها الهرمون بواسطة مستقبل الهرمون، وهو بروتين موجود إما داخل الخلية أو داخل غشاء الخلية. سيقوم المستقبل بمعالجة الرسالة عن طريق بدء أحداث إشارة أخرى أو آليات خلوية تؤدي إلى استجابة الخلية المستهدفة. تتعرف مستقبلات الهرمونات على الجزيئات ذات الأشكال والمجموعات الجانبية المحددة، وتستجيب فقط لتلك الهرمونات التي يتم التعرف عليها. قد يوجد نفس النوع من المستقبلات على خلايا في أنسجة الجسم المختلفة، ويؤدي إلى استجابات مختلفة نوعًا ما. وبالتالي، فإن الاستجابة التي يسببها الهرمون لا تعتمد فقط على الهرمون، ولكن أيضًا على الخلية المستهدفة.
بمجرد أن تتلقى الخلية المستهدفة إشارة الهرمون، يمكنها الاستجابة بعدة طرق. قد تشمل الاستجابة تحفيز تخليق البروتين، وتنشيط الإنزيمات أو تعطيلها، وتغيير نفاذية غشاء الخلية، وتغيير معدلات الانقسام ونمو الخلايا، وتحفيز إفراز المنتجات. علاوة على ذلك، قد يكون هرمون واحد قادرًا على تحفيز استجابات مختلفة في خلية معينة.
المسارات التي تشمل مستقبلات الهرمونات داخل الخلايا
توجد مستقبلات الهرمون داخل الخلايا داخل الخلية. يجب أن تكون الهرمونات المرتبطة بهذا النوع من المستقبلات قادرة على عبور غشاء الخلية. تُشتق هرمونات الستيرويد من الكوليسترول وبالتالي يمكن أن تنتشر بسهولة من خلال الطبقة الثنائية الدهنية لغشاء الخلية للوصول إلى المستقبل داخل الخلايا (الشكل\(\PageIndex{2}\)). كما أن هرمونات الغدة الدرقية، التي تحتوي على حلقات بنزين مرصعة باليود، قابلة للذوبان في الدهون ويمكن أن تدخل الخلية.
يختلف موقع ارتباط الستيرويد وهرمون الغدة الدرقية اختلافًا طفيفًا: قد يرتبط هرمون الستيرويد بمستقبله داخل السيتوسول أو داخل النواة. في كلتا الحالتين، ينتج هذا الارتباط مركب مستقبلات الهرمونات الذي يتحرك نحو الكروماتين في نواة الخلية ويرتبط بجزء معين من الحمض النووي للخلية. في المقابل، ترتبط هرمونات الغدة الدرقية بالمستقبلات المرتبطة بالفعل بالحمض النووي. بالنسبة لكل من هرمونات الستيرويد والغدة الدرقية، يؤدي ربط مركب مستقبلات الهرمونات بالحمض النووي إلى نسخ الجين المستهدف إلى mRNA، الذي ينتقل إلى السيتوسول ويوجه تخليق البروتين بواسطة الريبوسومات.

المسارات التي تشمل مستقبلات هرمون الغشاء الخلوي
الهرمونات المحبة للماء أو القابلة للذوبان في الماء غير قادرة على الانتشار عبر الطبقة الدهنية لغشاء الخلية وبالتالي يجب أن تنقل رسالتها إلى مستقبل موجود على سطح الخلية. باستثناء هرمونات الغدة الدرقية القابلة للذوبان في الدهون، ترتبط جميع الهرمونات المشتقة من الأحماض الأمينية بمستقبلات غشاء الخلية الموجودة، جزئيًا على الأقل، على السطح خارج الخلية لغشاء الخلية. لذلك، لا تؤثر بشكل مباشر على نسخ الجينات المستهدفة، ولكنها بدلاً من ذلك تبدأ سلسلة إشارات يتم تنفيذها بواسطة جزيء يسمى الرسول الثاني. في هذه الحالة، يُطلق على الهرمون اسم الرسول الأول.
المرسل الثاني الذي تستخدمه معظم الهرمونات هو أحادي فوسفات الأدينوزين الدوري (CamP). في نظام المراسلة الثاني cAMP، يرتبط هرمون قابل للذوبان في الماء بمستقبله في غشاء الخلية (الخطوة 1 في الشكل\(\PageIndex{3}\)). يرتبط هذا المستقبل بمكون داخل الخلايا يسمى بروتين G، ويؤدي ارتباط الهرمون إلى تنشيط مكون بروتين G (الخطوة 2). يقوم بروتين G المنشط بدوره بتنشيط إنزيم يسمى أدينيليل سيكلاز، المعروف أيضًا باسم أدينيلات سيكلاز (الخطوة 3)، والذي يحول أدينوزين ثلاثي الفوسفات (ATP) إلى CamP (الخطوة 4). بصفته المرسول الثاني، يقوم CamP بتنشيط نوع من الإنزيمات يسمى بروتين كيناز الموجود في السيتوسول (الخطوة 5). تبدأ كينازات البروتين المنشط سلسلة من الفسفرة، حيث تتفسور كينازات البروتين المتعددة (تضيف مجموعة فوسفات إلى) العديد من البروتينات الخلوية المختلفة، بما في ذلك الإنزيمات الأخرى (الخطوة 6).

يمكن أن تؤدي فسفرة البروتينات الخلوية إلى مجموعة متنوعة من التأثيرات، من استقلاب المغذيات إلى تخليق الهرمونات المختلفة والمنتجات الأخرى. تختلف التأثيرات وفقًا لنوع الخلية المستهدفة، وبروتينات G والكينازات المعنية، وفسفرة البروتينات. تشمل أمثلة الهرمونات التي تستخدم CamP كرسول ثانٍ الكالسيتونين، وهو أمر مهم لبناء العظام وتنظيم مستويات الكالسيوم في الدم؛ والجلوكاجون، الذي يلعب دورًا في مستويات الجلوكوز في الدم؛ وهرمون تحفيز الغدة الدرقية، الذي يتسبب في إطلاق T 3 و T 4 من الغدة الدرقية.
بشكل عام، تزيد سلسلة الفسفرة بشكل كبير من كفاءة وسرعة وخصوصية الاستجابة الهرمونية، حيث يمكن بدء الآلاف من أحداث الإشارة في وقت واحد استجابة لتركيز منخفض جدًا من الهرمون في مجرى الدم. ومع ذلك، فإن مدة إشارة الهرمون قصيرة، حيث يتم تعطيل CaMP بسرعة بواسطة إنزيم فوسفوديستراس (PDE)، الموجود في السيتوسول. يساعد عمل PDE على ضمان توقف استجابة الخلية المستهدفة بسرعة ما لم تصل هرمونات جديدة إلى غشاء الخلية.
الأهم من ذلك، هناك أيضًا بروتينات G التي تقلل من مستويات CamP في الخلية استجابة لارتباط الهرمونات. على سبيل المثال، عندما يرتبط هرمون تثبيط هرمون النمو (GHIH)، المعروف أيضًا باسم السوماتوستاتين، بمستقبلاته في الغدة النخامية، ينخفض مستوى CamP، وبالتالي يثبط إفراز هرمون النمو البشري.
لا تقوم جميع الهرمونات القابلة للذوبان في الماء بتشغيل نظام المراسلة الثاني CamP. يستخدم أحد الأنظمة البديلة الشائعة أيونات الكالسيوم كرسول ثانٍ. في هذا النظام، تقوم بروتينات G بتنشيط إنزيم فوسفوليباز C (PLC)، والذي يعمل بشكل مشابه لأدنيليل سيكلاز. بمجرد تنشيطه، يقوم PLC بتقسيم الفوسفوليبيد المرتبط بالغشاء إلى جزيئين: ثنائي الجلسرين (DAG) وإينوزيتول ثلاثي الفوسفات (IP 3). مثل CamP، ينشط DAG كينازات البروتين التي تبدأ سلسلة الفسفرة. في الوقت نفسه، يتسبب IP 3 في إطلاق أيونات الكالسيوم من مواقع التخزين داخل السيتوسول، مثل داخل الشبكة الإندوبلازمية الملساء. تعمل أيونات الكالسيوم بعد ذلك كناقلات ثانية بطريقتين: يمكنها التأثير على الأنشطة الأنزيمية وغيرها من الأنشطة الخلوية بشكل مباشر، أو يمكنها الارتباط بالبروتينات الرابطة للكالسيوم، وأكثرها شيوعًا هو الكالمودولين. عند ربط الكالسيوم، يكون الكالمودولين قادرًا على تعديل كيناز البروتين داخل الخلية. تشمل أمثلة الهرمونات التي تستخدم أيونات الكالسيوم كنظام مراسلة ثانٍ الأنجيوتنسين II، الذي يساعد على تنظيم ضغط الدم من خلال تضيق الأوعية، وهرمون إفراز هرمون النمو (GHRH)، الذي يتسبب في إفراز الغدة النخامية لهرمونات النمو.
العوامل المؤثرة على استجابة الخلايا المستهدفة
سوف تتذكر أن الخلايا المستهدفة يجب أن تحتوي على مستقبلات خاصة بهرمون معين إذا كان هذا الهرمون سيؤدي إلى استجابة. لكن هناك العديد من العوامل الأخرى التي تؤثر على استجابة الخلية المستهدفة. على سبيل المثال، يمكن أن يؤدي وجود مستوى كبير من الهرمون المتداول في مجرى الدم إلى تقليل الخلايا المستهدفة لعدد مستقبلاتها لهذا الهرمون. تسمى هذه العملية بالتخفيف، وتسمح للخلايا بأن تصبح أقل تفاعلًا مع مستويات الهرمون الزائدة. عندما ينخفض مستوى الهرمون بشكل مزمن، تنخرط الخلايا المستهدفة في التنظيم لزيادة عدد المستقبلات. تسمح هذه العملية للخلايا بأن تكون أكثر حساسية للهرمون الموجود. يمكن للخلايا أيضًا تغيير حساسية المستقبلات نفسها للهرمونات المختلفة.
يمكن أن يتفاعل هرمونان أو أكثر للتأثير على استجابة الخلايا بعدة طرق. الأنواع الثلاثة الأكثر شيوعًا للتفاعل هي كما يلي:
- التأثير المتساهل، حيث يؤدي وجود هرمون واحد إلى تمكين هرمون آخر من العمل. على سبيل المثال، تحتوي هرمونات الغدة الدرقية على علاقات تساهلية معقدة مع بعض الهرمونات التناسلية. لذلك يمكن أن يؤثر نقص اليود الغذائي، وهو أحد مكونات هرمونات الغدة الدرقية، على تطور الجهاز التناسلي وعمله.
- التأثير التآزري، حيث ينتج هرمونان لهما تأثيرات متشابهة استجابة مضخمة. في بعض الحالات، يلزم وجود هرمونين للاستجابة الكافية. على سبيل المثال، هناك حاجة إلى هرمونين تناسليين مختلفين - FSH من الغدة النخامية والإستروجين من المبيضين - لنضج البويضات الأنثوية (خلايا البويضات).
- التأثير المضاد، حيث يكون لهرمونين تأثيرات متعارضة. والمثال المألوف هو تأثير اثنين من هرمونات البنكرياس، الأنسولين والجلوكاجون. يزيد الأنسولين من تخزين الكبد للجلوكوز في صورة جليكوجين، مما يقلل من نسبة الجلوكوز في الدم، بينما يحفز الجلوكاجون تكسير مخازن الجليكوجين، مما يزيد من نسبة الجلوكوز في الدم.
تنظيم إفراز الهرمون
لمنع مستويات الهرمون غير الطبيعية وحالة المرض المحتملة، يجب التحكم في مستويات الهرمون بإحكام. يحافظ الجسم على هذه السيطرة من خلال موازنة إنتاج الهرمونات وتدهورها. تتحكم حلقات التغذية الراجعة في بدء معظم إفراز الهرمونات والحفاظ عليه استجابة للمنبهات المختلفة.
دور حلقات التغذية الراجعة
ستتم مراجعة مساهمة حلقات التغذية الراجعة في التوازن هنا لفترة وجيزة فقط. تتميز حلقات التغذية الراجعة الإيجابية بإطلاق هرمون إضافي استجابة لإطلاق هرمون أصلي. يعد إطلاق الأوكسيتوسين أثناء الولادة حلقة ردود فعل إيجابية. يبدأ الإطلاق الأولي للأوكسيتوسين في الإشارة إلى تقلص عضلات الرحم، مما يدفع الجنين نحو عنق الرحم، مما يؤدي إلى تمديده. وهذا بدوره يشير إلى أن الغدة النخامية تطلق المزيد من الأوكسيتوسين، مما يؤدي إلى تكثيف تقلصات المخاض. ينخفض إطلاق الأوكسيتوسين بعد ولادة الطفل.
الطريقة الأكثر شيوعًا لتنظيم الهرمونات هي حلقة التغذية الراجعة السلبية. تتميز ردود الفعل السلبية بتثبيط إفراز المزيد من الهرمون استجابة لمستويات كافية من هذا الهرمون. هذا يسمح بتنظيم مستويات الهرمون في الدم ضمن نطاق ضيق. مثال على حلقة التغذية الراجعة السلبية هو إطلاق هرمونات الجلوكوكورتيكويد من الغدد الكظرية، وفقًا لتوجيهات منطقة ما تحت المهاد والغدة النخامية. مع ارتفاع تركيزات الجلوكوكورتيكويد في الدم، تقلل منطقة ما تحت المهاد والغدة النخامية من الإشارة إلى الغدد الكظرية لمنع إفراز الجلوكوكورتيكويد الإضافي (الشكل\(\PageIndex{4}\)).
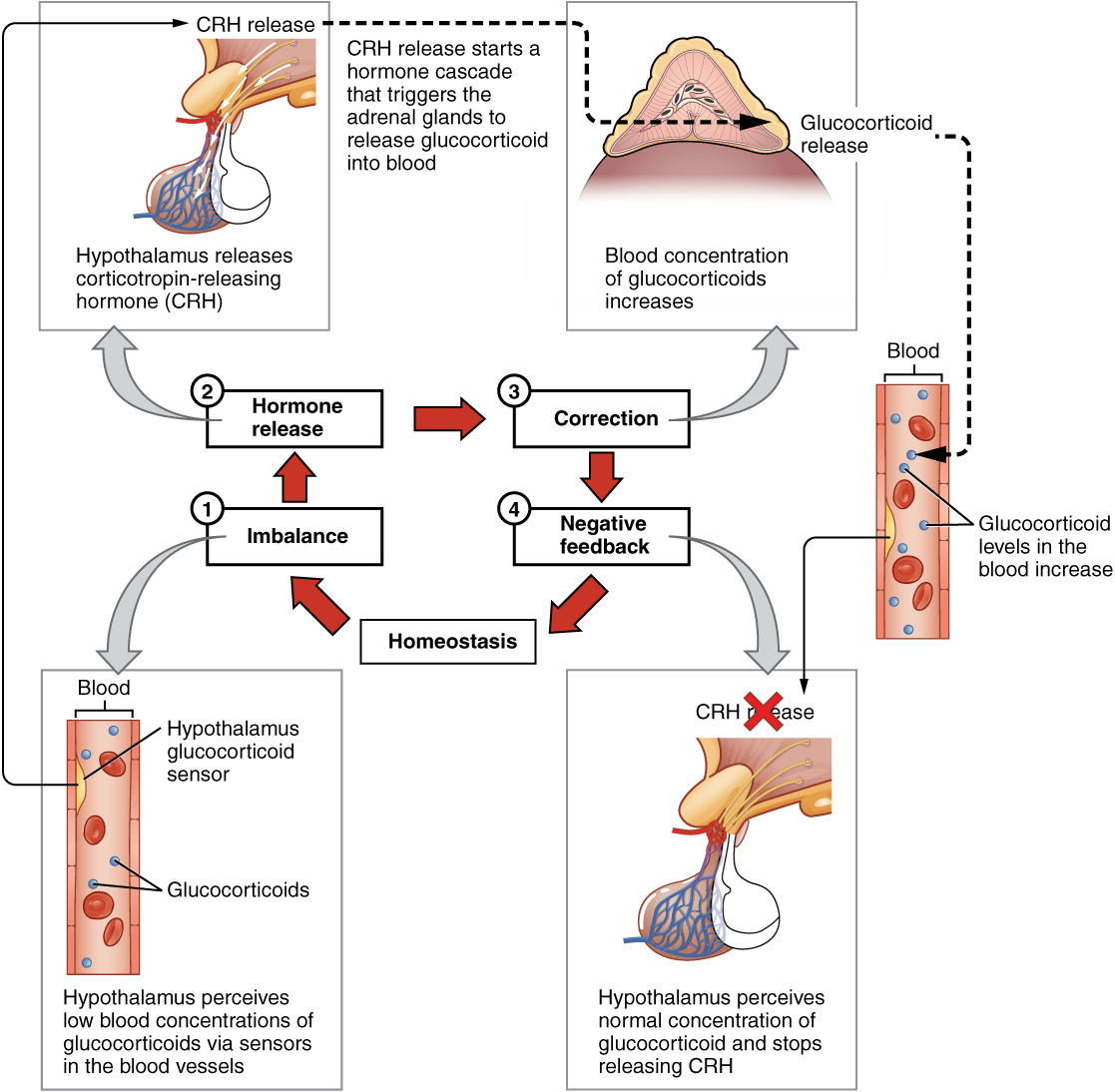
دور محفزات الغدد الصماء
تتحكم ردود الفعل الناتجة عن المنبهات الكيميائية والعصبية في نشاط الغدد الصماء. قد تكون ردود الفعل هذه بسيطة، حيث تتضمن استجابة هرمونية واحدة فقط، أو قد تكون أكثر تعقيدًا وتتضمن العديد من الهرمونات، كما هو الحال مع التحكم المهاد في العديد من الهرمونات التي تسيطر عليها الغدة النخامية الأمامية.
المنبهات الخلطية هي تغيرات في مستويات الدم للمواد الكيميائية غير الهرمونية، مثل العناصر الغذائية أو الأيونات، والتي تتسبب في إطلاق هرمون أو تثبيطه، بدوره، للحفاظ على التوازن. على سبيل المثال، تكتشف المستقبلات التناضحية في منطقة ما تحت المهاد التغيرات في الأسمولية الدموية (تركيز المواد المذابة في بلازما الدم). إذا كانت الأسمولية في الدم مرتفعة جدًا، مما يعني أن الدم ليس مخففًا بدرجة كافية، فإن مستقبلات الأسموستبلات تشير إلى منطقة ما تحت المهاد لإطلاق هرمون ADH. يتسبب الهرمون في قيام الكلى بإعادة امتصاص المزيد من الماء وتقليل حجم البول المنتج. يؤدي إعادة الامتصاص هذه إلى انخفاض الأسمولية في الدم، مما يؤدي إلى تمييع الدم إلى المستوى المناسب. تنظيم جلوكوز الدم هو مثال آخر. يؤدي ارتفاع مستويات الجلوكوز في الدم إلى إطلاق الأنسولين من البنكرياس، مما يزيد من امتصاص الجلوكوز بواسطة الخلايا وتخزين الكبد للجلوكوز في صورة جليكوجين.
قد تفرز الغدد الصماء أيضًا هرمونًا استجابةً لوجود هرمون آخر تنتجه غدة صماء مختلفة. غالبًا ما تتضمن هذه المحفزات الهرمونية منطقة ما تحت المهاد، التي تنتج هرمونات تفرز وتثبط الهرمونات التي تتحكم في إفراز مجموعة متنوعة من هرمونات الغدة النخامية.
بالإضافة إلى هذه الإشارات الكيميائية، يمكن أيضًا إطلاق الهرمونات استجابة للمنبهات العصبية. من الأمثلة الشائعة للمنبهات العصبية تنشيط استجابة القتال أو الطيران من قبل الجهاز العصبي الودي. عندما يرى الفرد خطرًا، ترسل الخلايا العصبية السمبثاوية إشارة إلى الغدد الكظرية لإفراز النوربينفرين والإيبينيفرين. يعمل الهورمونان على توسيع الأوعية الدموية وزيادة معدل ضربات القلب والجهاز التنفسي وقمع الجهاز الهضمي والجهاز المناعي. تعمل هذه الاستجابات على تعزيز نقل الجسم للأكسجين إلى الدماغ والعضلات، وبالتالي تحسين قدرة الجسم على القتال أو الفرار.
التوصيلات اليومية: بيسفينول أ واضطراب الغدد الصماء
ربما سمعت تقارير إخبارية عن تأثيرات مادة كيميائية تسمى bisphenol A (BPA) في أنواع مختلفة من عبوات المواد الغذائية. يستخدم BPA في تصنيع البلاستيك الصلب وراتنجات الايبوكسي. تشمل العناصر الشائعة المتعلقة بالطعام والتي قد تحتوي على BPA بطانة علب الألمنيوم، وحاويات تخزين الطعام البلاستيكية، وأكواب الشرب، وكذلك زجاجات الأطفال وأكواب «الشرب». تشمل الاستخدامات الأخرى لـ BPA المعدات الطبية وحشوات الأسنان وبطانة أنابيب المياه.
تشير الأبحاث إلى أن مادة BPA هي مادة مسببة لاختلال الغدد الصماء، مما يعني أنها تتداخل سلبًا مع نظام الغدد الصماء، خاصة خلال فترة النمو قبل الولادة وبعدها. على وجه الخصوص، يحاكي BPA التأثيرات الهرمونية لهرمون الاستروجين وله تأثير معاكس—تأثير الأندروجينات. تشير إدارة الغذاء والدواء الأمريكية (FDA) في بيانها حول سلامة BPA إلى أنه على الرغم من أن دراسات السموم التقليدية قد دعمت سلامة المستويات المنخفضة من التعرض لـ BPA، إلا أن الدراسات الحديثة التي تستخدم أساليب جديدة لاختبار التأثيرات الدقيقة أدت إلى بعض القلق بشأن الآثار المحتملة لـ BPA على الدماغ والسلوك وغدة البروستاتا لدى الأجنة والرضع والأطفال الصغار. تعمل إدارة الغذاء والدواء الأمريكية حاليًا على تسهيل تقليل استخدام BPA في المواد المتعلقة بالأغذية. قامت العديد من الشركات الأمريكية بإزالة مادة BPA طواعية من زجاجات الأطفال وأكواب «الشرب» وبطانات علب حليب الأطفال، وتفتخر معظم زجاجات المياه البلاستيكية القابلة لإعادة الاستخدام التي تُباع اليوم بأنها «خالية من BPA». في المقابل، حظرت كل من كندا والاتحاد الأوروبي تمامًا استخدام BPA في منتجات الأطفال.
تمت دراسة الآثار الضارة المحتملة لـ BPA في كل من النماذج الحيوانية والبشر وتشمل مجموعة كبيرة ومتنوعة من الآثار الصحية، مثل تأخر النمو والمرض. على سبيل المثال، قد يرتبط التعرض قبل الولادة لـ BPA خلال الأشهر الثلاثة الأولى من الحمل البشري بالصفير والسلوك العدواني أثناء الطفولة. قد يعاني البالغون المعرضون لمستويات عالية من BPA من تغيير إشارات الغدة الدرقية والخلل الجنسي عند الذكور. وقد لوحظ أن التعرض لـ BPA خلال فترة ما قبل الولادة أو ما بعد الولادة من التطور في النماذج الحيوانية يسبب تأخيرات عصبية وتغيرات في بنية الدماغ ووظيفته والخلل الجنسي والربو وزيادة خطر الإصابة بسرطانات متعددة. أظهرت الدراسات المختبرية أيضًا أن التعرض لـ BPA يسبب تغيرات جزيئية تبدأ في تطور سرطانات الثدي والبروستاتا والدماغ. على الرغم من أن هذه الدراسات قد ورطت BPA في العديد من الآثار الصحية السيئة، إلا أن بعض الخبراء يحذرون من أن بعض هذه الدراسات قد تكون معيبة وأنه يجب إجراء المزيد من الأبحاث. في غضون ذلك، توصي إدارة الغذاء والدواء (FDA) المستهلكين باتخاذ الاحتياطات اللازمة للحد من تعرضهم لـ BPA. بالإضافة إلى شراء الأطعمة في عبوات خالية من BPA، يجب على المستهلكين تجنب حمل أو تخزين الأطعمة أو السوائل في زجاجات باستخدام رمز إعادة التدوير 3 أو 7. يجب عدم تسخين الأطعمة والسوائل في الميكروويف بأي شكل من أشكال البلاستيك: استخدم الورق أو الزجاج أو السيراميك بدلاً من ذلك.
مراجعة الفصل
يتم اشتقاق الهرمونات من الأحماض الأمينية أو الدهون. تنشأ الهرمونات الأمينية من الأحماض الأمينية التربتوفان أو التيروزين. تشمل هرمونات الأحماض الأمينية الكبيرة الببتيدات وهرمونات البروتين. يتم اشتقاق هرمونات الستيرويد من الكوليسترول.
هرمونات الستيرويد وهرمون الغدة الدرقية قابلة للذوبان في الدهون. جميع الهرمونات الأخرى المشتقة من الأحماض الأمينية قابلة للذوبان في الماء. الهرمونات الكارهة للماء قادرة على الانتشار عبر الغشاء والتفاعل مع مستقبلات داخل الخلايا. في المقابل، يجب أن تتفاعل الهرمونات المحبة للماء مع مستقبلات غشاء الخلية. ترتبط هذه عادةً ببروتين G، الذي يتم تنشيطه عندما يربط الهرمون المستقبل. يؤدي ذلك إلى بدء سلسلة إشارات تتضمن مرسلًا ثانيًا، مثل أحادي فوسفات الأدينوزين الدوري (CaMP). تعمل أنظمة المراسلة الثانية على تضخيم إشارة الهرمون بشكل كبير، مما يخلق استجابة أوسع وأكثر كفاءة وأسرع.
يتم إطلاق الهرمونات عند التحفيز الذي يكون من أصل كيميائي أو عصبي. يتم تنظيم إطلاق الهرمونات في المقام الأول من خلال ردود الفعل السلبية. قد تتسبب المنبهات المختلفة في إفراز الهرمونات، ولكن هناك ثلاثة أنواع رئيسية. المنبهات الخلطية هي تغيرات في مستويات الأيونات أو العناصر الغذائية في الدم. المنبهات الهرمونية هي تغيرات في مستويات الهرمونات التي تبدأ أو تمنع إفراز هرمون آخر. أخيرًا، يحدث التحفيز العصبي عندما تؤدي النبضات العصبية إلى إفراز هرمون أو تثبيطه.
مراجعة الأسئلة
س: لوحظ أن مبيد الآفات المطور حديثًا يرتبط بمستقبلات هرمون داخل الخلايا. في حالة الابتلاع، يمكن أن تؤدي بقايا هذا المبيد إلى تعطيل مستويات ________.
أ. الميلاتونين
ب. هرمون الغدة الدرقية
C. هرمون النمو
د. الأنسولين
الإجابة: ب
س: يرتبط جزيء صغير ببروتين G، مما يمنع تنشيطه. ما التأثير المباشر الذي سيحدثه ذلك على الإشارات التي تتضمن CamP؟
ج: لن يكون الهرمون قادرًا على الارتباط بمستقبلات الهرمون.
لن يتم تنشيط B. لن يتم تنشيط أدينيل سيكلاز.
ج- سيتم إنتاج كميات مفرطة من CamP.
د- سيتم البدء في سلسلة الفسفرة.
الإجابة: ب
س: يتعرض الطالب لحادث سيارة، وعلى الرغم من عدم إصابته، فإنه يعاني على الفور من اتساع حدقة العين وزيادة معدل ضربات القلب والتنفس السريع. ما نوع تحفيز نظام الغدد الصماء الذي حصل عليه الطالب؟
أ. خلقي
ب. هرموني
C. عصبي
د. ردود فعل إيجابية
الإجابة: ج
أسئلة التفكير النقدي
س: قارن وقارن بين أحداث إرسال الإشارات المتضمنة في المرسلين الثانيين CamP و IP 3.
ج: في كل من CamP و IP 3 - إشارات الكالسيوم، يرتبط الهرمون بمستقبلات هرمون غشاء الخلية المقترن ببروتين G. يتم تنشيط بروتين G عندما يرتبط الهرمون. في حالة إرسال إشارات CamP، ينشط بروتين G المنشط أدينيل سيكلاز، مما يؤدي إلى تحويل ATP إلى CamP. يمكن لهذا الرسول الثاني بعد ذلك بدء أحداث إرسال إشارات أخرى، مثل سلسلة الفسفرة. في حالة إشارات IP 3 —الكالسيوم، ينشط بروتين G المنشط فوسفوليباز C، الذي يشق مركب فوسفوليبيد الغشائي إلى DAG و IP 3. يتسبب IP 3 في إطلاق الكالسيوم، وهو ناقل ثانٍ آخر، من المتاجر داخل الخلايا. يؤدي هذا إلى مزيد من أحداث الإشارة.
س: وصف آلية الاستجابة الهرمونية الناتجة عن ارتباط الهرمون بمستقبلات داخل الخلايا.
ج: يوجد مستقبل هرمون داخل الخلية. ينتشر هرمون كاره للماء عبر غشاء الخلية ويرتبط بمستقبلات الهرمون داخل الخلايا، والتي قد تكون في السيتوسول أو في نواة الخلية. يرتبط مركب مستقبلات الهرمون هذا بجزء من الحمض النووي. يؤدي هذا إلى نسخ الجين المستهدف، والنتيجة النهائية لذلك هي تجميع البروتين والاستجابة الهرمونية.
مسرد المصطلحات
- أدينيل سيكلاز
- إنزيم مرتبط بالغشاء يحول ATP إلى AMP دوري، مما يؤدي إلى تكوين CamP، نتيجة تنشيط بروتين G
- أحادي فوسفات الأدينوزين الدوري (CamP)
- المرسل الثاني الذي يؤدي، استجابة لتنشيط سيكلاز أدينيل، إلى سلسلة من الفسفرة
- دياسيل جليسرول (DAG)
- جزيء، مثل CamP، ينشط كينازات البروتين، وبالتالي يبدأ سلسلة من الفسفرة
- التنظيم الهابط
- انخفاض في عدد مستقبلات الهرمون، عادة استجابة لمستويات مفرطة مزمنة من الهرمون
- أول رسول
- هرمون يرتبط بمستقبلات هرمون غشاء الخلية ويؤدي إلى تنشيط نظام المراسلة الثاني
- بروتين جي
- بروتين مرتبط بمستقبلات هرمون غشاء الخلية الذي يبدأ الخطوة التالية في نظام المراسلة الثاني عند التنشيط عن طريق ربط الهرمونات والمستقبلات
- مستقبلات هرمون
- بروتين داخل الخلية أو على غشاء الخلية الذي يربط الهرمون، مما يؤدي إلى بدء استجابة الخلية المستهدفة
- إينوزيتول ثلاثي الفوسفات (IP 3)
- الجزيء الذي يبدأ إطلاق أيونات الكالسيوم من المخازن داخل الخلايا
- فوسفوديستراس (PDE)
- إنزيم السيتوسوليك الذي يعطل ويحلل CamP
- سلسلة الفسفرة
- حدث إرسال الإشارات حيث تقوم كينازات البروتين المتعددة بتفسور ركيزة البروتين التالية عن طريق نقل مجموعة الفوسفات من ATP إلى البروتين
- بروتين كيناز
- الإنزيم الذي يبدأ سلسلة الفسفرة عند التنشيط
- رسول ثاني
- الجزيء الذي يبدأ سلسلة إشارات استجابة لربط الهرمونات على مستقبل غشاء الخلية وتنشيط بروتين G
المساهمون والصفات
- upregulation
- increase in the number of hormone receptors, typically in response to chronically reduced levels of a hormone
- Template:ContribOpenStaxAP


