3.2: אנזימים
- Page ID
- 208486
זרזים ביולוגיים נקראים אנזימים, והרוב המכריע של האנזימים הם חלבונים. היוצאים מן הכלל הם סוג של מולקולות RNA הידועות בשם ריבוזימים, שרובן פועלות על עצמן (כלומר חלק מגדיל ה- RNA הוא מצע לחלק הריבוזים של הגדיל). בספר זה (וברוב ספרי הלימוד בתחום זה), אלא אם צוין אחרת, המונח אנזים מתייחס לאחד העשוי מחלבון. אנזימים מעניקים ספציפיות יוצאת דופן לתגובה כימית: תגובה שעלולה להתרחש בין מגוון מצעים פוטנציאליים במצב לא מזורז עשויה להיות מותרת רק בין שני מצעים ספציפיים כאשר היא מזורזת על ידי אנזים. אנזימים מאפשרים לתאים להפעיל תגובות כימיות בקצב של מיליון עד אפילו טריליון פעמים מהר יותר מאשר אותן תגובות היו פועלות בתנאים דומים ללא אנזימים. במקרים מסוימים, האנזימים al - תגובות נמוכות להמשך שבדרך כלל (כלומר ללא אנזים) דורשות טמפרטורה קיצונית יותר, לחץ או חומציות/בסיסיות. לבסוף, ואולי הכי חשוב לכל החיים, ניתן לווסת אנזימים. זה חיוני לתא, מכיוון שהוא חייב להיות מסוגל להגיב למצבים שונים, כגון זמינות אנרגיה, הצטברות של תוצרי לוואי רעילים, הצורך להתרבות וכו 'לא רק שניתן לשנות אנזימים באופן קוולנטי או לא קוולנטי כדי להגדיל או להקטין את פעילותם, התא יכול גם לווסת את ייצור האנזימים, ולספק רמה נוספת של שליטה על תגובות ביוכימיות תאיות מסוימות.
אנזימים קוטלגו וסווגו מאז שנות החמישים, ובמהלכם היה פיצוץ של תגליות אנזימים וצורך במינוח ובקטלוג מאוחד. הוקמה ועדה בינלאומית לאנזימים וכך החלה את רשימת האנזימים. לכל האנזימים יש כיום שמות מומלצים לשימוש נפוץ, המשקפים לעתים קרובות שמות היסטוריים, וגם שם שיטתי, שהוא מאוד ספציפי. יש להם גם מספר סיווג המבוסס על פעילותם. המחלקות העיקריות של אנזימים הן
- אוקסידורדוקטאזות המבצעות תגובות להפחתת חמצון,
- העברות המעבירות קבוצות פונקציונליות,
- הידרולאזים המבצעים תגובות הידרוליזה,
- ליאזות המבטלות קבוצות ליצירת קשרים כפולים,
- איזומראזות המסדרות מחדש את הקשרים במולקולה אך אינן מוסיפות או מסירות אטומים, ו
- ליגאזות היוצרות קשרים בתגובות המחוברות להידרוליזה של ATP.
כדוגמה, ליגאז DNA (שם מומלץ) מזרז יצירת קשר פוספודיסטר בין קצה 3' של שבר DNA אחד לקצה 5' של אחר. שמו השיטתי הארוך והמייגע למדי הוא "פולי (דאוקסיריבונוקלאוטיד) :פולי (דאוקסיר איבונוקלאוטיד) ליגאז (יוצר AMP)" ומספר הסיווג שלו הוא 6.5.1.1. בתור ליגאז, זה מחלקה 6; מכיוון שהוא יוצר קשרי אסטר זרחניים, זהו תת-מחלקה 5; תת-המשנה של 1 במקרה זה חסרת משמעות מכיוון שהיא תת-המחלקה היחידה של ליגאזות יוצרות קשר זרחן, אך המספר הסופי מייעד את ליגאז ה- DNA בנפרד מאנזימים אחרים של 6.5.1 כמו ליגאז RNA, שהוא 6.5.1.3.
אנזימים הם סוג החלבון המגוון ביותר בתא. הם משתנים לא רק בגודלם, אלא גם במספר יחידות המשנה המיוצרות באופן עצמאי שחייבות להתאחד כדי ליצור אנזים פעיל, או הולואנזים. חלק מהסיבה לדרוש כל כך הרבה אנזימים שונים היא שהם בדרך כלל מאוד ספציפיים למולקולות המצע שלהם, והספציפיות הזו מבוססת על שילוב של צורה ומטען. האינטראקציות בין מצע לאנזים משתווים לעתים קרובות למנעול ומפתח או לחתיכות פאזל. אם המצע מתאים לצורת האתר הפעיל של האנזים (החלק של האנזים שמבצע את התגובה הקטליטית בפועל), והמטענים מקיימים אינטראקציה (למשל חומצות אמינו טעונות חיוביות על האנזים בשורה עם מטענים שליליים על המצע), אז ייתכן שיש ייצוב נוסף של האינטראקציה על ידי ואן דר ואלס ואינטראקציות קשרי מימן. למעשה, היווצרות תוצר ביניים יציב של אנזים-מצע (ES) מקבילה אנרגטית למצב המעבר (איור\(\PageIndex{2}\)) של תגובות.
הספציפיות של אנזימים היא כזו שסטריאואיזומרים עשויים שלא להיות מוכרים על ידי אנזימים מסוימים: לדוגמה, פרוטאז (אנזימים הקוצצים חלבונים לחתיכות קטנות יותר על ידי הידרוליזה של קשרי הפפטיד בין חומצות אמינו ספציפיות) כגון טריפסין יכול להיות מעוכב על ידי נוכחות של חומצת אמינו D במקום חומצת האמינו L הרגילה בחלבון, למרות שמדובר בתמונת מראה של אותה חומצת אמינו ממש. ספציפיות זו פירושה שאנזימים הם סלקטיביים ביותר ביחס לתגובות שהם מזרזים, מה שאומר שניתן לשפר מאוד תגובות ספציפיות מבלי לגרום לעלייה כללית בתגובות כימיות רבות הקשורות. השלכה נוספת של הספציפיות הגבוהה היא שלאנזימים יכולה (ולעתים קרובות יש) זיקה גבוהה למצעים שלהם ללא בעיה של קשירת מולקולות שאינן סובסטרט (מלבד מעכבים ספציפיים - ראה להלן).
אם רוב התגובות הביוכימיות היו מתקדמות לאט במיוחד, אם בכלל, ללא קטליזה, יש צורך באנזימים כדי להוריד את אנרגיית ההפעלה הדרושה לתגובות כימיות לתמיכה בחיים. כיצד בדיוק אנזים מוריד את אנרגיית ההפעלה של תגובה? מה המשמעות של "אנרגיית הפעלה" בדיוק בהקשר של תא? כדי להבין זאת, ישנם שני עקרונות שכדאי לזכור: ראשית, כאשר אנו מדברים על תגובות כימיות, באופן כללי, אנו עוסקים באוכלוסיות של מולקולות מצע, מוצר ואנזים, ולא יחידים; ושנית, התגובות מתרחשות בדרך כלל בין מולקולות המומסות בציטופלזמה המימית של התא.
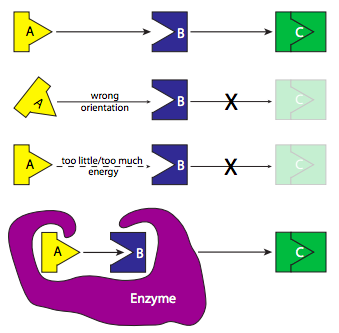
שקול תגובה שבה מצעים A ו- B מתקשרים ליצירת מוצר C (איור\(\PageIndex{3}\)). אם תגובה זו אינה מזורזת, זה תלוי במקרה שמולקולה של A נתקלת במולקולה של B בדיוק בכיוון הנכון, ובכמות האנרגיה הנכונה, כדי להגיב וליצור את המולקולה החדשה. אנו יכולים להמשיג את "אנרגיית ההפעלה" כקושי לחבר את A ו- B בצורה מושלמת כדי שהתגובה תוכל להמשיך. כיצד אנזים עשוי להוריד את אנרגיית ההפעלה הזו? על ידי הקלה על A ו- B למצוא אחד את השני עם הכיוון והאנרגיה הנכונים. כך שיכולים להיות לו אתרי קישור למולקולה A ומולקולה B, וברגע שהוא קשר את שתי המולקולות הללו, הוא משנה את הקונפורמציה שלו, ומפגיש את A ו-B בדיוק בתנאים הנכונים להגיב וליצור ג לאחר השלמת התגובה, המוצר צף מכיוון שלאנזים אין זיקה אליו, והאנזים חוזר לצורתו הראשונית, מוכן לקשור מצעים נוספים.
אנזימים עשויים גם להקל על תגובה כימית על ידי פעולה כאתר החזקה זמני לקבוצה פעילה המועברת ממצע אחד למשנהו. לחלופין, היווצרות זמנית של קשרי מימן או אפילו קשרים קוולנטיים בין האנזים למצע יכולה לשנות את המאפיינים הכימיים של המצע כדי לגרום לו להגיב ביתר קלות. דוגמה למנגנוני אנזים ברמה המולקולרית מוצגת בפרק 5: איור\(\PageIndex{1}\).
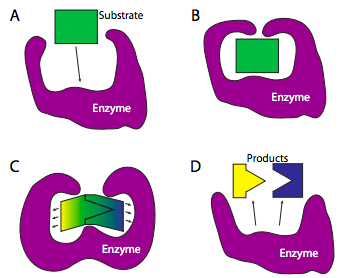
דוגמה נוספת עשויה להימצא עם אנזימים המפרקים מולקולה (איור\(\PageIndex{4}\)). על מנת שמולקולה תתפרק, יתכן שהיא תצטרך להתנגש במולקולה אחרת עם מספיק אנרגיה כדי לשבור אחד או יותר מהקשרים הקוולנטיים שלה. אנזים המזרז את תגובת הפירוק עשוי להיקשר למולקולה, ובקישור שלה, עובר שינוי קונפורמטיבי המכופף או מסובב את המולקולה בצורה כזו שהקשרים במולקולת המצע נחלשים או נשברים. שתי הדוגמאות הללו מפשטות יתר על המידה את הכימיה של פעילות האנזים לרעיון מכני, אך הקשר הכללי באופן שבו אנזים מוריד את אנרגיית ההפעלה לתגובה הוא מדויק.